NRR:南通大学王勇军教授团队揭示热热休克转录因子1激动剂修复损伤脊髓的潜力
撰文:何兵强,王勇军
成年哺乳动物脊髓损伤后难以再生,很大程度是由于神经元固有再生能力较低,以及损伤微环境中各种再生抑制因子的影响[1,2]。干预轴突生长相关分子或改善神经再生微环境,可以部分促进脊髓功能恢复,但效果甚微。比较生物学研究发现,一些成体低等脊椎动物如部分鱼类、两栖类和爬行类等,脊髓损伤后可以再生,并完全恢复神经支配功能 [3]。因此,研究低等脊椎动物自发性脊髓再生的分子机制,将为高等哺乳动物的脊髓再生提供重要参考[4-8]。热休克转录因子1(Heat shock transcription factor 1, HSF1)是动物在长期进化过程中形成的应对环境高温的应急保护因子。已有研究表明,激活HSF1有利于促进哺乳动物脊髓损伤后的修复过程[9],但哺乳动物脊髓损伤后HSF1的激活,具有时空局限性。爬行动物是进化中最靠近哺乳动物的低等羊膜生物,其中枢神经具备完全分化的神经元和胶质细胞。HSF1调控成体爬行动物损伤脊髓再生的细胞学基础以及相关分子机制尚不清楚。
近日,南通大学王勇军教授课题组在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“Heat shock factor 1 promotes neurite outgrowth and suppresses inflammation in the severed spinal cord of gecko”的研究论文。作者研究发现,爬行动物多疣壁虎脊髓损伤后,损伤信号诱导HSF1在神经元和小胶质细胞中表达。壁虎HSF1(gHSF1)抑制神经元中SOCS3的表达,促进神经元突起的生长;通过激活MER/ERK和PI3K/AKT信号通路,抑制caspase3的激活,促进神经元存活;调控IκB-α/NF-κB信号通路,抑制巨噬细胞炎症反应,改善损伤脊髓的炎性微环境。该研究为促进损伤脊髓的功能修复提供了新线索。何兵强为该论文第一作者,王勇军教授为论文通讯作者。
首先,作者通过构建多疣壁虎断尾脊髓损伤模型,检测了gHSF1在脊髓损伤后0 d、1 d、3 d、7 d和14 d的表达。结果发现,gHSF1在壁虎脊髓损伤后表达上调,且与NeuN阳性的神经元以及OX42阳性的小胶质细胞有共定位(图1),表明壁虎脊髓损伤后gHSF1参与调控神经元和小胶质细胞的生理作用,介导脊髓损伤修复过程。

图1 壁虎脊髓损伤后gHSF1在脊髓损伤处神经元和小胶质细胞中表达(图源:He et al., Neural Regen Res, 2023)
随后,作者构建了gHSF1过表达腺病毒Ad-gHSF1,并转染原代培养的壁虎神经元。发现壁虎神经元转染Ad-gHSF1 72h后,显著促进神经元突起的生长。接着,作者通过对再生相关基因进行分析,筛选和验证,证明HSF1通过抑制SOCS3转录,调控神经元突起的生长(图2)。
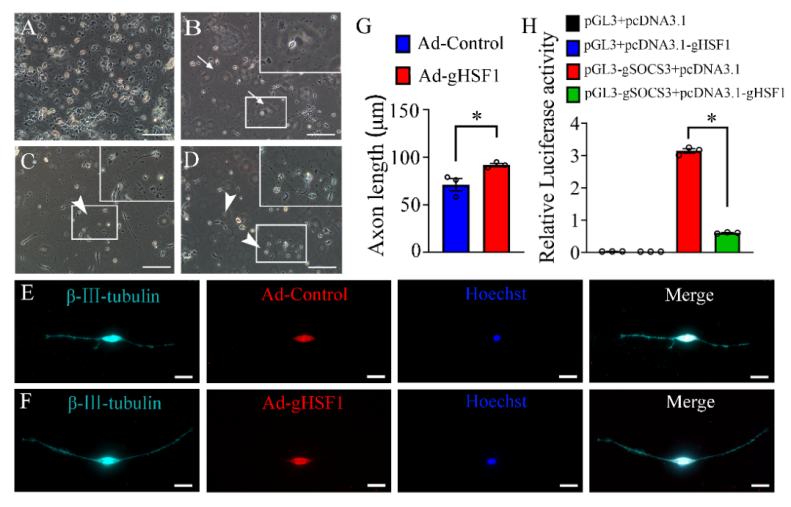
图2 过表达gHSF1促进壁虎神经元突起的生长(图源:He et al., Neural Regen Res, 2023)
为了进一步阐明gHSF1对神经元存活的影响,作者建立了神经元凋亡模型,结果发现神经元中过表达Ad-gHSF1可以抑制神经元凋亡。进一步研究表明,该促存活效应是通过激活MER/ERK和PI3K/AKT细胞存活信号通路、抑制凋亡蛋白caspase3的激活来实现的(图3)。
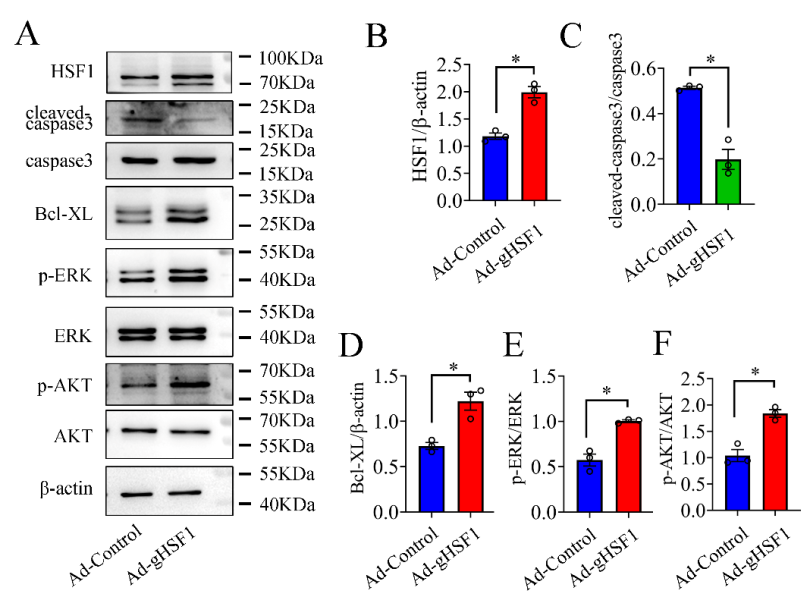
图3 gHSF1激活神经元中MER/ERK和PI3K/AKT细胞存活信号通路(图源:He et al., Neural Regen Res, 2022)
炎性微环境的形成往往不利于损伤脊髓的功能修复。为了进一步研究gHSF1对炎性微环境形成的影响,作者构建了巨噬细胞炎症反应激活模型。研究发现,巨噬细胞过表达Ad-gHSF1能够显著降低巨噬细胞中炎症因子的表达。进一步实验结果显示, gHSF1通过抑制IκB-α/NF-κB炎症信号通路,抑制炎症细胞的炎症反应的激活。该结果进一步证明了gHSF1能够抑制脊髓损伤后炎性微环境的形成(图4)。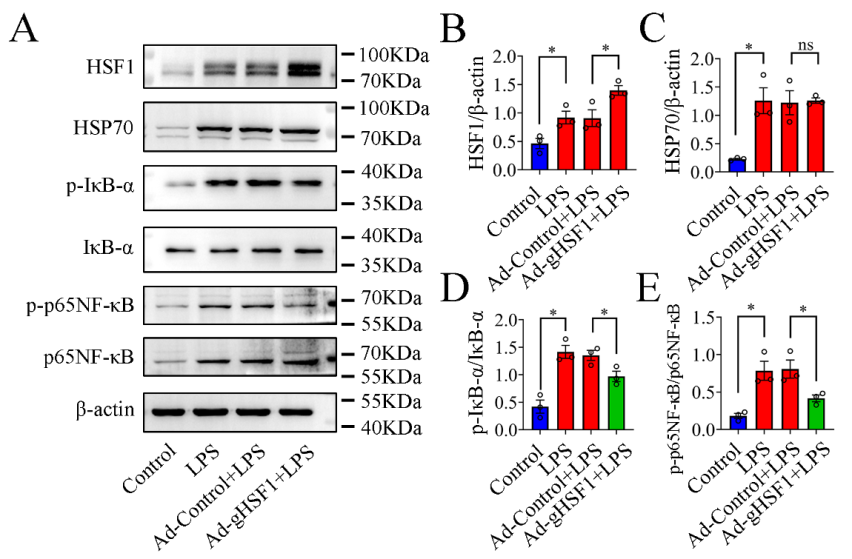
图4 gHSF1抑制巨噬细胞中IκB-α/NF-κB炎症信号通路(图源:He et al., Neural Regen Res, 2022)
总之,该研究揭示了HSF1在爬行动物脊髓损伤后参与调控神经元存活和轴突生长,以及抑制炎症微环境形成的双重作用。该研究为哺乳动物脊髓损伤修复提供了新的策略。当然该研究也存在一定的局限性,没有深入了解HSF1与髓鞘形成和星形胶质细胞反应之间的关系。总之,该研究为HSF1激动剂在修复损伤脊髓中的临床应用提供参考数据。
原文链接:https://doi.org/10.4103/1673-5374.366495
参考文献
[1] Steketee MB, Oboudiyat C, Daneman R, et al. Regulation of intrinsic axon growth ability at retinal ganglion cell growth cones. Invest Ophthalmol Vis Sci 2014;55:4369-4377.
[2] Sofroniew MV. Dissecting spinal cord regeneration. Nature 2018;557:343-350.
[3] Slack JM. Animal regeneration: ancestral character or evolutionary novelty? EMBO Rep 2017;18:1497-1508.
[4] Ma TC, Willis DE. What makes a RAG regeneration associated? Front Mol Neurosci 2015;8:43.
[5] Ineichen BV, Kapitza S, Bleul C, et al. Nogo-A antibodies enhance axonal repair and remyelination in neuro-inflammatory and demyelinating pathology. Acta Neuropathol 2017;134:423-440.
[6] Li H, He B, Zhang X, et al. D-dopachrome tautomerase drives astroglial inflammation via NF-kappaB signaling following spinal cord injury. Cell Biosci 2022;12:128.
[7] Muller F, De Virgiliis F, Kong G, et al. CBP/p300 activation promotes axon growth, sprouting, and synaptic plasticity in chronic experimental spinal cord injury with severe disability. PLoS Biol 2022;20:e3001310.
[8] Cheng Y, Yin Y, Zhang A, et al. Transcription factor network analysis identifies REST/NRSF as an intrinsic regulator of CNS regeneration in mice. Nat Commun 2022;13:4418.
[9] Li L, Li Y, He B, et al. HSF1 is involved in suppressing A1 phenotype conversion of astrocytes following spinal cord injury in rats. J Neuroinflammation 2021;18:205.
团队介绍

第一作者:何兵强(左一);通讯作者:王勇军教授(右一)
(照片提供自:南通大学神经再生重点实验室)
文章主要贡献者介绍、及基金支持等
本研究得到了国家自然科学基金(编号:31871211)的资助。




