NRR:武汉大学人民医院李明昌团队基因修饰牙髓干细胞移植治疗脑梗死的新方法
既往研究证明人类干细胞对缺血性脑卒中有潜在治疗作用。但是干细胞的在体内存活率低,导致发挥的作用有限。近期,武汉大学人民的李明昌团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“A valuable candidate gene for genetic modification of human dental pulp stem cells for the treatment of ischemic stroke: miR-34a”研究,通过将敲低miRNA-34a的慢病毒转染到牙髓干细胞中,构建了基因修饰的牙髓干细胞(anti34a-hDPSCs),观察了此干细胞的体外存活能力及揭示了部分机制,并通将anti34a-hDPSCs注入小鼠脑内,了解其对于缺血性脑卒中的治疗潜力。
研究背景#br#
1. 缺血性脑卒中是一种由脑血管闭塞引起的普遍的神经系统疾病,死亡率和发病率很高。尽管有适当的治疗,也会导致病人的残疾。重组组织蛋白酶原激活剂溶栓治疗和血管内血栓术是目前被批准的治疗这种疾病的医疗手段。#br#
2. 干细胞移植治疗缺血性脑卒中取得了快速进展。干细胞可以恢复神经功能,调节免疫反应,促进血管生成和神经再生。hDPSCs是间充质干细胞(MSCs)的一个亚型,起源于神经嵴。hDPSCs在小鼠tMCAO后具有功能恢复和减少梗死面积的效果,并具有伦理争议小和容易获得的优点。#br#
3. 在脑梗死的区域,炎症因子的释放和脑梗塞区活性氧(ROS)的产生降低了干细胞的存活率,导致干细胞治疗效果明显下降。因此,提高干细胞在体内的存活率已成为其临床应用的关键。基因修饰可以提高干细胞的体内存活率和功能。#br#
4. miRNA是由21-23个核苷酸组成的单链RNA分子。miR-34a是miR-34家族(miR-34a/b/c,miR-34s)的成员是第一个被发现直接受肿瘤抑制基因p53调节的miRNA。miR-34a被报道为对肿瘤细胞凋亡有抑制作用。#br#
5. WNT/β-catenin信号通路调节干细胞的多能性和更新,并维持干细胞数量。WNT1是触发WNT/β-catenin信号通路的WNT家族蛋白成员之一。SIRT1是一种去乙酰化酶,通过调节各种目标基因和蛋白质,在氧化应激损伤中发挥重要作用。SIRT1过表达能促进对氧化应激的抵抗力#br#
研究方法#br#
1. 将抑制miR-34a的慢病毒转染到牙髓干细胞中,构建基因修饰的的牙髓干细胞(anti34a-hDPSCs)。#br#
2. 评估anti34a-hDPSCs在体外的细胞活性,增殖情况,抗氧化应激能力,以及缺氧缺糖试验后的凋亡情况。#br#
3. 体外检测miR-34a对WNT1/β-catenin以及SIRT1/Nrf2/HO-1通路的影响,并通过双荧光素酶报告基因探索WNT1和SIRT1与miR-34a的作用方式#br#
4. 通过siRNA敲低anti34a-hDPSCs的WNT1以及SIRT1基因的表达,检测anti34a-hDPSCs在体外的细胞活性,增殖情况,抗氧化应激能力,以及缺氧缺糖试验后的凋亡情况。#br#
5. 将基因修饰的牙髓干细胞(anti34a-hDPSCs)注入脑梗死小鼠脑内,检测小鼠的运动功能、脑水肿、脑梗死及脑组织细胞凋亡情况。
结果表明,与普通牙髓干细胞相比,基因修饰的牙髓干细胞(anti34a-hDPSCs)在体外的增殖能力及抗氧化应激能力提高,并且是通过靶向结合在WNT1和SIRT1基因翻译的mRNA上,分别发挥促进增殖及促进抗氧化应激的功能。将基因修饰的牙髓干细胞(anti34a-hDPSCs)注入小鼠脑内后发现,anti34a-hDPSCs可显著抑制脑梗死后的细胞凋亡,脑水肿,降低脑梗死体积,改善小鼠的运动功能。
总结
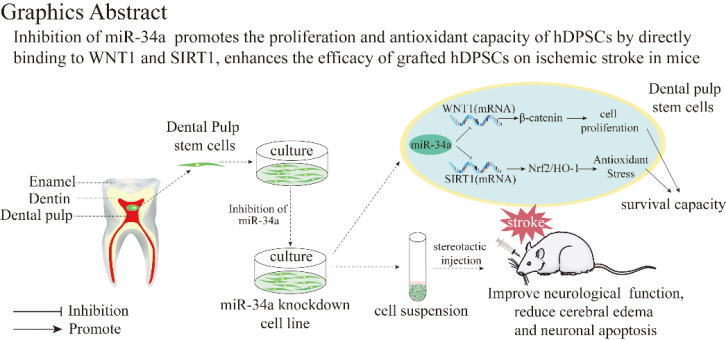
通过抑制牙髓干细胞的miR-34a可通过与WNT1和SIRT1翻译的mRNA结合,分别上调WNT1/β-catenin和SIRT1/Nrf2/HO-1信号通路,促进hDPSCs的增殖和抗氧化能力。hDPSC移植对缺血性脑卒小鼠中产生神经保护作用,特别是miR-34a敲除的hDPSCs。因此,miR-34a是干细胞基因修饰的一个有价值的候选基因,用于提高移植干细胞治疗缺血性脑卒中的疗效。
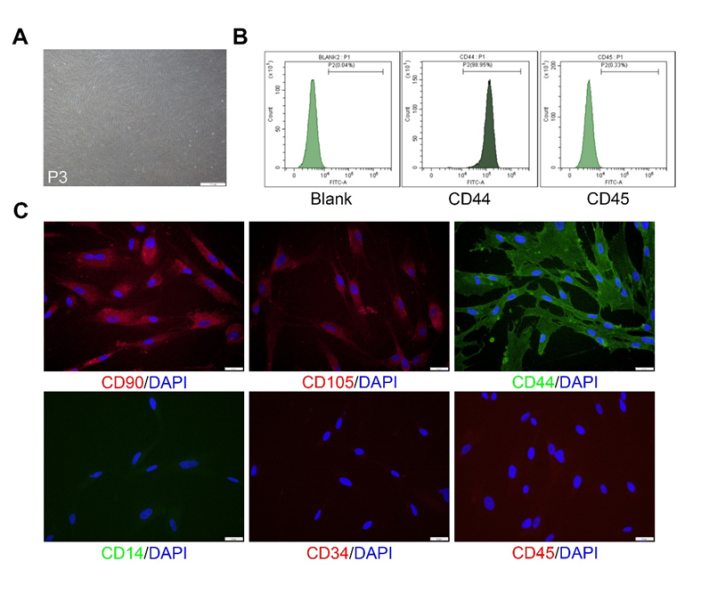
图1:牙髓干细胞的形态和鉴定(图源:Jian-Feng Wang et al., Neural Regen Res, 2023)
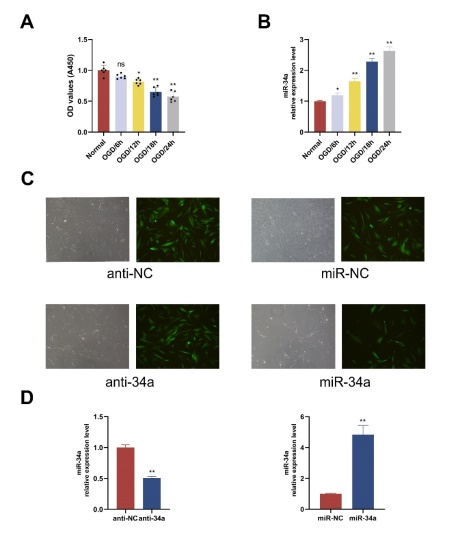
图2:OGD/R引起牙髓感谢的miR-34a上调以及构建基因修饰的牙髓干细胞(图源:Jian-Feng Wang et al., Neural Regen Res, 2023)

图3:抑制miR-34a抑制OGD/R引起的牙髓干细胞凋亡(图源:Jian-Feng Wang et al., Neural Regen Res, 2023)
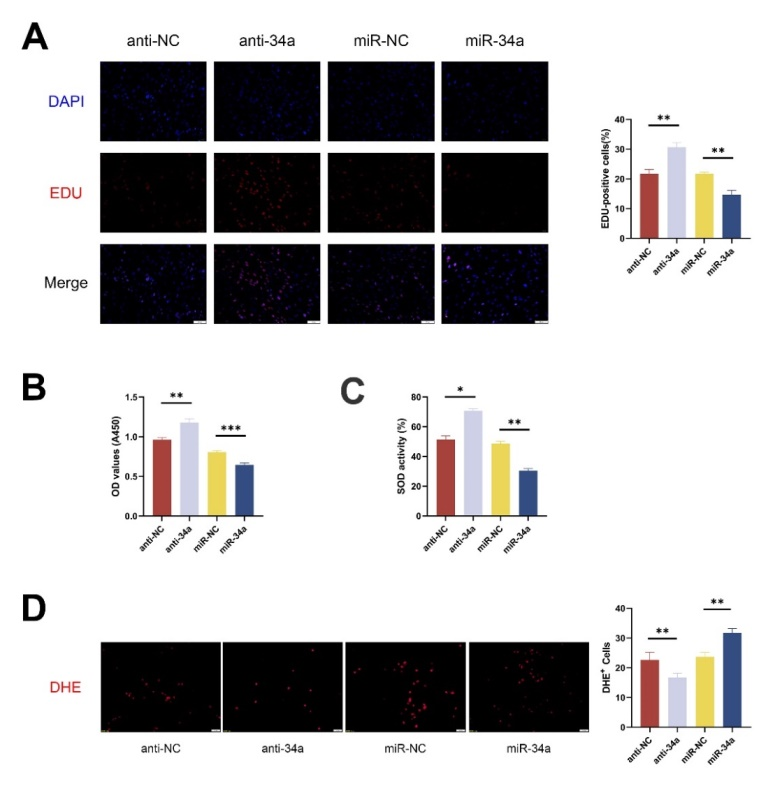
图4:抑制miR-34a提高牙髓干细胞活性,增强增殖能力及抗氧化应激能力(图源:Jian-Feng Wang et al., Neural Regen Res, 2023)
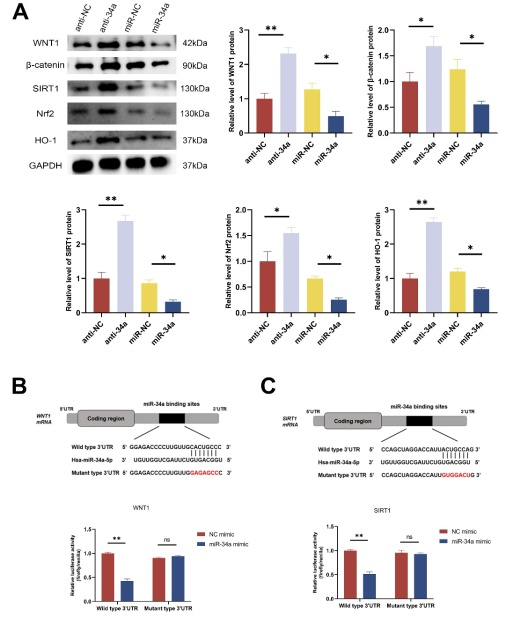
图5:抑制miR-34a通过靶向结合WNT1和SIRT1调控WNT1/β-catenin以及SIRT1/Nrf2/HO-1通路(图源:Jian-Feng Wang et al., Neural Regen Res, 2023)
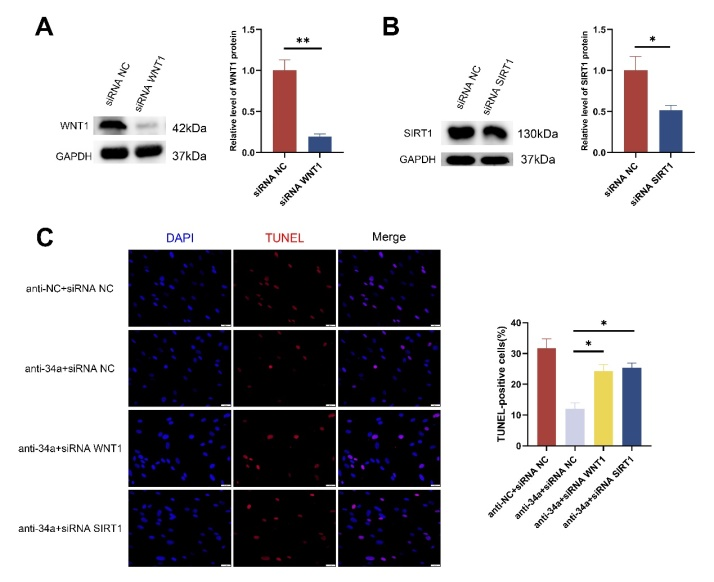
图6:敲低anti34a-hDPSCs的WNT1以及SIRT1基因的表达促进细胞凋亡 (图源:Jian-Feng Wang et al., Neural Regen Res, 2023)
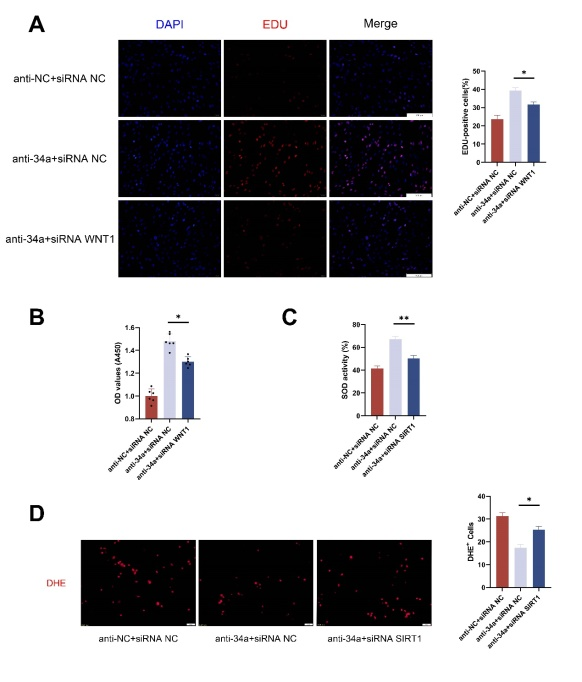
图7:敲低anti34a-hDPSCs的WNT1抑制细胞增殖,而敲低SIRT1抑制细胞的抗氧化应激能力(图源:Jian-Feng Wang et al., Neural Regen Res, 2023)

图8:anti34a-hDPSCs缓解tMCAO小鼠的组织学损伤,改善运动功能,缓解脑水肿,降低脑梗死体积(图源:Jian-Feng Wang et al., Neural Regen Res, 2023)
团队介绍
通讯作者:李明昌,主任医师/教授,博士生导师,长期致力于脑血管病的基础及临床研究,曾先后到美国、德国等全球先进的神经介入治疗中心进行研究学习,近年来主持并完成多项脑血管病课题,包括主持国家级课题基金4项,以第一作者或者通讯作者发表SCI收录的与脑血管病相关的论文20余篇,申请专利3项,以第一完成人获湖北省科技进步二等奖一项。2018年获中国神经外科最高荣誉奖项“王忠诚中国神经外科年度青年医师奖”。
共同通讯作者:叶青松,教授,博士生导师,拥有医学科学和口腔医学双博士学位,从事牙源性干细胞与再生医学研究以及错合畸形的临床矫治。在《Advanced Materials》、《Biomaterials》、《Nano Research》、《Stem Cells International》等杂志上发表了论文100余篇。参编卫生部研究生规划教材《循证口腔医学》。申请发明专利 7 项,实用新型专利1项,已授权3项;鉴于他的学术成就和影响力,他荣获2018Albert Nelson终身成就奖,被遴选为澳洲科研委员会及香港创新科技署基金评审专家库成员。
本文的第一作者王建丰,何沛邦为李明昌教授课题组的临床医学八年制博士。基金支持来自李明昌教授的国家自然科学基金(面上项目:82172173;81971870)

图片为通讯作者李明昌教授

图片为共同通讯作者叶青松教授










