NRR:脊髓损伤后神经与器官保护治疗研究领域新视野:“冬眠的力量”
撰文:陈旭义,刘彩芸
自然界中冬眠动物可以在寒冷漫长的冬季通过自主降低生理活动(排泄、饮食摄入)与生命体征(体温、代谢、心率、呼吸),在“静卧”长达数月之后复苏,肌肉骨骼力量并未大量丢失,机体器官功能与生理活动及其行为可以快速恢复至正常,无不惊叹“冬眠力量”的神奇,“人工冬眠”已逐渐成为近年研究热点。
脊髓损伤(Spinal cord injury,SCI)[1]可导致运动、感觉和自主神经功能的异常,是造成青年人残疾及死亡的主要因素之一。当前对于脊髓损伤多为对症支持治疗[2],SCI后神经与多器官保护治疗措施仍是临床SCI治疗研究领域需要解决的重要难题。有研究证实低温状态下对神经和器官具有积极保护作用[3-4]。推测人工冬眠技术对SCI后神经与多器官具有积极的治疗意义。
近期,武警特色医学中心陈旭义团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“The future of artificial hibernation medicine: protection of nerves and organs after spinal cord injury”的综述,通过总结低温与冬眠对器官与神经保护的相关研究证据,分析人工冬眠对于神经和多器官系统保护作用及可能机制(表1),为SCI后神经与多器官保护治疗研究提供新思路。
该综述将人工冬眠技术分为亚低温技术、冬眠诱导物和冬眠相关中枢神经调控技术,并进行相应介绍与研究进展的陈述。其中亚低温技术已应用于临床研究,并取得一定疗效,但是存在呼吸道并发症、肺部感染、凝血障碍、心动过缓并发症[3,5],以及无法避免机体对冷刺激的生理抵抗。人工冬眠技术中内源性冬眠诱导物和冬眠相关中枢神经调控技术通过激活特殊神经元,降低中枢恒温调定点,打破机体维持的正常恒温状态,形成中枢逆恒温调节,使机体“顺应”外界冷环境,减少冷刺激应激对神经和器官的损害。相比较亚低温技术的降温方式,或许更适用临床医疗,或通过对人工冬眠机制的研究以此发现新的治疗策略。近年来冬眠相关中枢神经调控技术诱导低温的研究在国内外已有相关报道[6-9],通过激活特定脑区实现哺乳动物体温降低,并在实验中发现动物会在cooling环境下会产生散热行为,推测这可能是由于特异性刺激中枢调温系统降低了中枢恒温调定点所引发的现象。冬眠诱导物包括内源性诱导物与人工合成诱导物。内源性诱导物来自冬眠动物血清中可以诱导休眠的物质,科学家发现血清中5`-单磷酸腺苷(5'-AMP)对腺苷A1受体(A1ARs)的激活在诱发休眠中具有重要意义[10],在低温环境下采用腺苷A1受体激动剂N6-cyclohexyladenosine (CHA)联合腺苷受体拮抗剂8-磺基苯基茶碱(8-SPT)(用以抵消心血管副作用)诱导休眠已取得了令人兴奋的结果[11]。然而,人工冬眠技术尚中除了亚低温技术应用于临床研究,其他技术还处在基础研究阶段,存在诸多待解决的技术缺陷。亚低温技术对治疗SCI的确切的有效性还需要大样本临床研究进行验证,冬眠诱导物技术与冬眠相关中枢神经调控技术需要高质量的研究报道。
陈旭义等通过对低温与冬眠对器官与神经保护的相关研究证据分析得出,人工冬眠技术可以通过降低体温实现对神经细胞的直接保护作用[12]。同时降低炎症因子水平,如IL-1β,IL-6和TNF-α,降低转化生长因子β2,减少IL-10的产生[13],缓解SCI后局部炎性反应,抑制凋亡因子[14]、轴突生长抑制因子的表达,达到保护神经细胞的目的。并通过降低白细胞[15]、适应性调节免疫细胞活跃的能力[16]、调控抗坏血酸浓度[17-18]、增加抗氧化剂水平[19](例如褪黑素),形成免疫抑制与氧化防御降,低缺血再灌注与氧化损伤实现对神经细胞的保护作用。此外,通过特异性刺激中枢形成中枢逆恒温调节,降低恒温点适应外界冷环境,保护神经与器官免受冷应激损害,过程中还可能产生中枢相关神经保护物质直接作用于受损神经(图1)。
人工冬眠技术不仅对神经具有积极的保护作用,还可以促进受损器官功能恢复与提高器官耐受不利环境的能力(图2)。i)呼吸和消化系统:肠、肝和肺存在相互影响的关系。冬眠状态下,肠道微生物发生改变,淋巴细胞、促炎因子水平增加,形成强大的免疫屏障保护[20],阻止SCI后菌群易位入血,进而保护肝脏与脆弱的肺脏[21-22]。此外,肝脏中乳酸脱氢酶释放量增加[23],提高了肝脏耐受性,并且H2S增加可降低机体耗氧与肺通气从而进一步保护肺脏[24-25]。ii)心血管系统:冬眠状态下胞内Ca2+稳态使心脏抵御室颤的能力增强[26]。并且低温可以通过阻断炎症相关受体,减缓SCI后自主神经反射异常引发的心血管损伤[27]。iii)运动系统:Ca2+稳态是冬眠状态下肌肉维持正常功能的重要机制[28],并且低温可以积极保护持骨骼肌细胞的功能与形态[29]。iv)泌尿系统:人工冬眠技术干预可以降低肾脏缺血再灌注引发的损伤[30],促进三磷酸腺苷(ATP)恢复[31],保护肾功能和组织结构。除了对器官存在有益作用,休眠状态下产生的内分泌物质可能对神经与器官具有治疗意义,例如:动物休眠期间褪黑素水平上升,研究发现褪黑素可以缓解氧化损伤,有利于减少缺血/再灌注引起氧化损伤,减轻炎症并发挥神经保护作用。
综上表明,人工冬眠技术对SCI后神经与器官保护治疗具有积极的意义。
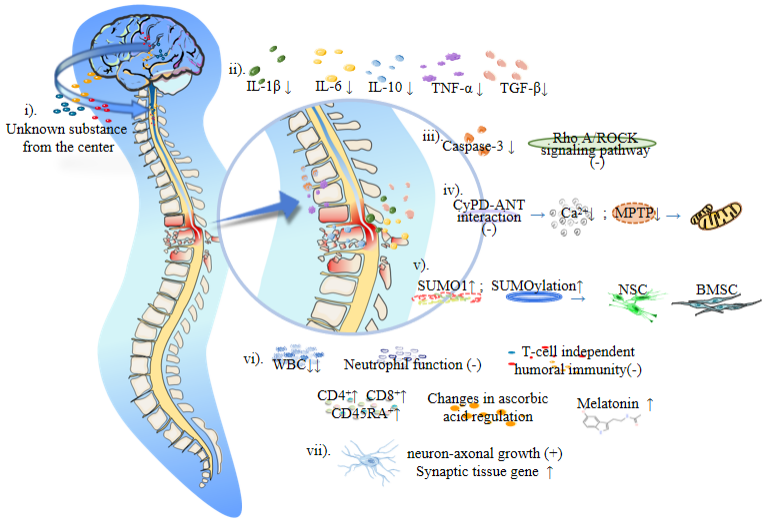
图1 人工冬眠对脊髓损伤神经保护作用机制

图2人工冬眠对器官的保护作用
不可否认的文章中所阐述的内容存在一定局限性。文章通过总结低温和冬眠对器官与神经保护的相关研究证据,分析得出人工冬眠对于SCI后神经和多器官系统保护作用及其相关机制,所得结果存在推测性。对此需要直接的研究证据作为基础,但冬眠诱导物与冬眠相关中枢神经调控技术在SCI中的研究还未见相关报道。对于人工冬眠技术还需要高质量、大样本研究的深入探索。
人工冬眠技术作为一种面向未来的颠覆性的生命保障和人体潜能激发技术,致力于调控机体自主进入休眠状态,极大降低冷刺激应激后引发的病理损伤,有助于SCI临床治疗与恢复。通过ⅰ)探究冬眠发生机制,发现并生产适用于人类的内源性冬眠诱导物质,实现人类冬眠,或通研究冬眠状态下动物的神经、器官、系统等保护作用机制,开发具有预防人类疾病的方法;ⅱ)明确参与诱导低温的脑区和神经核团,通过不同的中枢调温机制发现不同的神经保护机制一次发展多样的神经保护措施,这对于未来SCI后神经再生修复与器官保护医学研究具有巨大的潜在应用价值和科学意义。人工冬眠技术目前尚处于初级研究阶段,冬眠动物以及非冬眠动物的冬眠启动机制还未明确;对于人工冬眠干预后,中枢调控如何直接影响疾病的发展尚未清晰,以及人工冬眠状态下神经-免疫-内分泌系统如何调控机体内环境仍在研究中。任何事物都具有两面性,但这对于未来SCI救治医学研究与发展具有探索意义。
参考文献
[1]Ahuja CS, Wilson JR, Nori S, et al. Traumatic spinal cord injury. Nat Rev Dis Primers. 2017;3:17018.
[2]Huang H, Young W, Skaper S, et al. Clinical Neurorestorative Therapeutic Guidelines for Spinal Cord Injury (IANR/CANR version 2019). J Orthop Translat. 2020;20:14-24.
[3]Ransom SC, Brown NJ, Pennington ZA, et al. Hypothermia therapy for traumatic spinal cord injury: an updated review. J Clin Med. 2022;11:1585
[4]Shin HK, Park JH, Roh SW, et al. Meta-analysis on the effect of hypothermia in acute spinal cord injury. Neurospine. 2022;19:748-756.
[5]Darwazeh R, Yan Y. Mild hypothermia as a treatment for central nervous system injuries: Positive or negative effects. Neural Regen Res. 2013;8:2677-2686.
[6]Zhang Z, SHAN L, WANG Y, et al. Primate preoptic neurons drive hypothermia and cold defense[J]. Innovation (Camb). 2023;4:100358.
[7]Takahashi TM, Sunagawa GA, Soya S, et al. A discrete neuronal circuit induces a hibernation-like state in rodents. Nature. 2020;583:109-114.
[8]Hrvatin S, Sun S, Wilcox OF, et al. Neurons that regulate mouse torpor. Nature. 2020;583:115-121.
[9]Song K, Wang H, Kamm GB, et al. The TRPM2 channel is a hypothalamic heat sensor that limits fever and can drive hypothermia. Science. 2016;353:1393-1398.
[10]Muzzi M, Blasi F, Masi A, et al. Neurological basis of AMP-dependent thermoregulation and its relevance to central and peripheral hyperthermia. J Cereb Blood Flow Metab. 2013;33:183-190.
[11]Cerri M, Hitrec T, Luppi M, et al. Be cool to be far: Exploiting hibernation for space exploration. Neurosci Biobehav Rev. 2021;128:218-232.
[12]Wang HS, Han JS. Research progress on combat trauma treatment in cold regions. Mil Med Res. 2014;1:8.
[13]Han Z, Liu X, Luo Y, et al. Therapeutic hypothermia for stroke: Where to go? Exp Neurol. 2015;272:67-77.
[14]Li N, Chau C, Liu J, et al. Postcooling but not precooling benefits motor recovery by suppressing cell death after surgical spinal cord injury in rats. World Neurosurg. 2022;159:e356-364.
[15]Frerichs KU, Kennedy C, Sokoloff L, et al. Local cerebral blood flow during hibernation, a model of natural tolerance to "cerebral ischemia". J Cereb Blood Flow Metab. 1994;14:193-205.
[16]Bouma HR, Henning RH, Kroese FG, et al. Hibernation is associated with depression of T-cell independent humoral immune responses in the 13-lined ground squirrel. Dev Comp Immunol. 2013;39:154-160.
[17]Henry PG, Russeth KP, Tkac I, et al. Brain energy metabolism and neurotransmission at near-freezing temperatures: in vivo (1)H MRS study of a hibernating mammal. J Neurochem. 2007;101:1505-1515.
[18]Drew KL, Osborne PG, Frerichs KU, et al. Ascorbate and glutathione regulation in hibernating ground squirrels. Brain Res. 1999;851(1-2):1-8.
[19]Tan DX, Manchester LC, Sainz RM, et al. Physiological ischemia/reperfusion phenomena and their relation to endogenous melatonin production: a hypothesis. Endocrine. 2005;27:149-158.
[20]Kurtz CC, Otis JP, Regan MD, et al. How the gut and liver hibernate. Comp Biochem Physiol A Mol Integr Physiol. 2021;253:110875.
[21]Liu J, An H, Jiang D, et al. Study of bacterial translocation from gut after paraplegia caused by spinal cord injury in rats. Spine (Phila Pa 1976). 2004;29:164-169.
[22]Sun X, Jones ZB, Chen XM, et al. Multiple organ dysfunction and systemic inflammation after spinal cord injury: a complex relationship. J Neuroinflammation. 2016;13:260.
[23]Alva N, Bardallo RG, Basanta D, et al. Preconditioning-like properties of short-term hypothermia in isolated perfused rat liver (IPRL) system. Int J Mol Sci. 2018;19:1023.
[24]Heldmaier G, Ortmann S, Elvert R. Natural hypometabolism during hibernation and daily torpor in mammals. Respir Physiol Neurobiol. 2004;141:317-329.
[25]Jensen BS, Pardue S, Duffy B, et al. Suppression of mitochondrial respiration by hydrogen sulfide in hibernating 13-lined ground squirrels. Free Radic Biol Med. 2021;169:181-186.
[26]Li XC, Wei L, Zhang GQ, et al. Ca2+ cycling in heart cells from ground squirrels: adaptive strategies for intracellular Ca2+ homeostasis. PLoS One. 2011;6:e24787.
[27]Phillips AA, Krassioukov AV. Contemporary cardiovascular concerns after spinal cord injury: mechanisms, maladaptations, and management. J Neurotrauma. 2015;32:1927-1942.
[28]Fu W, Hu H, Dang K, et al. Remarkable preservation of Ca(2+) homeostasis and inhibition of apoptosis contribute to anti-muscle atrophy effect in hibernating Daurian ground squirrels. Sci Rep. 2016;6:27020.
[29]Martin LJ, Niedzwiecki MV, Wong M. Chronic intermittent mild whole-body hypothermia is therapeutic in a mouse model of ALS. Cells. 2021;10:320.
[30]Schleef M, Gonnot F, Pillot B, et al. Mild therapeutic hypothermia protects from acute and chronic renal ischemia-reperfusion injury in mice by mitigated mitochondrial dysfunction and modulation of local and systemic inflammation. Int J Mol Sci, 2022;23:9229.
[31]Yamamoto S, Yamamoto M, Nakamura J, et al. Spatiotemporal ATP dynamics during AKI predict renal prognosis. J Am Soc Nephrol. 2020;31:2855-2869.

