NRR:浙江大学虞军团队揭示Spi1是脑出血的潜在关键干预靶点
撰写:张国强,虞军
脑出血(Intracerebral hemorrhage,ICH) 是脑卒中最严重的类型之一,具有高发病率、高致残率、高死亡率等特点[1]。巨噬细胞和小胶质细胞局部浸润引起的神经炎症是脑出血后继发性损伤中影响ICH预后的关键因素[2]。Spi1作为编码PU.1的转录因子,在髓系和淋巴系细胞的发育中起着关键作用[3]。Spi1不仅可以促进巨噬细胞极化和成熟巨噬细胞存活[4],而且在中枢神经系统中,Spi1可以影响小胶质细胞转录组和表型改变[5-6],Spi1表达降低可引起小胶质细胞吞噬能力的降低[7-8],Spi1表达增加可促进酶蛋白吞噬增加[9]。在阿尔茨海默病中,Spi1可调节白细胞介素-33 (IL-33)的表达,诱导产生MHC-II+吞噬小胶质细胞,并增强小胶质细胞对β淀粉样蛋白的清除[10]。尽管Spi1在大脑中的部分功能已被证实,但其在脑出血中的作用仍未确定。研究Spi1对脑出血后小胶质细胞/巨噬细胞功能的影响,可以促进对脑出血继发性损失病理生理学的理解,并为其治疗提供更具体的靶点。
近期,浙江大学虞军团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“Spi1 regulates the microglial/macrophage inflammatory response via the PI3K/AKT/mTOR signaling pathway after intracerebral hemorrhage”的研究论文。通过研究,作者发现,Spi1可以通过调节小胶质细胞和巨噬细胞的功能来调节脑出血后的神经炎症反应和神经功能恢复。进一步研究表明,Spi1可能是通过调节PI3K/AKT/mTOR信号通路而改变小胶质细胞/巨噬细胞的转录组水平,进而促进细胞的吞噬作用。此外,高表达Spi1的小胶质细胞表现出更高水平的与神经功能恢复相关的细胞重构,包括糖酵解、髓鞘再生、血管生成和细胞凋亡等。该文带来的启示:Spi1可促进ICH后的小胶质细胞和巨噬细胞的吞噬作用,其可能在未来作为脑出血免疫相关的关键干预靶点。张国强为论文第一作者,虞军教授为论文通讯作者。
脑出血后,巨噬细胞和小胶质细胞局部浸润引起的神经炎症是引起继发性损伤的主要因素[2]。Spi1作为编码PU.1的转录因子,不仅可以促进巨噬细胞极化和成熟巨噬细胞存活[4],而且可以影响小胶质细胞转录组和表型改变[5-6]。然而Spi1对脑出血的影响尚不清楚。首先我们分析发现,小胶质细胞/巨噬细胞是脑出血后浸润脑实质的主要免疫细胞类型。Spi1作为脑出血后的关键转录因子,在脑出血后的表达水平显著升高(图1)。既往研究表明,Spi1可调节小胶质细胞转录组表达并增强其吞噬作用[9]。本研究的结果与之相符,我们发现Spi1的高表达与促进吞噬、糖酵解、自噬和髓鞘再生的通路有关,如PI3K/AKT/mTOR信号通路。进一步研究发现,Spi1可能会持续参与TREM2和FCGR1,并通过上游激活剂(如PI3K和Akt)诱导mTOR信号(图2)。在ICH小鼠高表达Spi1的小胶质细胞中,TGF-βR1/TGF-βR2和CSF1R的表达相似的增加,进一步证明了这一点。此外,高表达Spi1的小胶质细胞表现出更广泛的细胞重构改变,包括血管生成、补体激活和细胞凋亡等(图2)。

图1 脑出血后小胶质细胞内Spi1的表达水平显著升高(图源:GuoQiang Zhang et al., Neural Regen Res, 2023)
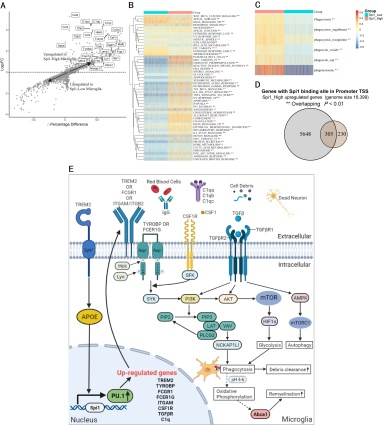
图2 Spi1通过调节PI3K/AKT/mTOR信号通路而促进小胶质细胞的吞噬作用(图源:GuoQiang Zhang, et al., Neural Regen Res, 2023)
总之,Spi1在脑出血后的小胶质细胞/巨噬细胞炎症反应中起着至关重要的作用。Spi1及其靶基因的调控可以促进我们对脑出血神经炎症的认识,并为脑出血的治疗提供潜在干预靶点。
当然该研究也存在一定的局限性。首先,该研究没有明确Spi1的敲除和过表达对ICH后小胶质细胞/巨噬细胞功能的影响。因此,需要进一步研究Spi1的表达变化与脑出血神经炎症之间的关系。其次,我们的研究结果主要是基于转录组数据确定的,因此,需要进一步的基础实验研究来证实研究的可靠性。其次,转录组测序数据本身在获取RNA和识别脑出血病理特异性靶基因的方法方面存在局限性,特别是在人类研究中。因此,该研究可能存在选择偏差。最后,该研究使用的数据集很小。因此,该研究结果的可靠性和有效性需要在进一步的纵向研究验证。
原文链接:https://doi.org/10.4103/1673-5374.375343
参考文献
1. Rosand J. Preserving brain health after intracerebral haemorrhage. Lancet Neurol. 2021;20:879-880.
2. Bai Q, Xue M, Yong VW. Microglia and macrophage phenotypes in intracerebral haemorrhage injury: therapeutic opportunities. Brain. 2020;143:1297-1314.
3. Anderson KL, Smith KA, Conners K, et al. Myeloid development is selectively disrupted in PU.1 null mice. Blood. 1998;91:3702-3710.
4. Karpurapu M, Wang X, Deng J, et al. Functional PU.1 in macrophages has a pivotal role in NF-κB activation and neutrophilic lung inflammation during endotoxemia. Blood. 2011;118:5255-5266.
5. Zhou N, Liu K, Sun Y, et al. Transcriptional mechanism of IRF8 and PU.1 governs microglial activation in neurodegenerative condition. Protein Cell. 2019;10:87-103.
6. Cakir B, Tanaka Y, Kiral FR, et al. Expression of the transcription factor PU.1 induces the generation of microglia-like cells in human cortical organoids. Nat Commun. 2022;13:430.
7. Smith AM, Gibbons HM, Oldfield RL, et al. The transcription factor PU.1 is critical for viability and function of human brain microglia. Glia. 2013;61:929-942.
8. Rustenhoven J, Smith AM, Smyth LC, et al. PU.1 regulates Alzheimer's disease-associated genes in primary human microglia. Mol Neurodegener. 2018;13:44
9. Pimenova AA, Herbinet M, Gupta I, et al. Alzheimer's-associated PU.1 expression levels regulate microglial inflammatory response. Neurobiol Dis. 2021;148:105217.
10. Lau SF, Chen C, Fu WY, et al. IL-33-PU.1 transcriptome reprogramming drives functional state transition and clearance activity of microglia in Alzheimer's disease. Cell Rep. 2020;31:107530.
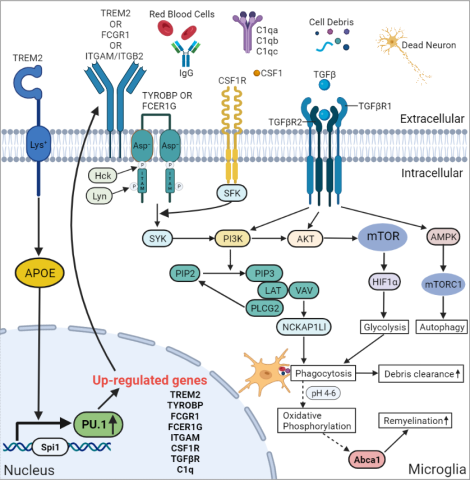
图示摘要(图源:GuoQiang Zhang, et al., Neural Regen Res, 2023)
主要贡献者介绍及基金支持
张国强为论文第一作者,虞军教授为论文通讯作者。研究受到国家自然科学基金(81971097)的资助。
虞军教授,主任医师,医学博士,博士生导师,神经外科病区主任,浙江省医师协会神经介入专委会总干事,毕业于浙江大学,擅长神经外科血管性疾病的综合手术治疗,学术研究方向为脑血管病的病理机制及治疗研究。

通讯作者虞军教授照片(照片由浙江大学医学院附属第二医院神经病学实验室提供)



