NRR:暨南大学师玲玲团队报道了一种能够在体外高效诱导分化中脑多巴胺能神经元的方案
撰文:陈亚兰,匡俊鑫,牛怡美,朱红谣,陈晓霞,苏国辉,徐安定,师玲玲
近期,暨南大学师玲玲团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“Multiple factors to assist human-derived induced pluripotent stem cells to efficiently differentiate into midbrain dopaminergic neurons”的研究论文。作者通过对诱导方案的两次优化,最终提出了一种通过多因素将人源诱导多能干细胞(human induced pluripotent stem cells,hiPSC)高效诱导分化为中脑多巴胺能神经元的方案。在hiPSC诱导过程中加入CHIR99021、SHH和FGF8结合双抑制剂SB431542和Dorsomorphin构建了三因子神经诱导方案。此方案诱导出的多巴胺能神经元中有31%-74%为中脑多巴胺能神经元,是一种高效的中脑多巴胺能神经元诱导方案,具有一定的临床治疗应用潜力。
多巴胺能神经元与运动、奖励、认知和情感等多种大脑功能调节有关。中脑多巴胺能神经元约占所有多巴胺能神经元的75%,由于这些神经元的大量损失或退化引起的脑区功能异常在神经退行性疾病如帕金森病等的发病机制中很重要[1]。生成特定类型神经元一直是再生医学领域一个主要研究目标,特别是可供移植的用于改善帕金森病患者运动障碍的中脑多巴胺能神经元。
近年来,关于中脑多巴胺能神经元诱导分化方面的研究已取得了巨大进展。采用双SMAD(Suppressor of Mother against Decapentaplegic)通路抑制剂能够将hiPSC高效分化为神经元,在体外产生能够表达多巴胺能神经元标记的细胞[2]。在神经元发育早期,有效形成底板细胞对中脑多巴胺能神经元的产生至关重要。人类胚胎干细胞在诱导早期暴露于高剂量的音猬因子(sonic hedgehog,SHH)能有效地诱导出功能性底板细胞[3]。而在人类胚胎干细胞诱导过程中加入糖原合成酶激酶3β的化学抑制剂(CHIR99021),能够诱导WNT信号的剂量依赖性激活,有效地引导人类胚胎干细胞向中脑腹侧发展,并产生大量底板祖细胞[4]。但是目前已有的神经元诱导方案所获得的中脑多巴胺能神经元比例较低,需要建立一种能够在体外高效诱导出中脑多巴胺能神经元的方案。
作者首先根据相关研究优化建立了SMAD信号双抑制剂方案(图1),从诱导开始到第8天使用5 μmol/L Dorsomorphin和5 μmol/L SB431542促进hiPSC的神经分化。加入双重抑制剂后,hiPSC开始分化为柱状上皮细胞。在第16天通过机械解离将细胞分离为大小均匀的簇状细胞进行悬浮培养形成神经前体细胞(Neural precursor cells,NPC)。悬浮培养阶段加入表皮生长因子(epidermal growth factor,EGF)和成纤维细胞生长因子(fibroblast growth factor,FGF)。NPC消化传代3次后接种到胶质细胞上,加入脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)和环磷酸腺苷(cyclic-AMP,c-AMP)使其进一步分化为神经元。作者发现使用优化后的诱导方案,在大约24天后成功将hiPSC诱导成神经元。
使用该方案能够将约84%的细胞诱导分化为多种亚型神经元,包括多巴胺能神经元、GABA能神经元和谷氨酸能神经元。然而该方案中多巴胺能神经元的分化效率较低,仅为21%(图2)。作者对诱导方案进行了进一步的优化,希望能够提高hiPSC向多巴胺能神经元分化的效率。
作者对SMAD信号双抑制剂方案进行了优化,构建了双因子SHH+FGF8诱导方案(图3),在添加双重抑制剂的基础上,于培养第8天往培养基中加入100 ng/mL SHH和100 ng/mL 成纤维细胞生长因子8(fibroblast growth factor 8,FGF8),直至NPC悬浮培养结束。为了保证多巴胺能神经元的存活率,在神经元分化阶段,补充添加20 ng/mL 胶质源性神经营养因子(glial cell-derived neurotrophic factor,GDNF)和0.2 mM 抗坏血酸(amino acid,AA)。
双因子SHH+FGF8诱导方案神经元分化效率约为83%,与优化前相比没有增加。然而,加入SHH和FGF8后,分化出的神经元中多巴胺能神经元的比例明显增加,达到约75%。作者将NPC消化为单细胞后使用DAT-Cherry转染6小时,随后在第33天通过免疫荧光染色检测所培养出神经元TH的表达。发现部分TH阳性神经元出现DAT信号,说明部分多巴胺能神经元已经分化至成熟阶段。同时作者发现该方案中仅部分多巴胺能神经元表现出中脑标志物FOXA2阳性(图4)。这表明在诱导方案中加入SHH和FGF8可以促进hiPSC向多巴胺能神经元的分化,并且可以分化出少量中脑多巴胺能神经元。然而与认知、高级情感和神经退行性疾病相关主要是中脑多巴胺能神经元,在此方案中诱导分化出的中脑多巴胺能神经元比例尚未令人满意,需要进一步优化。
作者再次优化诱导方案构建了三因子CHIR+SHH+FGF8诱导方案(图5)。在该方案中调整了SHH和FGF8添加时间,并且加入了2 μM SHH信号激动剂Purmorphamine和0.7 μM CHIR99021。作者发现调整后方案中诱导得到的NPC无法经过悬浮培养分化为神经元,因此后续改为平层培养。首先,作者将SHH、FGF8和Purmorphamine的添加时间提前为hiPSC诱导的第1天到第8天,减少了添加总天数,在一定程度上节省了试剂成本。其次,作者从诱导过程第3天到第13天添加0.7 μM CHIR99021。在分化后期,进行两次机械解离,以提高神经元分化效率。与之前方案不同,此方案中观察到类似于中脑神经嵴结构的形成。
三因子CHIR+SHH+FGF8诱导方案中,作者观察到hiPSC诱导分化至第6天时80%细胞表达FOXA2。说明该方案诱导出了高比例的底板细胞,这些细胞都被规范了中脑身份。与前两个悬浮培养方案相比,三因子CHIR+SHH+FGF8诱导方案中神经元分化效率有所下降,但分化效率也维持在75%。三因子诱导方案中诱导出的神经元约74%为多巴胺能神经元。同时作者发现加入CHIR99021诱导培养至第41天时,三因子CHIR+SHH+FGF8诱导方案与双因子SHH+FGF8诱导方案相比,更多的多巴胺能神经元能够被中脑标记物如FOXA2和PITX3标记。作者发现,在三因子 CHIR+SHH+FGF8诱导方案中的TH阳性神经元中约有31%与FOXA2共标记,而在双因子SHH+FGF8诱导方案中仅有15%与FOXA2共标记。在三因子 CHIR+SHH+FGF8诱导方案方案中,大约37%的TH阳性神经元与PITX3共标记,而在双因子SHH+FGF8诱导方案中只有7%与PITX3共标记。在作者构建的三因子CHIR+SHH+FGF8诱导方案中,培养至第6天时80%细胞表达FOXA2形成底板祖细胞,而在神经元阶段作者观察到TH阳性神经元即多巴胺能神经元占比为74%,但是TH与FOXA2共标的神经元仅占31%,TH与PITX3共标的神经元仅占37%。有研究表明,FOXA2对于决定细胞向腹侧中脑发育至关重要,除此之外在神经元形成过程中FOXA2是中脑多巴胺能神经元规范的关键。在中脑多巴胺能神经元成熟阶段并非所有神经元都表达FOXA2。而PITX3是准确诱导成熟中脑多巴胺能神经元的关键参与者,在成熟的中脑多巴胺能神经元中更多表达。因此无论是FOXA2还是PITX3都不足以单独定义所有的中脑多巴胺能神经元[6-7]。结合该方案中多巴胺能神经元占比为74%,作者推测该方案诱导的中脑多巴胺能神经元占比应该为31%-74%。与前两个方案相比显著上升(图6)。随后作者进行了电生理检测,结果显示所获得的神经元具有钠电流和超级化峰,符合多巴胺能神经元亚型特征(图7)。因此作者构建出的三因子CHIR+SHH+FGF8诱导方案能够高效诱导分化出中脑多巴胺能神经元,是一种稳定、有效的诱导方案,带来更多的临床应用可能性。
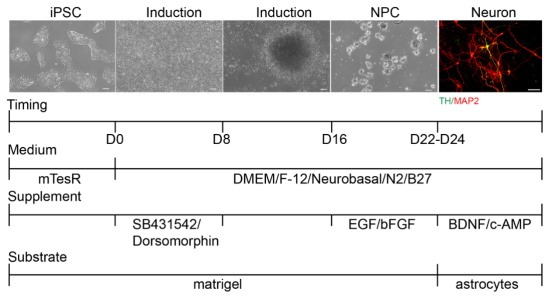
图1 SMAD信号双抑制剂方案流程图。
(图源:Yalan Chen et al., Neural Regen Res, 2024)

图2 SMAD信号双抑制剂方案能够诱导分化出多种亚型神经元,其中多巴胺能神经元占比较低。
(图源:Yalan Chen et al., Neural Regen Res, 2024)
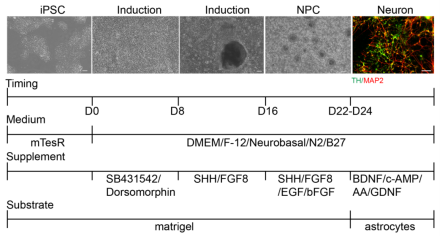
图3 双因子SHH+FGF8诱导方案流程图。
(图源:Yalan Chen et al., Neural Regen Res, 2024)
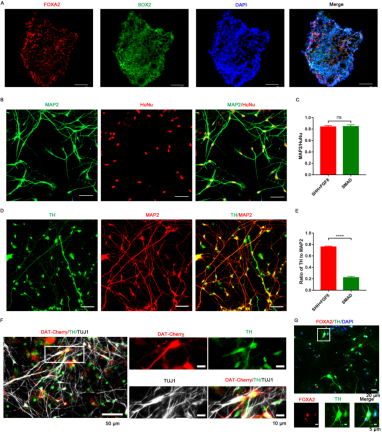
图4 双因子SHH+FGF8诱导方案能够诱导分化出较高比例多巴胺能神经元,但中脑多巴胺能神经元比例较低。
(图源:Yalan Chen et al., Neural Regen Res, 2024)

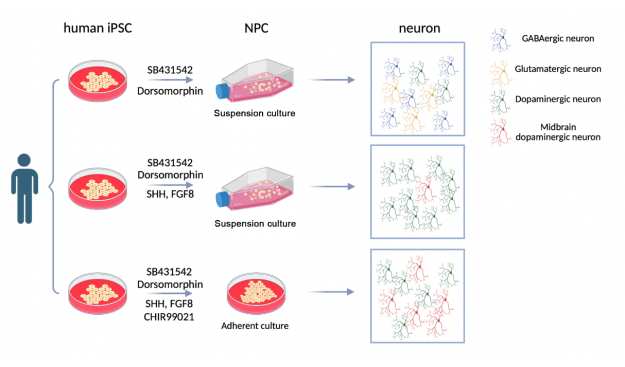
图5 三因子CHIR+SHH+FGF8诱导方案流程图。
(图源:Yalan Chen et al., Neural Regen Res, 2024)
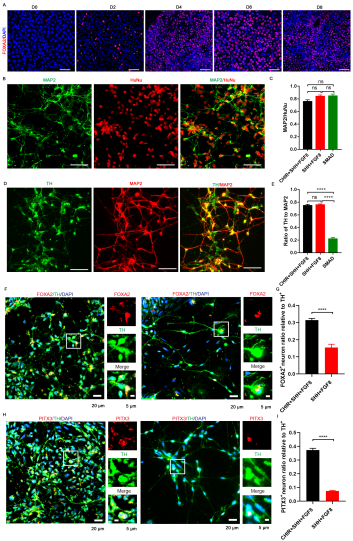
图6 三因子CHIR+SHH+FGF8诱导方案能够诱导分化出较高比例的中脑多巴胺能神经元。
(图源:Yalan Chen et al., Neural Regen Res, 2024)
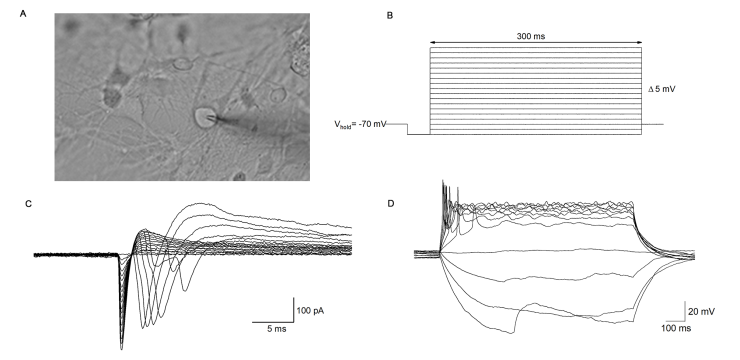
图7 三因子CHIR+SHH+FGF8诱导方案诱导出的多巴胺能神经元具有电生理特性。
(图源:Yalan Chen et al., Neural Regen Res, 2024)
作者的研究旨在开发一个稳定高效的方案,能够将hiPSC分化为中脑多巴胺能神经元,可用于修复老化或受损的神经组织,也可作为研究神经元发育过程或神经系统疾病机制的细胞模型。作者提出的诱导方案是在既往研究方案的基础上进行适当优化的[2-4]。首先作者优化双SMAD信号通路抑制剂方案,将hiPSC高效转化为神经元,但该方案没有提高多巴胺能神经元的分化比例。随后作者优化了诱导方案,在细胞培养的第8天加入SHH和FGF8直至悬浮培养结束。该方案显著提高了多巴胺能神经元的分化比例,但其中中脑多巴胺能神经元比例较低。作者进一步对诱导方案进行优化,调整SHH和FGF8添加时间并加入了Premorphamine和CHIR99021,并且将悬浮培养改为平层培养。该方案在放弃一部分神经元分化效率的前提下,显著提高了中脑多巴胺能神经元的分化比例。#br#
作者提出的三因子CHIR+SHH+FGF8诱导方案能从hiPSC中诱导分化出稳定的高比例中脑多巴胺能神经元,对细胞移植治疗尤其重要。然而仍有许多不足之处。更换为平层培养后使得从hiPSC诱导为中脑多巴胺能神经元的过程时间长、成本高。该方案诱导分化出的中脑多巴胺能神经元还需要移植至动物模型中进一步验证神经元是否能够存活且发挥治疗效果,从而评估该方案诱导出的中脑多巴胺能神经元治疗潜力。
原文链接:https://doi.org/10.4103/1673-5374.378203
参考文献
[1]Tanudjojo B, Shaikh SS, Fenyi A, et al. Phenotypic manifestation of α-synuclein strains derived from Parkinson's disease and multiple system atrophy in human dopaminergic neurons. Nat Commun. 2021;12:3817.
[2]Chambers SM, Fasano CA, Papapetrou EP, et al. Highly efficient neural conversion of human ES and iPS cells by dual inhibition of SMAD signaling. Nat Biotechnol. 2009;27:275-280.
[3]Fasano CA, Chambers SM, Lee G, et al. Efficient derivation of functional floor plate tissue from human embryonic stem cells. Cell Stem Cell. 2010;6:336-347.
[4]Kirkeby A, Grealish S, Wolf DA, et al. Generation of regionally specified neural progenitors and functional neurons from human embryonic stem cells under defined conditions. Cell Rep. 2012;1:703-714.
[5]Kirkeby A, Nolbrant S, Tiklova K, et al. Predictive markers guide differentiation to improve graft outcome in clinical translation of hESC-based therapy for Parkinson's disease. Cell Stem Cell. 2017;20:135-148.
[6]Kouwenhoven WM, von Oerthel L, Smidt MP. Pitx3 and En1 determine the size and molecular programming of the dopaminergic neuronal pool. PLoS One. 2017;12:e0182421.
文章封面图
图片提供自师玲玲团队实验室

师玲玲,医学博士,暨南大学中枢神经再生教育部重点实验室副研究员,博士生导师,美国南加州大学Zilkha神经遗传研究所博士后,中国神经科学学会儿童认知与脑功能障碍分会委员,暨南大学第一临床医学院儿童心理发育行为专科医师。








