NRR:天津大学郑晨光团队综述脊髓损伤与肠道菌群双向调控作用与机制
脊髓损伤(SCI)是一种毁灭性的神经系统疾病,可导致损伤平面以下的运动、感觉和自主神经功能障碍[1]。近几十年来,SCI基础与临床研究不断创新和突破;但由于SCI愈合机制复杂,损伤后再生能力有限,治疗效果仍不理想。因此,开发临床更安全、更有效的治疗技术以实现SCI后的功能重建具有重要意义。微生物群被认为是遗传多样性的来源,宿主免疫的重要组成部分,营养和药物代谢的效应者[2]。越来越多的证据表明,肠道菌群通过脑肠轴影响中枢神经系统疾病的发生和进展,脊髓作为中枢神经系统的重要组成部分,脊髓损伤与肠道相互作用之间的潜在联系尚不清楚。最近的研究表明,SCI患者经常出现肠道功能障碍和肠道生态紊乱[3-5]。脊髓损伤后肠道菌群的改变加重了肠屏障的破坏[6,7],加剧神经炎[8,9]阻碍脊髓损伤神经功能修复及其并发症[10,11]。因此,研究肠道菌群与脊髓损伤的相互调节作用具有重要的临床意义,针对肠道微生物群或其代谢物的治疗方法可能成为促进脊髓功能恢复和改善脊髓损伤并发症的一种有前途的方法。
近期,天津大学郑晨光团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)发表了题为“Dual-directional regulation of spinal cord injury and the gut microbiota”的综述文章,详细论述了脊髓损伤与肠道菌群之间的双向调节作用。作者首先回顾了肠道微生物群在脊髓损伤合并神经源性肠功能障碍患者中的特点,讨论了肠道菌群作为表征脊髓损伤肠道与运动功能生物标记物的观点,并提出脊髓损伤后肠道菌群的失衡可能对脊髓损伤患者多器官多系统产生深远的影响。随后,作者详细分析了脊髓损伤后导致肠道菌群失衡的可能原因,即SCI后自主神经功能障碍导致肠道转运与肠道免疫功能紊乱以及频繁使用抗生素等。通过对现有文献的整理与分类,作者阐述了肠道菌群及其代谢产物影响脊髓损伤后神经重塑的可能机制,具体包括肠道菌群代谢途径(短链脂肪酸,色氨酸);肠道菌群的免疫途径(细胞因子,toll样受体,NLRP3炎症小体等)。作者汇总了现有文献中靶向调节肠道菌群治疗脊髓损伤的临床与基础研究,揭示了粪菌移植、益生菌、饮食干预和康复训练等疗法在SCI中发挥的神经保护作用。最后该文章讨论了目前脊髓损伤与肠道菌群的临床与基础研究存在的问题与不足,提出针对肠道菌群或其代谢产物的治疗可能成为一种有前景的脊髓损伤治疗方法。天津大学研究生崔银洁,天津中医药大学研究生刘婧怡为该综述的共同第一作者,郑晨光教授,李忠正副教授为通讯作者。
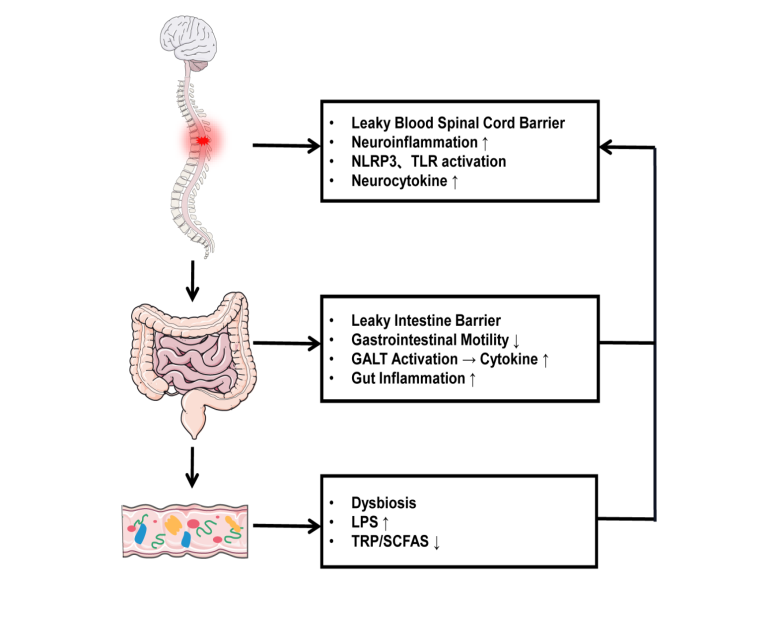
图1脊髓损伤和肠道菌群的双向调控
NLRP3: NOD-like receptor family, pyrin domain containing 3; TLR: Toll-like receptors; GALT: gut-associated lymphoid tissue;
LPS: Lipopolysaccharide; TRP: Tryptophan; SCFAS: short chain fatty acid.
原文链接:https://doi.org/10.4103/1673-5374.380881
参考文献
[1]Tang H, Guo Y, Zhao Y, et al. Effects and mechanisms of acupuncture combined with mesenchymal stem cell
transplantation on neural recovery after spinal cord injury: progress and prospects. Neural Plast. 2020;2020:8890655.
[2]Grice EA, Segre JA. The human microbiome: our second genome. Annu Rev Genomics Hum Genet. 2012;13:151-170.
[3]Gungor B, Adiguzel E, Gursel I, et al. Intestinal microbiota in patients with spinal cord injury. PLoS One. 2016;11:e0145878.
[4]Zhang C, Jing Y, Zhang W, et al. Dysbiosis of gut microbiota is associated with serum lipid profiles in male patients with chronic traumatic cervical spinal cord injury. Am J Transl Res. 2019;11:4817-4834.
[5]Yu B, Qiu H, Cheng S, et al. Profile of gut microbiota in patients with traumatic thoracic spinal cord injury and its clinical implications: a case-control study in a rehabilitation setting. Bioengineered. 2021;12:4489-4499.
[6]Kigerl KA, Hall JC, Wang L, et al. Gut dysbiosis impairs recovery after spinal cord injury. J Exp Med. 2016;213:2603-2620.
[7]Jing Y, Yang D, Bai F, et al. Melatonin Treatment Alleviates Spinal Cord Injury-Induced Gut Dysbiosis in Mice. J Neurotrauma. 2019;36:2646-2664.
[8]Jing Y, Yu Y, Bai F, et al. Effect of fecal microbiota transplantation on neurological restoration in a spinal cord injury mouse model: involvement of brain-gut axis. Microbiome. 2021;9:59.
[9]Rong Z, Huang Y, Cai H, et al. Gut microbiota disorders promote inflammation and aggravate spinal cord injury through the TLR4/MyD88 signaling pathway. Front Nutr. 2021;8:702659.
[10]Groah SL, Nash MS, Ljungberg IH, et al. Nutrient intake and body habitus after spinal cord injury: an analysis by sex and level of injury. J Spinal Cord Med. 2009;32:25-33.
[11]Schmidt E, Torres-Espin A, Raposo P, et al. Fecal transplant prevents gut dysbiosis and anxiety-like behaviour after spinal cord injury in rats. PLoS One. 2020;15:e0226128.

通讯作者:郑晨光,天津大学医学部/精仪学院教授,2013年毕业于南开大学计算神经生理实验室获博士学位,在美国UT Austin学习记忆中心Laura Colgin课题组从事博士后研究。科研工作聚焦于解码大脑神经网络中复杂的放电活动,以揭示多种认知与记忆行为的重要神经机制。主持多项国家级、科技部及天津市级科研项目,在Neuron、Nature Communications等期刊发表论文30篇,参与撰写神经科学类书籍2部。

第一作者:
崔银洁,医学硕士,现就读于天津大学,生物医学工程专业。主要研究方向:肠道菌群与神经免疫。
基金支持:国家自然科学基金(青年基金项目)(82105019);国家自然科学基金(面上基金项目)(82271218);国家自然科学基金委员会(地区科学基金项目)(20JCZDJC00540)


