NRR:浙大医学院附属第一医院胡智勇团队揭示全身麻醉剂通过星形胶质细胞诱发神经毒性的作用
撰文:杨雁嫦,胡智勇
星形胶质细胞起源于外胚层的神经上皮细胞,广泛分布于中枢神经系统。星形胶质细胞拥有多种电压和配体依赖性离子通道,例如半通道(HCs),bestrophin-1通道和体积调节阴离子通道[1]。此外,许多不同类型的神经递质受体和转运蛋白(谷氨酸转运蛋白1,谷氨酸天冬氨酸转运蛋白和GABA转运体)在星形胶质细胞的表面膜上表达[3]。星形胶质细胞能够通过伴随神经冲动活动的细胞外空间中的离子变化以及神经递质、生长因子和其他神经胶质信号分子的释放来传递信息[4,5]。全身麻醉剂(general anesthetic agents, GAAs)可以通过以上多种离子通道和递质受体靶向星形胶质细胞[6],参与镇静、镇痛和遗忘作用,同时可介导全身麻醉诱导的神经毒性和术后认知功能障碍。目前,关注GAAs对星形胶质细胞影响的研究较少,GAA通过星形胶质细胞与神经元相互作用的机制也尚未得到充分解释。探索GAAs对星形胶质细胞作用机制的最新进展,可以帮助我们更好地理解GAAs如何通过星形胶质细胞作用于神经元及其对神经系统的影响,并希望据此作出针对星形胶质细胞的干预措施,以减少麻醉剂诱发的神经毒性。
近期,浙江大学医学院附属第一医院胡智勇团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“General anesthetic agents induce neurotoxicity through astrocytes”的综述文章。星形胶质细胞作为GAAs的重要靶标,不仅参与镇静、镇痛和遗忘作用,而且还介导全身麻醉诱发的神经毒性及术后认知功能障碍。星形胶质细胞在调节神经功能方面及影响神经胶质递质释放方面也有着重要作用。在这篇综述中,作者阐述了GAAs对星形胶质细胞作用机制的最新进展,总结了GAAs如何通过星形胶质细胞作用于神经元,并探讨了神经元与星形胶质细胞之间的相互作用。为干预GAAs的潜在神经毒性提供新的研究方向。杨雁嫦为文章第一作者,胡智勇教授为通讯作者。胡智勇团队长期从事全身麻醉药对脑功能影响的研究,主持国家自然科学基金3项,省部级课题10项。
星形胶质细胞上拥有多种离子通道和受体,使其能够成为GAAs的重要靶标(图1)。然而目前针对这方面的研究很少,这篇综述重点讨论了GAAs如何对星形胶质细胞产生作用及诱发的药物不良反应和神经毒性。在这篇叙述性综述中,作者归纳和总结了多种全身麻醉药物对星形胶质细胞的可能作用机制。
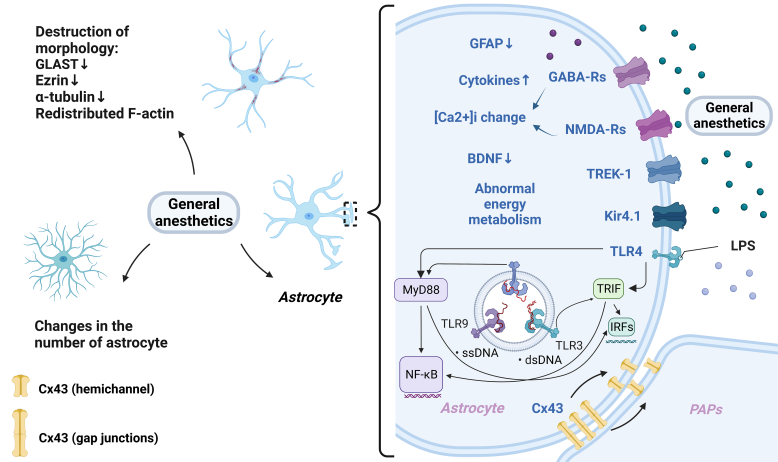
图1 全身麻醉药物(GAAs)暴露后星形胶质细胞功能变化的示意图。(图源:Yang et al., Neural Regen Res, 2024)
吸入麻醉剂
1.1七氟醚
七氟醚对星形胶质细胞的作用一方面反映在其对星形胶质细胞形态和增殖的影响,另一方面反映在对星形胶质细胞功能的调节。七氟醚不仅可以通过干扰星形胶质细胞中Ca2+的稳态来抑制Ezrin的表达,从而影响星形胶质细胞的形态成熟[7],还可以通过干扰JAK/STAT途径来抑制星形胶质细胞的增殖和成熟[10]。星形胶质细胞表达的GABAA受体也是七氟醚的重要靶标[2,12]。有证据表明,七氟醚可以增加海马体中星形胶质细胞GABAA受体的功能[13]。这增加了星形胶质细胞中的GABAA受体与GAA相互作用并成为上游信号以触发可溶性因子释放和离子信号改变的可能性。谷氨酸转运蛋白GLAST在星形胶质细胞中占主导地位,谷氨酸稳态的破坏在许多神经系统疾病发病机制中起重要作用。七氟醚暴露显着降低了星形胶质细胞的数量和GLAST的表达[10]。七氟醚对星形胶质细胞的抑制将导致细胞外谷氨酸浓度增加,诱导兴奋性神经元毒性,增加发育中神经元凋亡。
手术可能是Aβ增加的主要原因,七氟醚通过上调星形胶质细胞中的水通道蛋白-4来增加Aβ的消除[15]。同样,七氟醚通过抑制短暂性脑缺血大鼠的TLR4/NF-κB途径来减少促炎因子的释放[16]。这些证据表明,七氟醚具有一定的神经保护作用,这可能与七氟醚的抗炎作用密切相关。 GAAs可产生神经保护和神经毒性作用,这表明尽管信号通路相同,但在不同浓度的GAAs或不同的生理或病理条件下,对通路的影响可能并不相同。
1.2异氟醚
与七氟醚类似,异氟醚干扰星形胶质细胞和星形胶质细胞网络的形态和发生,主要是通过破坏肌动蛋白细胞骨架,影响未成熟星形胶质细胞α-微管蛋白的发育,并重新分配F-action来实现[17]。然而,有证据表明,在发育过程中反复暴露于异氟醚,将增加视觉识别记忆受损、学习障碍、注意力缺陷/多动、社交行为障碍和焦虑相关行为,这分别与相应大脑区域的星形胶质细胞增殖有关,通过影响大脑关键区域及其连接的发育而损害正常功能[18]。此外,异氟醚通过降低海马缝隙连接表达和增强半通道活性,干扰星形胶质细胞网络通讯,促进神经炎症和认知缺陷[19]。GAAs对星形胶质细胞功能改变产生不同结果,可能与异氟醚的剂量、暴露年龄和动物模型密切相关。
异氟醚在亚麻醉剂量下可以显著抑制星形胶质细胞的钙瞬变,而神经元对异氟醚的敏感性较低[20]。星形胶质细胞对异氟醚的高敏感性决定了Ca2+信号的复杂变化。在异氟醚麻醉下,与清醒小鼠相比,躯体感觉皮层中星形胶质细胞的自发Ca2+活性降低了约85%,在海马和皮质脑切片中降低了55%[21]。星形胶质细胞内Ca2+信号传导以内在振荡波、传播波和微域中Ca2+动态变化的形式存在[22]。因此,GAAs对这种主要通信模式的影响将不可避免地干扰星形胶质细胞与星形胶质细胞以及相应的神经元信号传导和细胞外环境中的其他变化。异氟醚影响星形胶质细胞中膜受体和通道的表达,不仅触发细胞表面α5GABAA受体的表达,而且还抑制Kir4.1/5.1和上调TREK-1通道,这将进一步干扰星形胶质细胞的功能表达[8,23,24]。异氟醚可以通过减少星形胶质细胞中的BDNF表达来抑制轴突生长,从而间接参与认知功能障碍,这一过程可能通过TREK-1通道介导[8]。#br#
对于已确定的神经退行性病变,GAAs可发挥神经保护特性。星形胶质细胞利用多个EGF样结构域途径通过吞噬机制帮助消除突触[14]。最近的研究表明,异氟醚可以减弱体外海马脑片中Aβ1-42诱导的突触消除的增强,这可能是通过下调多个 EGF样结构域 10实现[25]。这些结果为异氟醚不触发或减弱Aβ来源的阿尔茨海默病发病机制提供了证据,为异氟醚的神经保护作用提供了新的研究方向。
2.静脉麻醉剂
2.1丙泊酚
丙泊酚主要通过GABA受体和NMDA受体发挥麻醉作用。在星形胶质细胞中表达的这两种类型的受体可能是丙泊酚作用于星形胶质细胞的重要靶点[26]。此外,丙泊酚在一定程度上可以通过减少星形胶质细胞中BDNF的分泌来促进神经元死亡,星形胶质细胞BDNF介导的细胞保护作用可能在减弱丙泊酚诱导的神经毒性方面具有显著潜力[26]。
丙泊酚通过抑制星形胶质细胞间隙链接、半通道来保护星形胶质细胞免受LPS和相关炎症因子的侵害[27]。关于丙泊酚保护作用的一种假设表明,丙泊酚促进 Cx43的降解,导致细胞间活性氧转运衰减[28]。丙泊酚也被证明可以通过诱导自噬来预防氧化应激诱导的细胞凋亡[29]。因此,丙泊酚是否通过诱导自噬促进受损星形胶质细胞中Cx43的降解值得探讨。另一个假设表明丙泊酚干扰翻译后Cx43修饰。生化和免疫组织化学分析表明,丙泊酚不会改变 Cx43的蛋白质表达水平[30]。但是,它确实改变了Cx43的迁移模式。这证实了翻译后修饰受到了干扰[30]。
丙泊酚具有抗炎作用,通过抑制TLR4/MyD88依赖性NF-κB,ERK1/2和p38丝裂原活化蛋白激酶通路来减弱LPS诱导的星形胶质细胞活化和随后的炎症反应[9]。有趣的是,这种抗炎作用仅在使用临床相关浓度(10μM)的丙泊酚时才显着,相同的结果在另一项研究中得到证实[31]。另一方面,高浓度的丙泊酚(300μM)增加了星形胶质细胞TNF-α的分泌[31]。然而也有报道,丙泊酚(30和300μM)不影响LPS诱导的大鼠神经胶质细胞原代培养物中的亚硝酸盐或TNF-α的产生[32]。造成这些不同结果的原因可能是丙泊酚和LPS的浓度不同,以及使用不同类型的细胞模型。值得注意的是,丙泊酚也可通过干扰micoRNA的表达来诱导星形胶质细胞的凋亡,其机制需要进一步探索[33]。
2.2氯胺酮
氯胺酮是一种NMDA受体拮抗剂,可能通过突触外NMDA受体抑制星形胶质细胞介导的缓慢向内电流(slow inward currents,SICs)同步[34]。低剂量的氯胺酮足以抑制星形胶质细胞中的自发钙瞬变和SICs,而不影响神经元活动,这进一步表明星形胶质细胞似乎对氯胺酮更敏感[34。与丙泊酚对缝隙连接和半通道的显着抑制作用类似,氯胺酮在50μM而不是临床剂量(<50μM)时对半通道具有更强的抑制作用,减少约60%[36]。由于缝隙连接和半通道参与星形胶质细胞之间钙波的传播[37,38],这可能是高剂量麻醉剂影响星形胶质细胞钙信号传导的机制之一。
氯胺酮减少了神经元和星形胶质细胞中BDNF的分泌,并增加了星形胶质细胞中brain-derived neurotrophic factor-antisense(BDNF-AS)和pro-BDNF 的分泌[39]。BDNF-AS与中枢神经系统损伤、帕金森病和其他中枢神经系统病理密切相关[40]。这表明BDNF参与氯胺酮诱导的发育中大脑的神经毒性作用。此外,氯胺酮暴露诱导星形胶质细胞的细胞外囊泡功能发生改变,这在促进神经元死亡中具有重要作用[40]。然而,右美托咪定促进星形胶质细胞中BDNF的释放,并减轻依托咪酯麻醉后的记忆和认知缺陷[11]。这些结果表明GAAs对星形胶质细胞同一途径有着不同的影响结果。
以上分析表明,GAAs不仅会引起星形胶质细胞形态的破坏,而且会影响星形胶质细胞的增殖,抑制星形胶质细胞之间的连接蛋白,从而破坏星形胶质细胞网络的平衡。此外,GAAs还可通过靶向星形胶质细胞上的多种信号通路及递质受体,影响星形胶质细胞与星形胶质细胞之间、星形胶质细胞到邻近神经元,以及其他神经胶质细胞群和血管细胞的信号传导,从而参与镇静、镇痛和遗忘作用,甚至诱导神经毒性作用。
综上所述,GAAs不仅会引起星形胶质细胞形态的破坏,而且会影响星形胶质细胞的增殖,抑制星形胶质细胞之间的连接蛋白,破坏星形胶质细胞网络的平衡。GAAs还可以通过作用于星形胶质细胞中的 GABA、NMDA受体和K+通道来影响胶质递质、细胞因子和神经营养因子的释放。例如,GAA可以通过影响BDNF和乳酸的释放来干扰认知和记忆的形成。此外,GAAs影响星形胶质细胞中的Ca2+信号传导,还可参与介导星形胶质细胞中的抗炎和促炎过程并通过影响microRNA的表达促进星形胶质细胞凋亡,这将不可避免地对星形胶质细胞之间、星形胶质细胞到邻近神经元、及其他神经胶质细胞群和血管细胞的信号传导产生重大影响。大量的体内和体外研究表明,常用的麻醉剂可以通过多种信号通路靶向星形胶质细胞,从而参与麻醉作用或诱导神经毒性。尽管GAA通过星形胶质细胞与神经元相互作用的机制尚未得到充分解释,但不可否认的是,针对星形胶质细胞的干预措施有望为减少麻醉药诱发的神经毒性以及治疗神经、精神疾病具有潜在的应用价值。
原文链接:10.4103/1673-5374.385857
参考文献
[1]Verkhratsky A, Steinhauser C. Ion channels in glial cells. Brain Res Brain Res Rev. 2000;32:380-412.
[2]Verkhratsky A, Nedergaard M. Physiology of astroglia. Physiol Rev. 2018;98:239-389.
[3]Danbolt NC. Glutamate uptake. Prog Neurobiol. 2001;65:1-105.
[4]Kim YS, Choi J, Yoon BE. Neuron-glia interactions in neurodevelopmental disorders. Cells 2020;9:2176.
[5]Brandebura AN, Paumier A, Onur TS, et al. Astrocyte contribution to dysfunction, risk and progression in neurodegenerative disorders. Nat Rev Neurosci. 2023;24:23-39.
[6]Allen NJ, Lyons DA. Glia as architects of central nervous system formation and function. Science. 2018;362:181-185.
[7]Zhou B, Chen L, Liao P, et al. Astroglial dysfunctions drive aberrant synaptogenesis and social behavioral deficits in mice with neonatal exposure to lengthy general anesthesia. PLoS Biol. 2019;17:e3000086.
[8]Zhou CH, Zhang YH, Xue F, et al. Isoflurane exposure regulates the cell viability and BDNF expression of astrocytes via upregulation of TREK‑1. Mol Med Rep. 2017;16:7305-7314.
[9]Zhou CH, Zhu YZ, Zhao PP, et al. Propofol inhibits lipopolysaccharide-induced inflammatory responses in spinal astrocytes via the Toll-like receptor 4/MyD88-dependent nuclear factor-kappaB, extracellular signal-regulated protein kinases 1/2, and p38 mitogen-activated protein kinase pathways. Anesth Analg 2015;120:1361-1368.
[10]Wang W, Lu R, Feng DY, et al. Sevoflurane inhibits glutamate-aspartate transporter and glial fibrillary acidic protein expression in hippocampal astrocytes of neonatal rats through the Janus kinase/signal transducer and activator of transcription (JAK/STAT) pathway. Anesth Analg. 2016;123:93-102.
[11]Wang DS, Kaneshwaran K, Lei G, et al. Dexmedetomidine prevents excessive gamma-aminobutyric acid type A receptor function after anesthesia. Anesthesiology. 2018;129:477-489.
[12]Garcia PS, Kolesky SE, Jenkins A. General anesthetic actions on GABA(A) receptors. Curr Neuropharmacol. 2010;8:2-9.
[13]Chung W, Wang DS, Khodaei S, et al. GABA(A) Receptors in astrocytes are targets for commonly used intravenous and inhalational general anesthetic drugs. Front Aging Neurosci. 2021;13:802582.
[14]Chung WS, Allen NJ, Eroglu C. Astrocytes control synapse formation, function, and elimination. Cold Spring Harb Perspect Biol. 2015;7:a020370.
[15]Gao X, Ming J, Liu S, et al. Sevoflurane enhanced the clearance of Abeta1-40 in hippocampus under surgery via up-regulating AQP-4 expression in astrocyte. Life Sci. 2019;221:143-151.
[16]Hwang JW, Jeon YT, Lim YJ, et al. Sevoflurane postconditioning-induced anti-inflammation via inhibition of the Toll-like receptor-4/nuclear factor kappa B pathway contributes to neuroprotection against transient global cerebral ischemia in rats. Int J Mol Sci. 2017;18:2347.
[17]Lunardi N, Hucklenbruch C, Latham JR, et al. Isoflurane impairs immature astroglia development in vitro: the role of actin cytoskeleton. J Neuropathol Exp Neurol. 2011;70:281-291.
[18]Neudecker V, Perez-Zoghbi JF, Martin LD, et al. Astrogliosis in juvenile non-human primates 2 years after infant anaesthesia exposure. Br J Anaesth. 2021;127:447-457.
[19]Dong R, Han Y, Jiang L, et al. Connexin 43 gap junction-mediated astrocytic network reconstruction attenuates isoflurane-induced cognitive dysfunction in mice. J Neuroinflammation. 2022;19:64.
[20]Schummers J, Yu H, Sur M. Tuned responses of astrocytes and their influence on hemodynamic signals in the visual cortex. Science. 2008;320:1638-1643.
[21]Mulkey DK, Olsen ML, Ou M, et al. Putative Roles of Astrocytes in General Anesthesia. Curr Neuropharmacol. 2022;20:5-15.
[22]Khakh BS, McCarthy KD. Astrocyte calcium signaling: from observations to functions and the challenges therein. Cold Spring Harb Perspect Biol. 2015;7:a020404.
[23]Zurek AA, Yu J, Wang DS, et al. Sustained increase in alpha5GABAA receptor function impairs memory after anesthesia. J Clin Invest. 2014;124:5437-5441.
[24]Ou M, Kuo FS, Chen X, et al. Isoflurane inhibits a Kir4.1/5.1-like conductance in neonatal rat brainstem astrocytes and recombinant Kir4.1/5.1 channels in a heterologous expression system. J Neurophysiol. 2020;124:740-749.
[25]Shi D, Wong JKY, Zhu K, et al. The anaesthetics isoflurane and xenon reverse the synaptotoxic effects of Aβ1-42 on Megf10-dependent astrocytic synapse elimination and spine density in ex vivo hippocampal brain slices. Int J Mol Sci. 2023;24:912.
[26]Liu Y, Yan Y, Inagaki Y, et al. Insufficient astrocyte-derived brain-derived neurotrophic factor contributes to propofol-induced neuron death through Akt/Glycogen synthase kinase 3beta/mitochondrial fission pathway. Anesth Analg. 2017;125:241-254.
[27]Yuan D, Su G, Liu Y, et al. Propofol attenuated liver transplantation-induced acute lung injury via connexin43 gap junction inhibition. J Transl Med. 2016;14:194.
[28]Yuan D, Li X, Luo C, et al. Inhibition of gap junction composed of Cx43 prevents against acute kidney injury following liver transplantation. Cell Death Dis. 2019;10:767.
[29]Yoon JY, Baek CW, Kim EJ, et al. Propofol protects against oxidative-stress-induced COS-7 cell apoptosis by inducing autophagy. J Dent Anesth Pain Med. 2017;17:37-46.
[30]Nuriya M, Yasui D, Yamada T, et al. Direct posttranslational modification of astrocytic connexin 43 proteins by the general anesthetic propofol in the cerebral cortex. Biochem Biophys Res Commun. 2018;497:734-741.
[31]Liu J, Gao XF, Ni W, et al. Effects of propofol on P2X7 receptors and the secretion of tumor necrosis factor-alpha in cultured astrocytes. Clin Exp Med. 2012;12:31-37.
[32]Shibakawa YS, Sasaki Y, Goshima Y, et al. Effects of ketamine and propofol on inflammatory responses of primary glial cell cultures stimulated with lipopolysaccharide. Br J Anaesth. 2005;95:803-810.
[33]Sun WC, Liang ZD, Pei L. Propofol-induced rno-miR-665 targets BCL2L1 and influences apoptosis in rodent developing hippocampal astrocytes. Neurotoxicology. 2015;51:87-95.
[34]Zhang Y, Wu S, Xie L, et al. Ketamine within clinically effective range inhibits glutamate transmission from astrocytes to neurons and disrupts synchronization of astrocytic SICs. Front Cell Neurosci. 2019;13:240.
[35]Thrane AS, Rangroo Thrane V, Zeppenfeld D, et al. General anesthesia selectively disrupts astrocyte calcium signaling in the awake mouse cortex. Proc Natl Acad Sci U S A. 2012;109:18974-18979.
[36]Liu X, Gangoso E, Yi C, et al. General anesthetics have differential inhibitory effects on gap junction channels and hemichannels in astrocytes and neurons. Glia. 2016;64:524-536.
[37]Scemes E, Giaume C. Astrocyte calcium waves: what they are and what they do. Glia. 2006;54:716-725.
[38]Leybaert L, Sanderson MJ. Intercellular Ca(2+) waves: mechanisms and function. Physiol Rev. 2012;92:1359-1392.
[39]Penning DH, Cazacu S, Brodie A, et al. Neuron-glia crosstalk plays a major role in the neurotoxic effects of ketamine via extracellular vesicles. Front Cell Dev Biol. 2021;9:691648.
[40]Ghafouri-Fard S, Khoshbakht T, Taheri M, et al. A concise review on the role of BDNF-AS in human disorders. Biomed Pharmacother. 2021;142:112051.
基金支持:该研究得到国家自然科学基金[82171260; 81641042; 81471240]和浙江省自然科学基金[LZ22H090002; 2014C33170]的资助。
团队介绍
第一作者:杨雁嫦,浙江大学附属第一医院麻醉科,从事手术期重要器官保护及全身麻醉药对发育中大脑神经毒性的研究工作。参与发表SCI论文1篇。

通讯作者:胡智勇,浙江大学医学院附属第一医院麻醉科副主任。多年从事围手术期重要器官保护及全身麻醉药对发育中大脑神经毒性的研究工作。主持各类课题10余项,其中国家自然科学基金项目2项。先后发表学术论文60余篇,其中SCI收录25篇。作为执笔者制定“小儿日间手术麻醉指南”,参编专著9部,其中主编1部、副主编3部。

