NRR:湖北医药学院王云甫团队揭示雷帕霉素对帕金森病的新作用机制
撰文:朱敬,刘彤宇
帕金森病(Parkinson’s disease,PD)是一种以运动系统功能障碍为特征的神经退行性疾病[1],其最主要的病理改变是中脑黑质多巴胺(dopamine, DA)能神经元的变性死亡,由此而引起纹状体DA含量显著性减少而致病[2]。研究表明1-甲基-4-苯基四氢吡啶(MPTP)可导致黑质纹状体细胞死亡,引起一种非典型帕金森病[3-4]。哺乳动物雷帕霉素靶蛋白(mTOR)信号通路是调控细胞生长增殖和蛋白质合成的重要信号通路,介导多种神经系统疾病的发生和发展[5]。雷帕霉素(Rapamycin, Rapa)作为mTOR信号通路的特异性抑制剂,也是经典的自噬诱导剂,可以抑制由多种因素诱导的细胞凋亡,且已有研究表明其可对帕金森病起保护作用[6],但作用机制尚不明确。铁死亡是一种非典型的细胞死亡方式,与自噬、凋亡、坏死等在细胞死亡形态,以及诱发和抑制的生物学背景上都有着千丝万缕的联系[7],这种新的细胞死亡方式在PD的相关研究中也有报道[8]。在帕金森病重Rapa与铁死亡之间的联系却并不完全清楚。因此,通过探索铁死亡在Rapa对帕金森病神经保护中的作用,及其发挥作用的机制,以期为进一步探究PD的潜在治疗靶点提供新思路。
近期,湖北医药学院王云甫团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“Rapamycin reverses ferroptosis by increasing autophagy in MPTP/MPP+-induced models of Parkinson’s disease”的研究论文。通过研究,作者发现,Rapa可通过激活自噬通路逆转PD中发生的铁死亡,在一定程度上对PD产生保护作用。该文带来的启示:铁死亡、自噬可作为PD的潜在治疗靶点;Rapa作为免疫抑制剂,其可能在未来PD的治疗中起到关键作用。刘彤宇和汪佩涵为论文共同第一作者,王云甫教授和朱敬副教授为论文共同通讯作者。
PD是多因素介导的中老年退行性疾病,其分子发病机制包括多种因素,如蛋白质稳态受损、氧化应激、线粒体功能障碍、突触传递障碍、钙稳态失衡、朊病毒样α-突触核蛋白传递与神经元炎症等[9-11]。此外,脑部铁离子代谢相关的基因损伤也是PD的常见病因。PD 患者的神经影像学检查以及尸检病理报告均显示在PD的发病早期铁选择性沉积在黑质[12]。Rapa对PD的改善作用也已有报道[13],多认为与抑制老化过程中的自噬有关,但其作用机制尚不明确。基于此,本研究作者推测铁死亡也与PD的发生有着密切地联系,Rapa是否通过抑制铁死亡的发生对PD产生神经保护作用。
该研究从PD小鼠和细胞模型两方面着手,以自噬和铁死亡为主线,用Rapa预处理PD小鼠和细胞模型,检测自噬和铁死亡等相关指标,揭示Rapa在PD中的神经保护作用及其机制。体内研究实验结果显示,经Rapa治疗的PD模型小鼠行为学明显改善(图1)、黑质中酪氨酸羟化酶的表达较模型组增加。这些结果说明Rapa对PD小鼠具有神经保护作用。同时,在Rapa的作用下,PD小鼠的黑质组织中自噬被激活、铁死亡被抑制,经铁死亡诱导剂诱导后可逆转其保护作用,这说明Rapa对PD的保护作用与自噬及铁死亡具有一定的相关。在体外研究中, Rapa预作用于MPP+诱导后的PC12细胞模型,同时检测自噬相关蛋白LC3及P62、铁死亡相关蛋白GPX4及SLC7A11,发现经Rapa预作用后,PD细胞模型中自噬同样被激活、铁死亡被抑制(图2),均与小鼠组织中的发现一致。而使用铁死亡诱导剂组可逆转Rapa的铁死亡抑制作用及对PD的保护作用。使用自噬抑制剂可逆转自噬激活的同时,还可同样逆转Rapa的铁死亡抑制作用及对PD的保护作用。这些结果说明Rapa可通过诱导自噬而逆转PD中的铁死亡机制,从而对PD产生神经保护作用。
目前,对于PD患者的临床治疗方案仍以药物治疗为主,手术治疗是药物治疗的一种有效补充[14],康复治疗、心理治疗及良好的护理也能在一定程度上改善症状[15]。目前临床上用于治疗PD的药物主要分为多巴制剂、抗胆碱能制剂、金刚烷胺、多巴胺受体激动剂、单胺氧化酶B型抑制剂、儿茶酚-氧位-甲基转移酶抑制剂等六大类。其中,这些药物治疗及手术治疗均以缓解PD患者临床症状、提高PD患者生活质量为主,并不针对PD的病理机制,无法阻止黑质纹状体多巴胺能神经元的变性,也存在一定程度的副作用。目前尚无彻底治愈PD的好办法。因此,有关PD的病理机制的探究是非常必要的,该研究为探寻一种新的、安全有效的神经元保护性药物提供了一个新的方向。
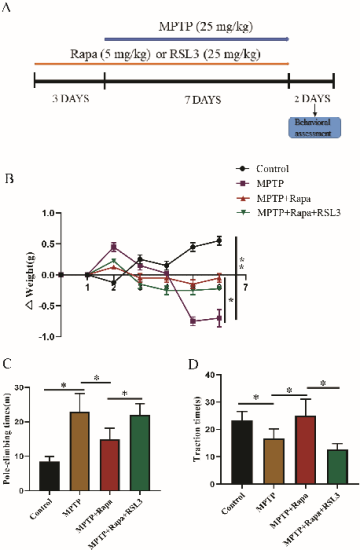
图1 Rapa逆转了PD小鼠模型中由MPTP导致的体重减轻和行为障碍(图源:Liu et al., Neural Regen Res, 2023)
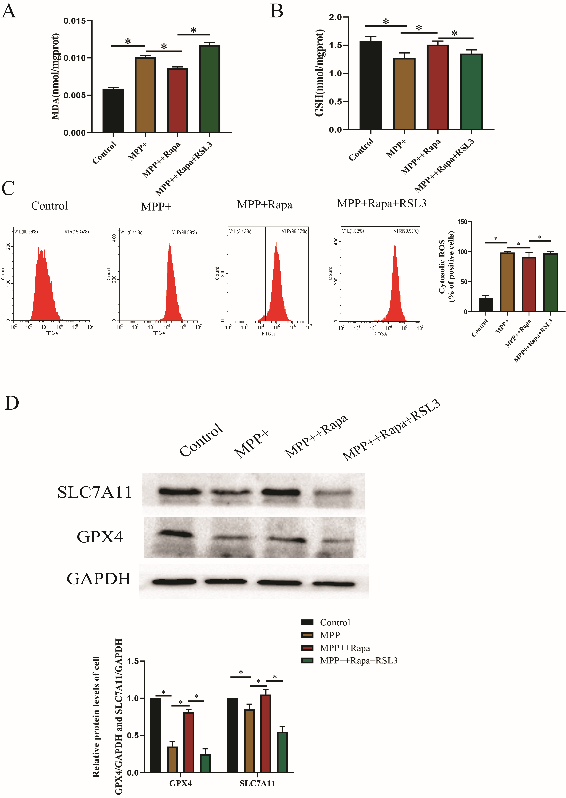
图2 Rapa逆转了PD细胞模型中由MPP+ 引起的铁死亡(图源:Liu et al., Neural Regen Res, 2023)
综上所述,Rapa可对PD起到一定程度的神经保护作用,这种保护作用是通过激活自噬、逆转铁死亡而实现的。主要表现在经Rapa处理的PD小鼠症状有所改善、多巴胺能神经元丢失减少、自噬激活、铁死亡出现逆转。同时,Rapa可减轻经MPP+干预后的PCI2细胞的死亡,而自噬抑制剂又可促进铁死亡发生。该研究结果将为PD的临床特异性治疗提供实验和理论依据。
当然,该研究也存在一定性局限性。首先,该研究只关注雄性小鼠。为了有更多的临床意义,未来的研究应该考虑使用雌性小鼠。此外,不同的Rapa预作用时间、给药方式、浓度可能会有不同的作用效果,考虑这可能与药物毒性、Rapa参与的其他重要信号通路、自噬的双重作用等相关,其调控的机制也十分复杂。因此,有关其中的平衡作用还需进一步深入研究探寻。
原文链接:https://doi.org/10.4103/1673-5374.371381
参考文献
[1]. Khan AU, Akram M, Daniyal M, et al. Awareness and current knowledge of Parkinson's disease: a neurodegenerative disorder. Int J Neurosci. 2019;129(1):55-93.
[2]. Jankovic J, Tan EK. Parkinson's disease: etiopathogenesis and treatment. J Neurol Neurosurg Psychiatry. 2020;91(8):795-808.
[3]. Bazzu G, Calia G, Puggioni G, et al. alpha-Synuclein- and MPTP-generated rodent models of Parkinson's disease and the study of extracellular striatal dopamine dynamics: a microdialysis approach. CNS Neurol Disord Drug Targets. 2010;9(4):482-490.
[4]. Blandini F, Armentero MT. Animal models of Parkinson's disease. FEBS J. 2012;279(7): 1156-1166.
[5]. Polchi A, Magini A, Meo DD, et al. mTOR Signaling and Neural Stem Cells: The Tuberous Sclerosis Complex Model. Int J Mol Sci. 2018;19(5):1474.
[6]. Zhang K, Zhu S, Li J, et al. Targeting autophagy using small-molecule compounds to improve potential therapy of Parkinson's disease. Acta Pharm Sin B. 2021;11(10):3015-3034.
[7]. Su LJ, Zhang JH, Gomez H, et al. Reactive oxygen species-induced lipid peroxidation in apoptosis, autophagy, and ferroptosis. Oxid Med Cell Longev. 2019;2019:5080843.
[8]. Ke Y, Ming Qian Z. Iron misregulation in the brain: a primary cause of neurodegenerative disorders. Lancet Neurol. 2003;2(4):246-253.
[9]. Lu J, Wu M, Yue Z. Autophagy and Parkinson's Disease. Adv Exp Med Biol, 2020;1207:21-51.
[10]. Jagadeesan AJ, Murugesan R, Vimala Devi S, et al. Current trends in etiology, prognosis and therapeutic aspects of Parkinson's disease: a review. Acta Biomed. 2017;88(3):249-262.
[11]. Redenšek S, Trošt M, Dolžan V. Genetic determinants of parkinson's disease: can they help to stratify the patients based on the underlying molecular defect? Front Aging Neurosci. 2017;9:20.
[12]. Schapira A, Chaudhuri KR, Jenner P. Non-motor features of Parkinson disease. Nat Rev Neurosci, 2017; 18(7): 435-450.
[13]. Sasazawa Y, Sato N, Umezawa K, et al. Conophylline protects cells in cellular models of neurodegenerative diseases by inducing mammalian target of rapamycin (mTOR)-independent autophagy. J Biol Chem. 2015;290(10):6168-6178.
[14]. Singer C, Reich SG. Parkinson disease. Clin Geriatr Med, 2020;36(1): xiii-xiv.
[16]. Armstrong MJ, Okun MS. Choosing a Parkinson disease treatment. JAMA. 2020;323(14): 1420.


第一作者:刘彤宇、汪佩涵,湖北医药学院在读硕士研究生。
通讯作者:王云甫、朱敬,湖北医药学院院长、教授;湖北医药学院副教授。



