NRR:中国天津医科大学冯世庆团队揭示TGF-β1-SMAD2信号通路在脊髓损伤后神经元衰老中的关键作用
脊髓损伤是一种严重的中枢神经系统损伤,发病率持续上升,对患者和社会造成巨大负担[1]。脊髓损伤后,氧化应激诱导的细胞状态改变破坏微环境,是阻碍恢复的重要病理机制之一 [2]。细胞衰老是脊髓损伤后常见现象,其特征包括细胞周期停滞和P16INK4α上调。衰老细胞的积累会损害脊髓功能并增加相关病理风险。在灵长类动物和小鼠脊髓中可见衰老神经元的积累,这与SMAD2磷酸化相关。清除衰老神经元已被证明具有神经保护作用 [3]。
转化生长因子β1(TGF-β1)在脊髓损伤后发挥重要作用,尤其在慢性阶段由M2型巨噬细胞大量分泌。TGF-β1通过激活SMAD信号通路诱导细胞周期抑制基因(如p15,p21)的表达,从而导致神经元进入衰老状态。这一机制在肝损伤等模型中已得到验证 [4],但在脊髓损伤中的具体作用尚不清楚。
中国天津医科大学冯世庆团队在《中国神经再生研究(英文)》(Neural Regeneration Research)发表的研究发现,巨噬细胞分泌的TGF-β1可通过激活SMAD2信号通路加重脊髓损伤(脊髓损伤)后神经元衰老,并与衰老标志物P16INK4α和β-半乳糖苷酶活性增加密切相关。向脊髓损伤模型小鼠施用LY-364947(SMAD2抑制剂)或氯膦酸盐脂质体可减少衰老神经元数量,改善组织修复和运动功能恢复。该研究表明,靶向TGF-β1-SMAD2通路或可作为缓解脊髓损伤后神经元老化的潜在治疗策略。冯海文为第一作者,冯世庆、宁广智和宋晓萌为通讯作者。
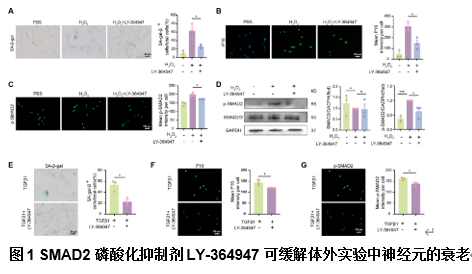
冯世庆等在体外实验中,研究使用低浓度的过氧化氢和外源性TGF-β1处理HT22细胞以诱导神经元衰老。结果显示,SA-β-gal阳性细胞比例显著增加,表明细胞衰老被成功诱导。然而,加入LY-364947后,SA-β-gal阳性细胞比例显著降低。免疫荧光染色进一步显示,过氧化氢可显著上调P16蛋白表达,而LY-364947则能抑制这一变化。这表明低浓度过氧化氢可诱导神经元衰老,而SMAD2磷酸化抑制剂可缓解该效应(图1)。
#br#
为研究脊髓损伤4周后衰老细胞的分布,冯世庆等利用苏木精-伊红染色和β-半乳糖苷酶染色进行了分析。在脊髓矢状面中,衰老细胞主要分布于腹侧灰质,集中在损伤中心两侧,而损伤核心区缺乏衰老细胞。脊髓冠状面中,衰老细胞主要分布于脊髓前角,并具有较大的细胞体特征。进一步通过β-半乳糖苷酶染色联合神经元标记物NeuN的免疫荧光染色发现,大多数衰老细胞共表达SA-β-gal和NeuN,确认神经元,尤其是运动神经元,是主要的衰老细胞群体(图2)。
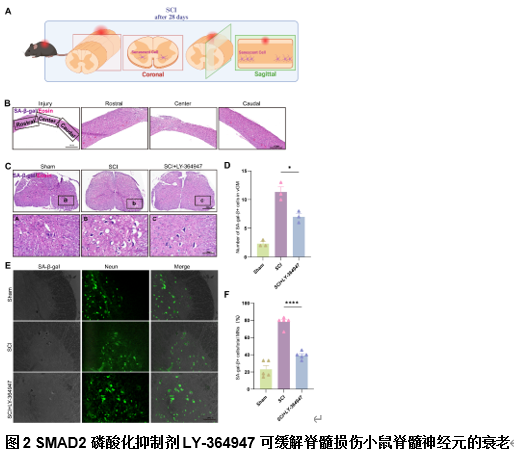
脊髓损伤后可见神经元衰老的增加。为探讨体内衰老神经元的蛋白表达是否与体外一致,冯世庆等通过免疫荧光染色和Western blot检测P16和p-SMAD2的表达。结果显示,脊髓损伤后4周时,损伤中心周围P16和p-SMAD2的表达显著增加。SMAD2/3磷酸化抑制剂的使用显著降低了p-SMAD2和P16的表达水平,表明SMAD2磷酸化是诱导脊髓损伤后神经元衰老的关键因素,阻断该通路可延缓衰老进程。
对脊髓损伤后4周的组织恢复进行了免疫荧光染色分析。结果显示,抑制TGF-β1-SMAD2/3通路显著增加了损伤边缘神经元的存活,减少了由星形胶质细胞形成的瘢痕,改善了髓鞘保存并保护了神经轴突。另外分析了小鼠的膀胱功能和后肢运动功能,发现抑制TGF-β1-SMAD2/3通路的小鼠可见膀胱功能改善、肌肉萎缩减轻及运动和神经功能增强。
这些结果表明,脊髓损伤后大量衰老细胞的存在阻碍了组织修复,不仅减少了神经元存活和轴突再生,还对星形胶质细胞和少突胶质细胞产生不利影响,可能与衰老神经元释放炎性因子有关。综上,抑制SMAD2磷酸化通路以靶向神经元衰老,有望促进脊髓损伤后的组织修复和功能恢复。
为探讨小鼠巨噬细胞在脊髓损伤后是否通过分泌TGF-β1促进运动神经元衰老,进行了体外和体内实验。体外实验中,通过IL-4诱导巨噬细胞极化,并使用流式细胞术评估极化状态。结果显示,与PBS组相比IL-4组极化巨噬细胞比例增加45%,ELISA显示IL-4组TGF-β1分泌水平为PBS组的2倍。体内实验中,利用氯膦酸盐脂质体耗竭巨噬细胞。28d后流式细胞术分析显示,巨噬细胞数量减少75%,Western blot显示TGF-β1表达减少80%。苏木精-伊红和β-半乳糖苷酶染色结果表明,巨噬细胞耗竭显著减少了脊髓组织中的衰老细胞数量(图3)。
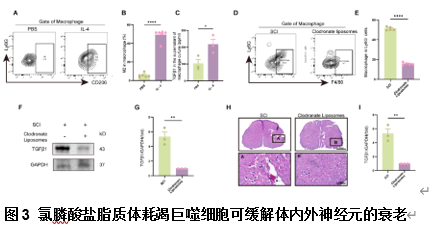
总之,脊髓损伤后衰老神经元主要积累在损伤前后角的运动神经元中。体外实验中,低浓度过氧化氢可诱导神经元衰老,与TGF-β1诱导的SMAD2磷酸化密切相关。体内实验则显示,抑制SMAD2磷酸化显著减少了衰老神经元数量,并改善了组织修复,包括神经元保存增加、瘢痕减少以及轴突和髓鞘保留。此外,耗竭巨噬细胞降低了TGF-β1水平并减少衰老神经元。这表明巨噬细胞极化和TGF-β1分泌在脊髓损伤后运动神经元衰老中起关键作用。
尽管研究证实衰老细胞积累对脊髓损伤恢复不利,但其作用复杂。衰老相关分泌表型(SASP)可通过炎症因子影响周围细胞,导致瘢痕增生和髓鞘丢失。然而,在某些模型中,如斑马鱼和蝾螈的再生研究中,衰老细胞在早期清除会阻碍修复,而短暂存在可促进组织再生。因此,未来治疗应着眼于选择性清除衰老细胞或利用其有益作用。
研究还揭示,TGF-β1在脊髓损伤早期具有抗炎和减少凋亡的作用,但后期持续分泌可能诱导衰老,表现出时间依赖性。衰老细胞通过分泌SASP显著影响损伤后的微环境,深入研究其分泌特征或将成为改善脊髓损伤治疗的新方向。研究进一步指出,运动神经元在脊髓损伤后衰老中占主导,探索特定细胞抗衰老机制可能有助于改善运动功能恢复。
原文链接:https://doi.org/10.4103/NRR.NRR-D-24-01376
参考文献#br#
[1]
Furlan JC, Noonan V, Singh A, et al. Assessment of impairment in patients with acute traumatic spinal cord injury: a systematic review of the literature. J Neurotrauma. 2011;28(8):1445-1477.#br#
[2]
Fan B, Wei Z, Yao X, et al. Microenvironment imbalance of spinal cord injury. Cell Transplant. 2018;27(6):853-866.#br#
[3]
Sun S, Li J, Wang S, et al. CHIT1-positive microglia drive motor neuron ageing in the primate spinal cord. Nature. 2023;624(7992):611-620.#br#
[4]
Bird TG, Müller M, Boulter L, et al. TGFβ inhibition restores a regenerative response in acute liver injury by suppressing paracrine senescence. Sci Transl Med. 2018;10(454):eaan1230.#br#
#br#


