中国神经再生研究(英文版) ›› 2021, Vol. 21 ›› Issue (5): 2031-2039.doi: 10.4103/NRR.NRR-D-24-00431
磁共振成像示踪超顺磁性纳米铁剂标记间充质基质细胞修复脊髓损伤的能力
Magnetic resonance imaging tracing of superparamagnetic iron oxide nanoparticle–labeled mesenchymal stromal cells for repairing spinal cord injury
Xiaoli Mai1, #, Yuanyuan Xie2, #, Zhichong Wu3, #, Junting Zou1 , Jiacheng Du4 , Yunpeng Shen5 , Hao Liu6 , Bo Chen7 , Mengxia Zhu1 , Jiong Shi8 , Yang Chen5 , Bing Zhang1, *, Zezhang Zhu3, *, Bin Wang2, *, Ning Gu9
- 1 Department of Radiology, Nanjing Drum Tower Hospital, Affiliated Hospital of Medical School, Nanjing University, Nanjing, Jiangsu Province, China; 2 Clinical Stem Cell Center, Nanjing Drum Tower Hospital, Affiliated Hospital of Medical School, Nanjing University, Nanjing, Jiangsu Province, China; 3 Department of Spinal Surgery, Nanjing Drum Tower Hospital, Affiliated Hospital of Medical School, Nanjing University, Nanjing, Jiangsu Province, China; 4 State Key Laboratory of Bioelectronics and Jiangsu Key Laboratory of Biomaterials and Devices, School of Biological Sciences and Medical Engineering, Southeast University, Nanjing, Jiangsu Province, China; 5 Laboratory of Image Science and Technology, Southeast University, Nanjing, Jiangsu Province, China; 6 Department of Neurosurgery, Nanjing Drum Tower Hospital, Affiliated Hospital of Medical School, Nanjing University, Nanjing, Jiangsu Province, China; 7 Institute of Materials Science and Devices, School of Materials Science and Engineering, Suzhou University of Science and Technology, Suzhou, Jiangsu Province, China; 8 Department of Pathology, Nanjing Drum Tower Hospital, Affiliated Hospital of Medical School, Nanjing University, Nanjing, Jiangsu Province, China; 9 Nanjing Key Laboratory for Cardiovascular Information and Health Engineering Medicine, Institute of Clinical Medicine, Nanjing Drum Tower Hospital, Affiliated Hospital of Medical School, Nanjing University, Nanjing, Jiangsu Province, China
摘要:
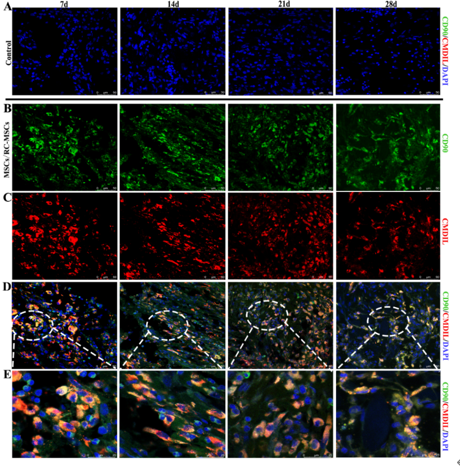
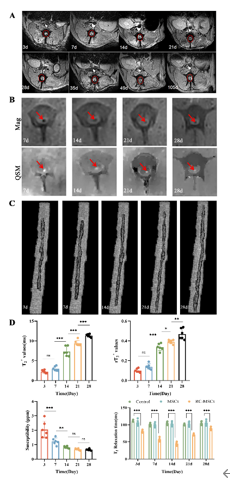
间充质基质细胞移植是治疗多种全身性和弥漫性疾病的一种有效而有前景的方法。但是目前尚不明确移植间充质基质细胞在体内的生物学特性,包括细胞活性、分布、迁移和在人体内的转归。传统的细胞示踪方法无法用于临床。使用超顺磁性氧化铁纳米粒子作为造影剂可在磁共振成像下对移植细胞进行观察。2016年国家医药产品监督管理局已批准一种新型超顺磁性氧化铁纳米粒子瑞存可用于临床试验的造影剂。此次实验使用比格犬制作半横断急性脊髓损伤模型,而后移植瑞存标记间充质基质细胞进行治疗。结果显示,瑞存标记的间充质基质细胞也能有效修复受损脊髓纤维,并部分恢复急性脊髓损伤动物的神经功能。且T2*WI上可见损伤脊髓两侧存在低信号区域。UTE-QSM量化结果显示,瑞存标记的间充质基质细胞可在损伤脊髓中稳定存在超过4周。提示磁共振成像在有效追踪瑞存标记的间充质基质细胞迁移变化及评估脊髓损伤修复能力方面有潜力。
https://orcid.org/0000-0003-3981-8849 (Bin Wang)