NRR: 中国华中科技大学附属同济医院王伟团队揭示霍乱毒素B亚基可通过坐骨神经注射示踪恒河猴脊髓环路
撰写:何紫郁
脊髓损伤(Spinal Cord Injury, SCI)是引起严重运动、感觉及自主神经功能障碍的主要原因[1]。随着再生医学和细胞治疗技术的飞速发展,研究者开始探索通过细胞移植等手段促进脊髓的修复与再生[2]。鉴于非人灵长类动物(Nonhuman Primates, NHPs)在神经解剖学和神经生理学上与人类的高度相似性,研究者普遍认为应在NHPs模型中首先验证细胞移植的安全性和有效性,再推进至临床试验[3]。为了更深入地理解脊髓损伤后移植神经元的连接和功能重建,追踪特定神经元及其突触连接的技术变得尤为重要。然而,目前缺乏有效的方法来示踪猴脊髓中的运动神经元和初级感觉传入神经。霍乱毒素B亚单位Cholera Toxin Subunit B, CTB)作为一种有效的神经示踪剂,在小鼠和大鼠模型中已得到广泛应用[4-6],但在NHPs中的应用尚未得到充分验证。
中国华中科技大学附属同济医院的王伟团队在《中国神经再生研究(英文)》(Neural Regeneration Research)发表的研究结果表明,霍乱毒素B亚单位能够有效标记恒河猴脊髓中的运动神经元和感觉传入神经,为神经示踪技术提供了一种稳定有效的方法。这一发现为进一步探索NHPs中神经元连接和功能重建提供了重要工具,促进了脊髓损伤研究的进展,并为未来的细胞移植和再生医学治疗的环路研究奠定了基础。何紫郁和刘智贤为论文共同第一作者,王伟教授和郑小龙博士为论文共同通讯作者。
在该研究中,恒河猴在T10脊髓损伤后接受了人胚胎干细胞来源的脊髓V3神经前体细胞的移植。约6个月后,进行了霍乱毒素B亚单位示踪实验。手术在严格遵循无菌和微创的原则下进行,过程持续不到2小时,所有生命体征均在正常范围内。通过对坐骨神经进行暴露、钳夹并注射霍乱毒素B亚单位,6天后对恒河猴实施安乐死,取T12-S2节段制成冠状切片进行霍乱毒素B亚单位免疫荧光染色。实验结果显示,霍乱毒素B亚单位注射后,在L4-S1脊髓节段的灰质中出现明显的霍乱毒素B亚单位阳性信号,集中分布于前角和后角,而白质中未见霍乱毒素B亚单位信号(图1)。在脊髓 L6-S1前角,霍乱毒素B亚单位阳性信号类似于细胞胞体,主要分布于 L6 和 L7 节段,对其计数证实 L6 和 L7 节段具有最多的 霍乱毒素B亚单位阳性细胞;在后角,霍乱毒素B亚单位阳性信号密集,主要分布于 L5-L7 节段,而在 L4 和 S1节段分布较少,对其面积分析证实 L5-L7 节段具有最多的霍乱毒素B亚单位标记结构(图1)。这些结果表明坐骨神经霍乱毒素B亚单位注射能够有效标记恒河猴腰骶脊髓的细胞和结构。
对L6-S1前角所标记的细胞进行免疫染色鉴定显示,霍乱毒素B亚单位标记的细胞表达神经元标记物NeuN共标,证实其为神经元。此外,霍乱毒素B亚单位标记的神经元还与胆碱能标记物ChAT和VAChT共标,表明这些细胞为胆碱能神经元(图2)。结合阳性胞体位于第IX板层并表达运动神经元特异性转录因子ISLET1,可以判断其为运动神经元。进一步定量分析发现,尽管霍乱毒素B亚单位标记的细胞未完全覆盖所有运动神经元,但在霍乱毒素B亚单位标记的细胞中,均为运动神经元(图2)。同时,根据猴脊髓的图谱[7],发现在L6-S1段的霍乱毒素B亚单位标记运动神经元主要支配臀肌、下肢伸肌和屈肌、腘绳肌、缝匠肌、股薄肌和半腱肌,而不支配躯干肌肉。研究者认为,霍乱毒素B亚单位标记的运动神经元为α运动神经元,因为它们具有较大的细胞体并且均表达NeuN,而γ运动神经元则具有较小的细胞体,并显著不表达NeuN[8]。因此,坐骨神经内注射霍乱毒素B亚单位能够标记猴子L6-S1脊髓中的许多α运动神经元,并结合猴脊髓的图谱及其他解剖和功能结果,可以定位支配特定目标肌肉的运动神经元群体。而在背角,霍乱毒素B亚单位标记的结构呈纤维末梢和点状,为初级感觉传入纤维,大量分布于脊髓灰质I和II板层,III-IV板层较之减少(图3)。同时放大视野发现阳性纤维信号在各个板层均有分布,包括VII-IX板层脊髓运动环路所在的区域;并且,在更头侧的T12-L3脊髓节段中,还可以观察到脊髓灰质中间板层靠内侧的少许阳性信号(图3),推测为向头侧延伸的本体感觉纤维,这与在啮齿动物上观察到的霍乱毒素B亚单位示踪结果高度一致。这些纤维末梢信号能与不同突触末梢标志物,如VGLUT1以及VGLUT3,共标,但不与VGLUT2共标(图3),证实霍乱毒素B亚单位所标记的结构包括Aβ类感觉纤维、C类低阈值机械感受器(C-Low Threshold Mechanoreceptors)以及本体感觉纤维。
在啮齿动物中,初级感觉传入纤维与多种脊髓感觉和运动相关中间神经元建立突触连接[9],因此为了探究恒河猴脊髓中的环路连接,研究人员分别观察了霍乱毒素B亚单位阳性纤维末梢与背腹侧不同脊髓神经元的连接情况。实验结果显示,霍乱毒素B亚单位阳性纤维末梢表达突触前标志物Synaptophysin并与突触后标志物Homer1在空间上紧邻(图4),证实其能形成突触连接。同时,也能观察到其与后角感觉中间神经元(兴奋性:LMX1B+;抑制性:LHX1+;钙结合蛋白:Calretinin+, Calbindin+),前角运动相关中间神经元(FOXP2+, SATB1+)和同样被霍乱毒素B亚单位标记的运动神经元建立兴奋性突触连接(图4)。这些结果说明,通过霍乱毒素B亚单位坐骨神经注射,证实恒河猴脊髓中存在与啮齿类动物相似的感觉运动环路连接。
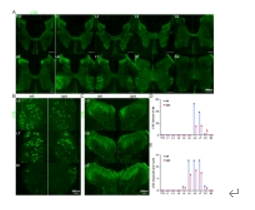
图1 通过坐骨神经注射霍乱毒素B亚单位成功标记猴腰骶脊髓灰质内的胞体和纤维结构
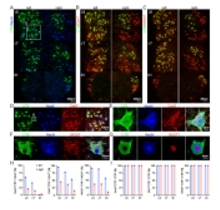
图2 霍乱毒素B亚单位标记猴腰骶脊髓前角的运动神经元
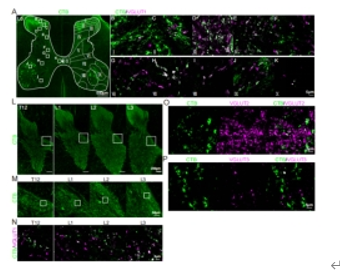
图3 霍乱毒素B亚单位标记猴腰骶脊髓后角的初级传入感觉纤维
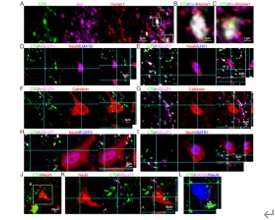
图4 TB标记的初级传入感觉纤维与多种猴脊髓神经元形成突触连接
综上所述,该研究首次系统地展示了霍乱毒素B亚单位在恒河猴腰骶脊髓中标记运动神经元和初级感觉传入神经纤维的有效性,并详细描述了其阳性信号在头尾节段、背腹板层的分布和性质鉴定,同时观察了霍乱毒素B亚单位阳性纤维末梢与猴脊髓神经元建立的突触连接。这些发现不仅为理解恒河猴脊髓的神经网络提供了重要的实验依据,也为未来在神经损伤和再生研究中应用霍乱毒素B亚单位示踪技术探索神经环路机制奠定了基础。该示踪技术可以广泛应用于包括脊髓损伤、肌萎缩性侧索硬化和神经病理性疼痛在内的恒河猴研究,来揭示神经投射以及环路连接的病理改变。
同时,研究也存在不足之处,因为考虑到动物伦理和整个课题的实验设计,该部分探索仅在一只恒河猴上完成。在未来,作者团队会致力于神经干细胞移植修复脊髓环路的研究中,并且会在后续的NHPs模型中应用霍乱毒素B亚单位示踪技术,届时,通过多样本的重复和比较,也会进一步完善和补充该示踪技术的结果。
参考文献
[1] GBD 2016 Neurology Collaborators. Global, regional, and national burden of neurological disorders, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol. 2019;18(5):459-480.
[2] Fischer I, Dulin JN, Lane MA. Transplanting neural progenitor cells to restore connectivity after spinal cord injury. Nat Rev Neurosci. 2020;21:366-383
[3] Olaya AMS, Almeida FM, Martinez AMB, et al. Treatment of spinal cord injury with biomaterials and stem cell therapy in non-human primates and humans. Neural Regen Res. 2025;20:343-353.
[4] Shehab SAS, Hughes DI. Simultaneous identification of unmyelinated and myelinated primary somatic afferents by co-injection of isolectin B4 and Cholera toxin subunit B into the sciatic nerve of the rat. J Neurosci Meth. 2011;198:213-221
[5] Hoeber J, Trolle C, Konig N, et al. Human embryonic stem cell-derived progenitors assist functional sensory axon regeneration after dorsal root avulsion injury. Sci Rep. 2015;5:10666.
[6] Lai BQ, Qiu XC, Zhang K, et al. Cholera toxin B subunit shows transneuronal tracing after injection in an injured sciatic nerve. PLoS One. 2015;10:e0144030
[7] Charles Watson GS, Tanaka I, The Mammalian Spinal Cord. Atlas of the rhesus monkey spinal cord. Elsevier Academic Press. 2021.
[8] Khan MN, Cherukuri P, Negro F, et al. ERR2 and ERR3 promote the development of gamma motor neuron functional properties required for proprioceptive movement control. PLoS Biol. 2022;20:e3001923.
[9] Lai HC, Seal RP, Johnson JE. Making sense out of spinal cord somatosensory development. Development. 2016;143(19):3434-3448.



