NRR:重医附一院杨琴团队揭示重组Shh蛋白通过调控S100A10抑制缺血性卒中后神经元泛凋亡
撰写:王玲,杨琴
#br#
脑缺血引起的神经元死亡是缺血性卒中患者在中风发作后出现残疾和死亡的主要原因[1]。泛凋亡(PANoptosis)是一种新近报道的细胞死亡模式,具有细胞焦亡、凋亡和坏死性凋亡的关键特征[2-4],在缺血性脑损伤后的病理生理过程中起重要作用。然而,调控神经元泛凋亡的关键分子机制尚不明确。S100钙结合蛋白A10(S100
calcium-binding protein A10,S100A10),也称为p11[5],是S100蛋白家族的成员之一,参与调控炎症、增殖、能量代谢和凋亡等途径。在大脑中,S100A10主要在神经元中表达[6],在抑郁症、帕金森病、缺血性卒中和阿尔茨海默病等神经系统疾病中研究较多[7-10]。在脑血管疾病背景下,研究主要集中在星形胶质细胞上[11],尚不清楚S100A10是否以及如何调控神经元泛凋亡的发生。Sonic Hedgehog(Shh)信号通路具有抗凋亡,抗氧化应激等作用[12],能够减轻脑缺血性损害,但其是否参与S100A10介导的泛凋亡调控目前仍未知。
近期,重庆医科大学附属第一医院杨琴团队在《中国神经再生研究(英文)》(Neural Regeneration Research)上发表的研究发现缺血性脑损伤诱导神经元泛凋亡发生并且上调S100A10和Shh蛋白的表达,敲低S100A10会加剧神经元泛凋亡过程,给予外源性重组Shh蛋白干预后,S100A10表达有所增加,并且有效抑制神经元泛凋亡现象。该文带来的启示:S100A10 调节神经元泛凋亡的作用可能部分由Shh调控。王玲为论文第一作者,杨琴教授为论文通讯作者。
作者首先研究了急性缺血性卒中后S100A10的水平变化。通过对健康对照组以及急性缺血性卒中患者发病3天内的血清进行ELISA检测,发现患者血清中S100A10蛋白水平高于对照组。这提示S100A10可能作为内源性保护因子参与神经保护机制。此外,作者发现在大鼠缺血脑组织中S100A10蛋白水平高于假手术组。接下来为了确定表达S100A10的细胞类型,对脑组织切片进行多重免疫荧光染色,结果显示S100A10主要与神经元共定位(图1)。这些结果表明,S100A10在缺血神经元中的表达明显增加。
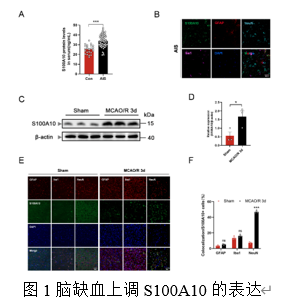
泛凋亡是一种新近报道的炎症性程序性细胞死亡,兼具细胞焦亡(pyroptosis)、凋亡(apoptosis)和坏死性凋亡(necroptosis)的关键特征。神经元死亡是缺血性卒中的病理特征[13-14]。为此,作者检测了缺血性脑损伤后是否诱导泛凋亡发生。结果显示缺血区域凋亡细胞与焦亡标志物(Caspase1)、凋亡标志物(Caspase3)及坏死性凋亡标志物(MLKL)均存在共定位现象,提示多个细胞死亡通路被同步激活。此外,缺血性脑损伤后泛凋亡相关蛋白表达显著上调以及神经元
ZBP1-泛凋亡小体形成(图2)。这些结果表明缺血性脑损伤诱导了泛凋亡发生。
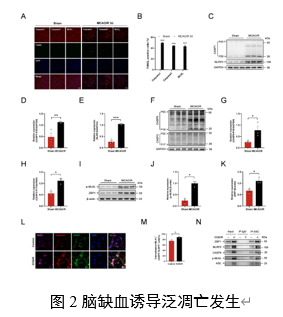
S100A10在缺血后神经元中表达上调,提示可能与缺血后神经元泛凋亡发生直接相关,
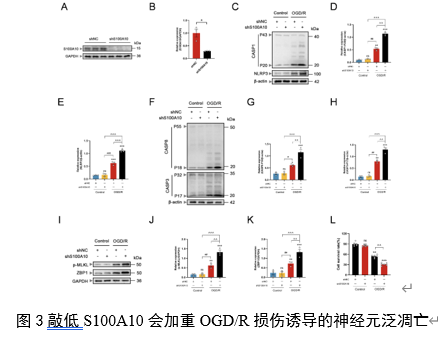
接下来作者利用慢病毒转染敲低S100A10来探讨其是否影响OGD/R后神经元泛凋亡。结果发现S100A10敲低增加了泛凋亡相关蛋白的表达,降低了神经元活力(图3)。既往研究表明Shh信号在调节缺血性脑损伤中起重要的作用。接下来探讨Shh 是否通过 S100A10
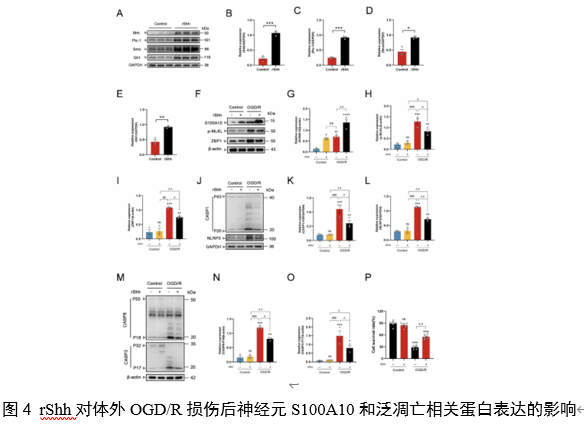
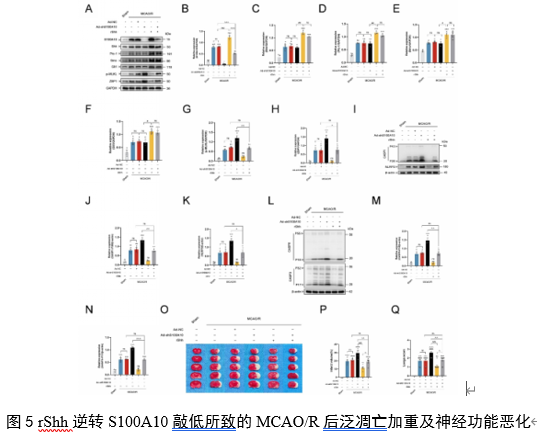
影响神经元泛凋亡。重组Shh蛋白干预后S100A10表达升高,神经元活力增加,泛凋亡相关蛋白水平有所下降(图4)。这些结果表明,重组Shh蛋白在体外上调 S100A10的表达,减轻泛凋亡,并促进OGD/R后的神经元存活。并且在体内进行了验证,敲低S100A10加剧MCAO/R
后泛凋亡、增加梗死体积、恶化神经功能,而重组Shh蛋白能逆转S100A10敲低的上述作用(图5)。
总之,S100A10对抑制缺血性脑损伤后神经元泛凋亡非常重要。作者的研究表明,S100A10的表达在缺血性脑损伤后升高,敲低S100A10会加剧神经元泛凋亡,上调S100A10可明显抑制神经元泛凋亡,改善神经功能。此项研究结果为早日开发新药干预缺血性脑损伤后神经元泛凋亡的发生,从而促进神经功能恢复奠定实验基础。#br#
当然,该研究也存在一定的局限性。首先,该研究仅验证MCAO/R模型,为了有更多的临床意义,未来的研究应该考虑在ET-1或光栓模型中重复;此外,该研究仅研究了发病后3天的时间点,可以考虑在其他有意义的时间点(如24小时内或7天) 进行进一步研究。 #br#
#br#
参考文献#br#
[1] Guo Q, Kawahata I, Cheng A, et al. Fatty acid-binding proteins 3 and 5 are involved in the initiation of mitochondrial damage in ischemic neurons. Redox Biol 2023;59:102547.#br#
[2] Malireddi RKS, Kesavardhana S, Kanneganti TD. ZBP1 and TAK1: Master regulators of NLRP3 inflammasome/pyroptosis, apoptosis, and necroptosis (PAN-optosis). Front Cell Infect Microbiol 2019;9:406.#br#
[3] Wang Y, Kanneganti TD. From pyroptosis, apoptosis and necroptosis to PANoptosis: A mechanistic compendium of programmed cell death pathways. Comput Struct Biotechnol J 2021;19:4641-4657.#br#
[4] Gao L, Shay C, Teng Y. Cell death shapes cancer immunity: spotlighting PANoptosis. J Exp Clin Cancer Res 2024;43(1):168.#br#
[5] Rescher U, Gerke V. S100A10/p11: family, friends and functions. Pflugers Arch 2008;455(4):575-582.#br#
[6] Milosevic A, Liebmann T, Knudsen M, et al. Cell- and region-specific expression of depression-related protein p11 (S100a10) in the brain. J Comp Neurol 2017;525(4):955-975.#br#
[7] Green H, Zhang X, Tiklova K, Volakakis N, et al. Alterations of p11 in brain tissue and peripheral blood leukocytes in Parkinson's disease. Proc Natl Acad Sci U S A 2017;114(10):2735-2740.#br#
[8] Guo H, Fan Z, Wang S, et al. Astrocytic A1/A2 paradigm participates in glycogen mobilization mediated neuroprotection on reperfusion injury after ischemic stroke. J Neuroinflammation 2021;18(1):230.#br#
[9] Chédeville AL, Lourdusamy A, Monteiro AR, et al. Investigating Glioblastoma Response to Hypoxia. Biomedicines 2020;8(9):310.#br#
[10] Svenningsson P, Chergui K, Rachleff I, et al. Alterations in 5-HT1B receptor function by p11 in depression-like states. Science 2006;311(5757):77-80.#br#
[11] Hernández IH, Villa-González M, Martín G, et al. Glial cells as therapeutic approaches in brain ischemia-reperfusion injury. Cells 2021;10(7):1639.#br#
[12] Dai R, Xia Y, Mao L, et al. Involvement of PI3K/Akt pathway in the neuroprotective effect of Sonic hedgehog on cortical neurons under oxidative stress. J Huazhong Univ Sci Technolog Med Sci 2012;32(6):856-860.#br#
[13] Yuan J. Neuroprotective strategies targeting apoptotic and necrotic cell death for stroke. Apoptosis 2009;14(4):469-77.#br#
[14] Hoque A, Hossain MI, Ameen SS, et al. A beacon of hope in stroke therapy-Blockade of pathologically activated cellular events in excitotoxic neuronal death as potential neuroprotective strategies. Pharmacol Ther 2016;160:159-79.#br#
#br#




