NRR:“智能支架+基因调控”双剑合璧!中国天津医科大学总医院冯世庆团队创新3D打印技术修复脊髓损伤
脊髓损伤是一种严重的神经系统疾病,常导致患者运动、感觉及自主神经功能障碍。巨噬细胞作为炎症微环境的核心调控者,在脊髓损伤后呈现明显的极化特征:促炎型M1巨噬细胞释放肿瘤坏死因子-α、白介素-6等促炎因子,抑制神经再生;而抗炎型M2巨噬细胞则分泌白介素-4、白介素-10等抗炎因子,促进组织修复[1-3]。
近年研究发现,干扰素调节因子(interferon regulatory
factor, IRF)家族中的干扰素调节因子5和干扰素调节因子4在巨噬细胞极化中发挥关键作用。干扰素调节因子5通过结合髓样分化因子88(myeloid differentiation factor 88, MyD88)促进M1极化,而干扰素调节因子4可能通过竞争性结合髓样分化因子88或激活信号转导与转录激活因子6(signal transducer and activator of transcription 6,
STAT6)促进M2极化。然而,干扰素调节因子4在脊髓损伤中的具体调控机制尚不明确,且现有干扰素调节因子4递送方法(如静脉注射或原位注射)存在靶向性差、药物代谢快等问题[4-7]。
在组织工程领域,3D打印水凝胶支架(3D-printed hydrogel scaffold)因其可定制化的孔隙结构和生物相容性,成为脊髓损伤修复的研究热点。其中,甲基丙烯酰化明胶(gelatin methacryloyl, GelMA)因其优异的机械性能和仿生特性被广泛应用[8-9]。然而,传统支架与宿主组织的接触面积有限,且缺乏对炎症微环境的主动调控能力。因此,如何构建一种兼具高效药物递送和免疫调控功能的智能支架,成为脊髓损伤修复领域亟待解决的关键问题。#br#
近日,天津医科大学总医院冯世庆团队在《中国神经再生研究(英文)》(Neural Regeneration Research)发表的研究构建搭载干扰素调节因子4蛋白的3D打印甲基丙烯酰化明胶支架,通过干扰素调节因子4/干扰素调节因子5轴调节巨噬细胞的极化,改善脊髓损伤后炎症微环境。研究表明,缓释的干扰素调节因子4蛋白通过竞争性结合髓样分化因子88抑制干扰素调节因子5的促炎作用,并通过激活信号转导与转录激活因子6通路促进M2型巨噬细胞极化,从而促进神经再生和脊髓功能恢复。该研究为脊髓损伤的修复提供了新的思路,为改善炎症微环境促进神经再生提供新的靶点。#br#
脊髓损伤引发的继发性损伤机制包括氧化应激和神经炎症等反应,导致神经功能严重丧失[10,11],该研究重点观察了通过3D打印甲基丙烯酰化明胶支架递送干扰素调节因子4蛋白对脊髓损伤后炎症反应的调节作用。研究通过分子对接发现干扰素调节因子4能够与髓样分化因子88结合,并且在干扰素调节因子4-髓样分化因子88-干扰素调节因子5共存的体系中,干扰素调节因子4能够竞争性地结合干扰素调节因子5与髓样分化因子88的结合位点。随后,分子动力学模拟结果提示干扰素调节因子4在不同结合体中的动态结构稳定,且未发生明显的构象变化。这表明,干扰素调节因子4能够通过稳定的结构与髓样分化因子88结合,从而有效抑制干扰素调节因子5的促炎作用,并维持蛋白功能的完整性。此结果揭示了干扰素调节因子4与髓样分化因子88和信号转导与转录激活因子6的结合作用,进而调节巨噬细胞的极化方向(图1)。#br#
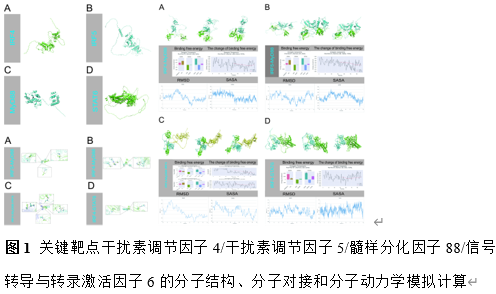
3D打印的甲基丙烯酰化明胶支架被用作药物递送载体,并通过脊髓损伤动物模型验证了其在脊髓损伤中的应用效果(图2)。结果显示,3D打印生物支架持续缓释干扰素调节因子4蛋白,促进了巨噬细胞从M1型极化转向M2型极化,改善了损伤部位的炎症微环境,促进了神经功能的恢复。促进脊髓损伤后运动、感觉和泌尿功能的恢复。此外,3D打印支架的机械性能和亲水性也使其成为理想的递送平台,有效增强了药物的局部释放和疗效。这一研究成果为脊髓损伤的治疗提供了新的治疗策略,并展示了3D打印技术在药物递送中的广泛应用潜力。
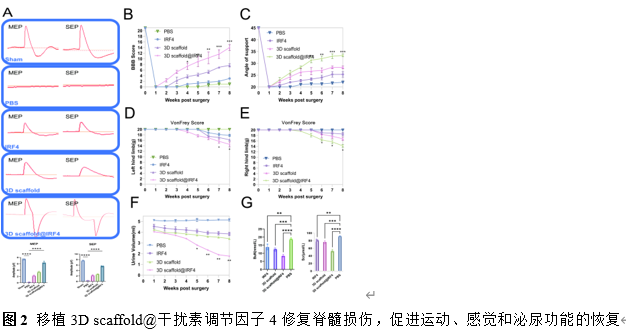
该研究通过增材制造制备3D scaffold@干扰素调节因子4,实现了干扰素调节因子4蛋白的持续释放,并通过调节巨噬细胞的极化促进脊髓损伤后的神经修复。研究结果表明,干扰素调节因子4蛋白通过抑制M1型巨噬细胞的极化并促进M2型巨噬细胞的极化,显著改善了损伤部位的炎症微环境,促进神经元和轴突的再生。尽管研究取得了积极成果,但干扰素调节因子4在不同类型脊髓损伤中的疗效仍需进一步验证,特别是对于慢性损伤的效果。此外,干扰素调节因子4的长期稳定释放、支架的降解速度和与宿主组织的整合性等问题也需要进一步研究。未来,靶向蛋白的联合治疗、3D打印支架药物释放性能优化,以及临床转化应用等方向,仍是该领域研究的重点。总体而言,该研究为脊髓损伤的治疗提供了新的思路,并为靶向蛋白递送系统的开发提供了宝贵的参考。#br#
#br#
参考文献#br#
[1] Rahman MM, Hwang SM, Go EJ, et al. Irisin alleviates CFA-induced inflammatory pain by modulating macrophage polarization and spinal glial cell activation. Biomed Pharmacother. 2024;178:117157.#br#
[2] Gordon S, Martinez FO. Alternative activation of macrophages: mechanism and functions. Immunity. 2010;32:593-604.#br#
[3] Zhou J, Li Z, Wu T, et al.LncGBP9/miR-34a axis drives macrophages toward a phenotype conducive for spinal cord injury repair via STAT1/STAT6 and SOCS3. J Neuroinflammation. 2020;17:134.#br#
[4] Fu SP, Chen SY, Pang QM, et al. Advances in the research of the role of macrophage/microglia polarization-mediated inflammatory response in spinal cord injury. Front Immunol. 2022;13:1014013.#br#
[5] Qin RX, Ma XY, Han ZY, et al. IRF2 Affects LPS- and IFN-γ-Induced Pro-Inflammatory Responses, Cell Viability, Migration and Apoptosis of Macrophages by Regulating IRG1. J Inflamm Res. 2024;17:9651-9664.#br#
[6] Tugal D, Liao X, Jain MK. Transcriptional control of macrophage polarization. Arterioscler Thromb Vasc Biol. 2013;33:1135-1144.#br#
[7] Wang J, Tian F, Cao L, et al. Macrophage polarization in spinal cord injury repair and the possible role of microRNAs: A review. Heliyon. 2023;9:e22914.#br#
[8] Koffler J, Zhu W, Qu X, et al. Biomimetic 3D-printed scaffolds for spinal cord injury repair. Nat Med. 2019;25:263-269.#br#
[9] Walsh CM, Wychowaniec JK, Brougham DF, et al. Functional hydrogels as therapeutic tools for spinal cord injury: New perspectives on immunopharmacological interventions. Pharmacol Ther. 2022;234:108043.#br#
[10] Anjum A, Yazid MD, Fauzi Daud M, et al. Spinal cord injury: pathophysiology, multimolecular interactions, and underlying recovery mechanisms. Int J Mol Sci. 2020;21:7533.#br#
[11] Hellenbrand DJ, Quinn CM, Piper ZJ, et al. Inflammation after spinal cord injury: a review of the critical timeline of signaling cues and cellular infiltration. J Neuroinflammation. 2021;18:284.#br#

