NRR:同济大学袁琼兰团队揭示5-羟色胺受体3在阿尔茨海默病中的作用机制
撰文:刘利芬、刘宇彤、袁琼兰
阿尔茨海默病最显著的病理特征是脑组织出现淀粉样蛋白β淀粉样斑,继而引起神经炎症、神经元和突触的损伤与丢失[1]。淀粉样蛋白β淀粉样斑是由细胞外沉积的淀粉样蛋白β和周围失营养的神经突起所构成,在阿尔茨海默病早期存在于大脑皮质和海马。而在海马中,淀粉样蛋白β斑主要位于中间神经元所在的区域[2, 3]。那么究竟是什么类型的神经元在疾病早期产生了淀粉样蛋白β淀粉样斑?目前尚无研究报道。对这一问题的揭示,可能为阿尔茨海默病疾病的生物标记和治疗提供潜在的靶标。
淀粉样蛋白β淀粉样斑学说是阿尔茨海默病的重要发病机制之一,但什么类型的神经元在疾病早期产生淀粉样蛋白β未见文献报道[1]。袁琼兰等意外发现阿尔茨海默病模型小鼠在淀粉样蛋白β出现的初期和淀粉样蛋白β未出现前的脑组织5-羟色胺受体3亚单位A(5-hydroxytryptamine type receptor 3 subunit A,HTR3A)表达显著增加,且阿尔茨海默病患者脑组织5-羟色胺受体3亚单位A表达也显著增加。5-羟色胺受体3亚单位A是构成功能性5-羟色胺受体3的必需亚单位[3],可丰富表达于大脑皮质和海马中间神经元中,尤其在海马中高表达[4]。那么,5-羟色胺受体3亚单位A中间神经元是否与位于中间神经元所在区域的淀粉样蛋白β淀粉样斑产生有关呢?
免疫双标共聚焦显微镜观察显示阿尔茨海默病模型小鼠5-羟色胺受体3亚单位A强阳性神经元与淀粉样蛋白β淀粉样斑产生有关(图1)。5-羟色胺受体3亚单位A是构成功能性5-羟色胺受体的必需亚单位,5-羟色胺受体是配体门控的离子型通道,对Ca2+,K+和Na+离子可通透[5, 6]。为进一步证实5-羟色胺受体3亚单位A中间神经元与淀粉样蛋白β产生有关,该研究团队用托烷司琼慢性干扰5-羟色胺受体3功能,可见阿尔茨海默病模型小鼠的认知缺陷明显改善,淀粉样蛋白β淀粉样斑及与之相关的神经炎症、5-羟色胺受体3亚单位A的表达也显著减少(图2和3);其机制可能与Ca2+/钙调神经磷酸酶/激活T-细胞核转录因子通路有关。这些结果表明,5-羟色胺受体3亚单位A中间神经元与淀粉样蛋白β淀粉样斑生成有关。
图1阿尔茨海默病模型小鼠和阿尔茨海默病患者脑组织增加的5-羟色胺受体3的表达(图源:Liu et al., Neural Regen Res, 2023)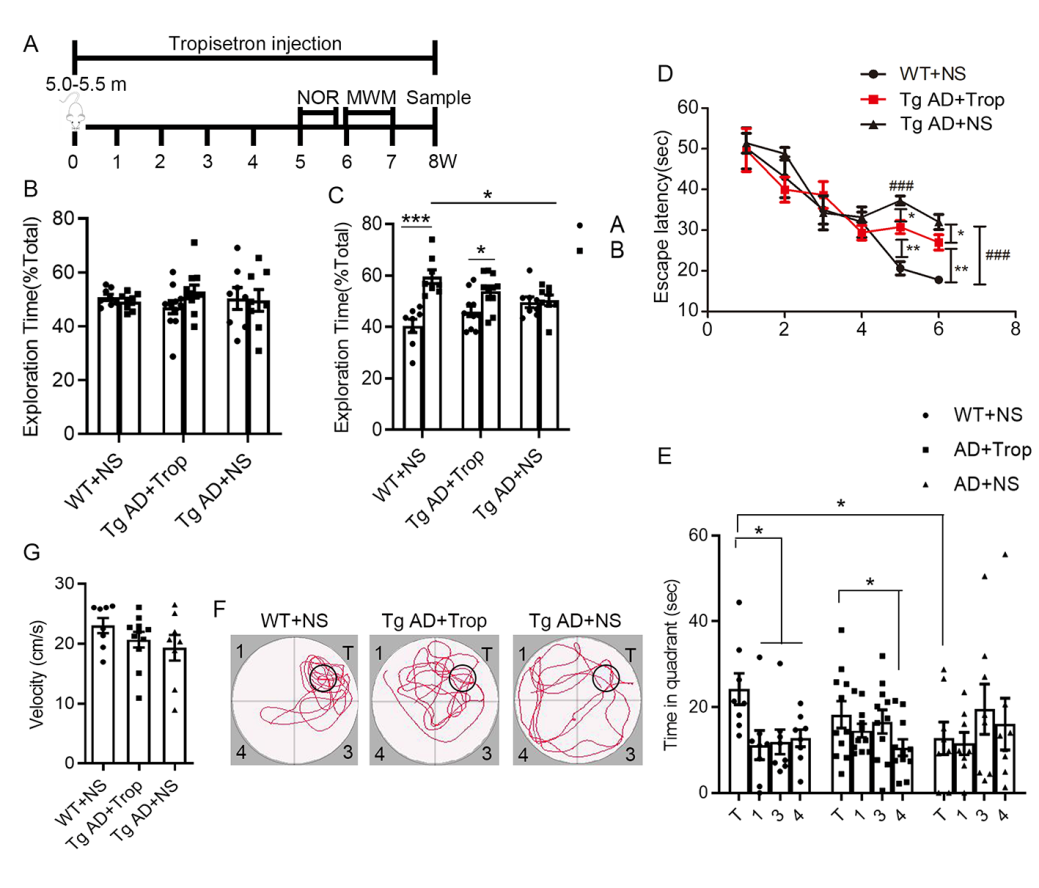
图2 慢性5-羟色胺受体3受体阻断剂托烷司琼减轻了阿尔茨海默病模型小鼠的认知障碍(图源:Liu et al., Neural Regen Res, 2023)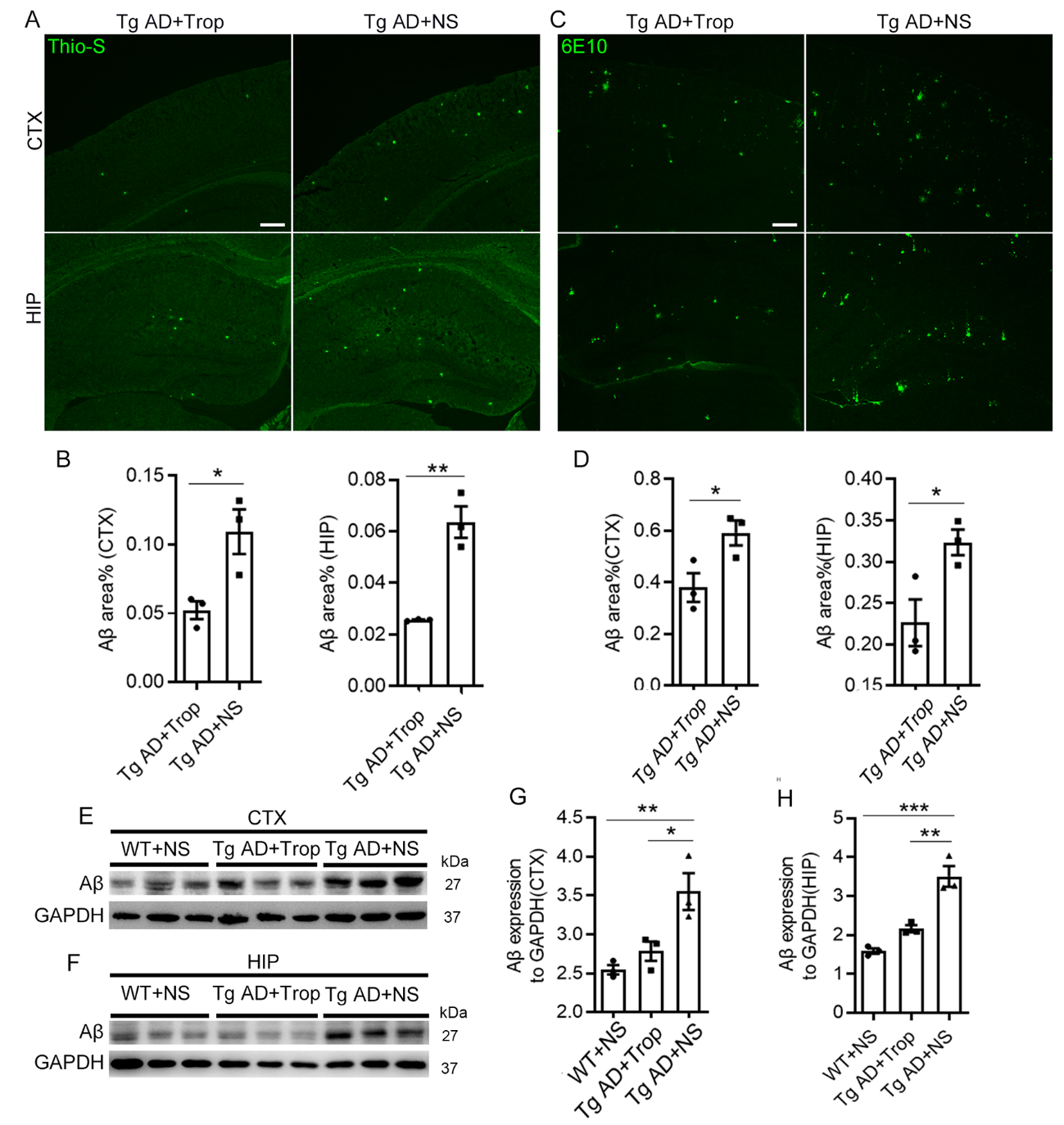
图3 慢性5-羟色胺受体3受体阻断剂托烷司琼减少了阿尔茨海默病模型小鼠脑组织淀粉样蛋白β淀粉样斑(图源:Liu et al., Neural Regen Res, 2023)
综上,阿尔茨海默病模型小鼠脑组织5-羟色胺受体3亚单位A表达显著增加,且在淀粉样蛋白β淀粉样斑出现前显著增加;5-羟色胺受体3亚单位A强阳性的中间神经元与淀粉样蛋白β斑的产生有关;重要的是阿尔茨海默病患者脑组织5-羟色胺受体3亚单位A表达也显著增加。用5-羟色胺受体3受体阻断剂调控慢性干扰,可改善小鼠的认知障碍及减少淀粉样蛋白β斑,并降低5-羟色胺受体3亚单位A的表达。由于5-羟色胺受体3亚单位A在物种间的高度保守性,此项研究结果为阿尔茨海默病治疗和早期的生物标记提供了新的靶标。该研究近期在《中国神经再生研究(英文版)》(Neural Regeneration Research)发表。
由于该研究在观察阿尔茨海默病患者脑组织5-羟色胺受体3亚单位A表达时,仅使用了蛋白杂交方法,仍需免疫双标确认5-羟色胺受体3亚单位A中间神经元与淀粉样蛋白β斑之间的关系。另外,干扰5-羟色胺受体3功能是用受体阻断剂,使用脑立体定位注射沉默5-羟色胺受体3亚单位A的腺病毒效果效果更能得到认可。
原文链接:https://doi.org/10.4103/1673-5374.366492
参考文献
[1] Hardy J, Selkoe DJ. The amyloid hypothesis of Alzheimer's disease: progress and problems on the road to therapeutics. Science. 2002;297(5580):353-356.
[2] Krauthausen M, Kummer MP, Zimmermann J, et al. CXCR3 promotes plaque formation and behavioral deficits in an Alzheimer's disease model. J Clin Invest. 2015;125(1):365-378.
[3] Liu L, Liu Y, Li N, et al. Multiple inflammatory profiles of microglia and altered neuroimages in APP/PS1 transgenic AD mice. Brain Res Bull. 2020;156:86-104.
[4] Koyama Y, Kondo M, Shimada S. Building a 5-HT3A receptor expression map in the mouse brain. Sci Rep. 2017;7:42884.
[5] Maricq AV, Peterson AS, Brake AJ, et al. Primary structure and functional expression of the 5HT3 receptor, a serotonin-gated ion channel. Science. 1991;254(5030):432-437.
[6] Mcmahon LL, Kauer JA. Hippocampal interneurons are excited via serotonin-gated ion channels. J Neurophysiol. 1997;78(5):2493-2502.
第一作者刘利芬为同济大学博士研究生。#br#
#br#
刘宇彤为共同第一作者。

袁琼兰教授,为该文通讯作者,是同济大学医学院课题组长、教授、博士研究生导师,从事神经精神疾病机制与干预研究。该项研究获得国家自然科学基金及上海市科技创新行动计划自然科学基金的支持。



