NRR:空军军医大学西京医院胡学昱团队提出光生物调节改善脊髓损伤后轴突生长的方法
撰文:张智昊、宋志文、罗亮、王哲、胡学昱
脊髓损伤作为一种神经系统疾病,可由外伤、车祸或高处坠落等外部因素引起,常导致运动、感觉和自主神经功能的丧失[1]。硫酸软骨素蛋白聚糖在脊髓损伤后瘢痕内和瘢痕周围聚集,且研究表明硫酸软骨素蛋白聚糖是脊髓损伤后轴突再生的主要抑制因子之一[2]。近年来,减少硫酸软骨素蛋白聚糖的表达,降低其在脊髓损伤后的生长抑制作用受到广泛关注,这对脊髓损伤后功能恢复具有重要的意义[3, 4],但临床推广仍面临诸多挑战。
光生物调节是一种副作用低且便于推广的治疗方法,在治疗退行性和创伤性中枢神经系统疾病方面有较好的效果[5]。来自中国空军军医大学西京医院胡学昱团队曾观察到810 nm光生物调节可有效调节脊髓损伤后硫酸软骨素蛋白聚糖的形成,减轻炎症反应,并显著改善运动功能[6]。然而,脊髓损伤后光生物调节促进硫酸软骨素蛋白聚糖清除的具体机制以及其干预硫酸软骨素蛋白聚糖的潜在靶点仍待阐明。
胡学昱等近期发表在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“Photobiomodulation inhibits the expression of chondroitin sulfate proteoglycans after spinal cord injury via the Sox9 pathway”的研究揭示了光生物调节对硫酸软骨素蛋白聚糖表达的作用。基于主成分分析验证了光生物调节对硫酸软骨素蛋白聚糖家族表达具有调节作用,并发现versican是光生物调节干预硫酸软骨素蛋白聚糖的关键靶分子之一,且发现MAPK/SOX9通路和Smad3/SOX9通路可能是这一过程中发挥调节作用。这项为光生物调节治疗脊髓损伤提供了治疗策略和理论支撑。
脊髓损伤可导致严重的永久性运动、感觉和自主神经丧失,且损伤神经元自身再生能力丧失和重建功能连接失败限制了其再生[7]。硫酸软骨素蛋白聚糖是脊髓损伤后抑制微环境的重要因素[2],因此降低脊髓损伤后硫酸软骨素蛋白聚糖含量成为治疗功能障碍的一种潜在方法,但其实际应用仍存在挑战[3, 4]。已发现光生物调节在临床上对脊髓损伤患者具有潜在的治疗效果,且对脊髓损伤后硫酸软骨素蛋白聚糖的表达具有调节作用[6, 8, 9],但其具体的调节机制和靶点尚不明确。因此对光生物调节干预硫酸软骨素蛋白聚糖表达的探究具有重要意义。
为验证光生物调节对脊髓损伤后硫酸软骨素蛋白聚糖家族分子表达的调节作用,胡学昱等在小鼠损伤部位皮下植入照射波长为810 nm的红外激光光纤,从损伤后即刻开始对小鼠进行照射治疗,每天1次,连续7d。结果显示,损伤组织中硫酸软骨素蛋白聚糖含量迅速积累,7d时达到峰值,之后的28d内逐渐下降。损伤后3,7,14和28d时,光生物调节均能下调硫酸软骨素蛋白聚糖表达水平。接下来采用免疫荧光共标方法更直观地验证了光生物调节对硫酸软骨素蛋白聚糖含量的影响。结果表明,光生物调节对脊髓损伤后硫酸软骨素蛋白聚糖的积累有重要的作用。
明确光生物调节对硫酸软骨素蛋白聚糖总体表达水平抑制后,胡学昱等进一步从生物信息学的角度对光生物调节的动态调控谱进行分析。首先在脊髓损伤后7d时对小鼠进行转录组测序,而后采用基因表型主成分分析对20种靶蛋白聚糖相关基因的表达进行分析,共识别出3个维度,这解释了总基因变异的90.36%,分别对应于维度1,2,3的66.9%、15.96%和7.5%;其中维度2中分子大部分朝同一方向移动,呈正相关负荷;而维度3中分子朝正负两方向移动。二维图可见光生物调节组与单纯损伤组在维度1和2中的分布与差异,这进一步证实脊髓损伤后光生物调节显著影响了蛋白聚糖相关基因的表达谱。对蛋白聚糖相关基因进行热图mRNA表达筛选和定量聚合酶链式反应验证也提示,与对照组相比,单纯脊髓损伤后7d时硫酸软骨素蛋白聚糖家族分子表达水平普遍上调,而光生物调节可抑制其表达,其中Versican是变化最显著的分子之一(图1)。提示光生物调节对脊髓损伤后蛋白聚糖相关基因的表达谱有显著影响,且Versican是潜在的干预靶点。
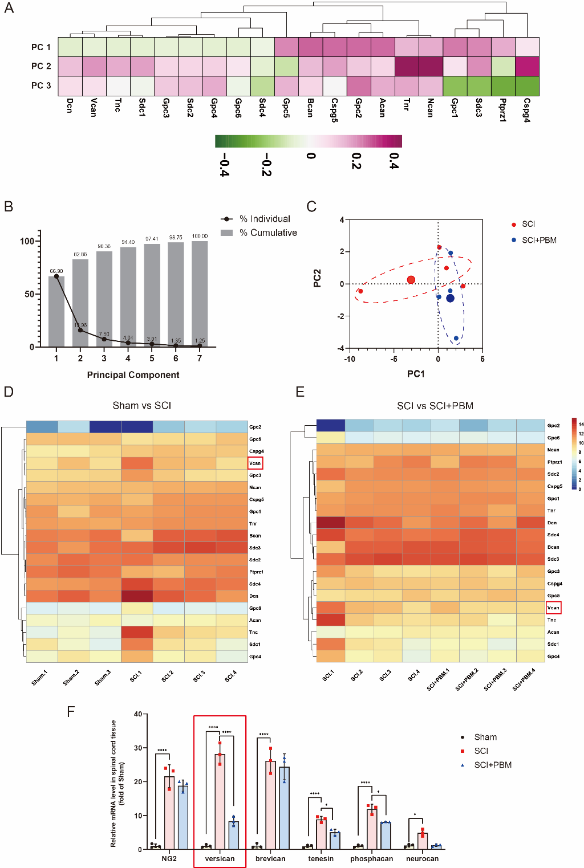
图1光生物调节可调控脊髓损伤后蛋白聚糖相关基因的分子表达谱(图源:Zhang et al., Neural Regen Res, 2023)
Versican是一种广泛表达的过渡基质蛋白聚糖,可在形态发生和生殖等生物学过程中发挥重要的作用[10, 11]。在炎症早期,Versican增加往往与白细胞侵袭同时发生,且Versican可通过透明质酸直接或间接地与炎症细胞产生相互作用而促进炎症反应的进展[12]。此外,在多发性硬化等中枢神经系统疾病中,Versican具有阻止修复、促进局部炎症进展以及加剧损伤的作用[13]。定量分析结果显示,Versican的表达在脊髓损伤后7d时达到峰值,随后逐渐下调,而光生物调节可下调Versican的表达。
在明确Versican可能是脊髓损伤后光生物调节干预硫酸软骨素蛋白聚糖表达的关键分子成分的基础上,胡学昱等进一步探索了光生物调节干预Versican表达的靶细胞。硫酸软骨素蛋白聚糖在脊髓损伤后主要由反应性星形胶质细胞分泌[14, 15],既往研究也证实光生物调节具有抑制星形胶质细胞炎症激活的作用[9]。因此实验验证了脊髓损伤后星形胶质细胞中Versican的表达。结果显示,脊髓损伤后,Versican存在于脊髓组织中星形胶质细胞中,且体外培养的原代星形胶质细胞在炎症诱导后Versican表达增加,而光生物调节可抑制其水平(图2)。
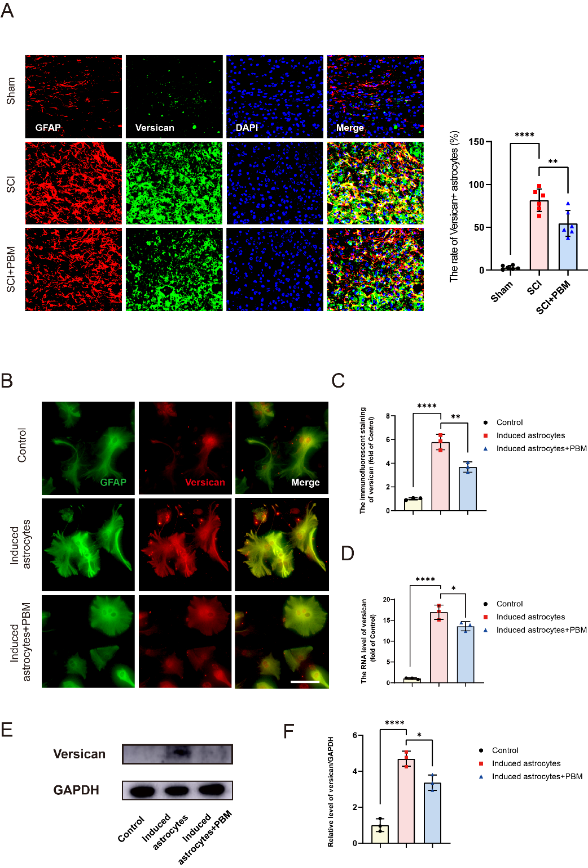
图2星形胶质细胞为光生物调节干预脊髓损伤后Versican表达的潜在靶细胞(图源:Zhang et al., Neural Regen Res, 2023)
既往研究发现,Smad3/Sox9通路和MAPK/Sox9通路都参与了硫酸软骨素蛋白聚糖的合成[16-18]。为探索光生物调节干扰星形胶质细胞Versican表达的具体机制,胡学昱等在体外实验中观察到在炎症刺激和光照后,磷酸化Smad3、磷酸化P38和磷酸化Erk的表达均发生了变化,但磷酸化JNK的表达却没有受到影响,因此推断Smad3/Sox9通路,P38/Sox9通路和Erk/Sox9通路可能参与了光生物调节对Versican表达的调控,而同为MAPK通路中的JNK通路可能在其中发挥的作用较小。为验证上述假设,在星形胶质细胞炎症诱导后,以FR 180204、SB 202190和(E)-SIS3分别特异性阻断Smad3、Erk和P38通路,可见Sox9和versican的上调。腹腔注射上述抑制剂也对小鼠损伤脊髓中Versican表达产生了相应的影响。这表明Versican可能是光生物调节干预脊髓损伤后硫酸软骨素蛋白聚糖表达的关键靶点,而Smad3/Sox9通路和MAPK/Sox9通路则是光生物调节发挥生物学功能的重要通路。
综上所述,胡学昱等确定了脊髓损伤后光生物调节干预硫酸软骨素蛋白聚糖的靶成分及相应的潜在通路,这有助于进一步理解光生物调节治疗脊髓损伤的机制。探索可能参与脊髓损伤病理过程的硫酸软骨素蛋白聚糖成分可能为未来干预提供潜在靶点。实验发现调控Sox9通路虽可抑制Versican在脊髓损伤后的表达,促进脊髓损伤正常运动功能的恢复,但Versican在脊髓损伤中发挥的具体作用仍需进一步研究。另外研究仅在脊髓损伤后急性期使用了光生物调节照射,延长照射时间是否能产生更好的治疗效果仍需进一步观察。
原文链接:https://doi.org/10.4103/1673-5374.374136
参考文献
[1] Alizadeh A, Dyck SM, Karimi-Abdolrezaee S. Traumatic spinal cord injury: an overview of pathophysiology, models and acute injury mechanisms. Front Neurol. 2019;10:282.
[2] Mukherjee N, Nandi S, Garg S, et al. Targeting chondroitin sulfate proteoglycans: an emerging therapeutic strategy to treat CNS injury. ACS Chem Neurosci. 2020;11(3):231-232.
[3] Bradbury EJ, Burnside ER. Moving beyond the glial scar for spinal cord repair. Nat Commun. 2019;10(1):3879.
[4] Tran AP, Warren PM, Silver J. The biology of regeneration failure and success after spinal cord injury. Physiol Rev. 2018;98(2):881-917.
[5] Salehpour F, Mahmoudi J, Kamari F, et al. Brain photobiomodulation therapy: a narrative review. Mol Neurobiol. 2018;55(8):6601-6636.
[6] Sun J, Zhang J, Li K, et al. Photobiomodulation therapy inhibit the activation and secretory of astrocytes by altering macrophage polarization. Cell Mol Neurobiol. 2020;40(1):141-152.
[7] Hutson TH, Di Giovanni S. The translational landscape in spinal cord injury: focus on neuroplasticity and regeneration. Nat Rev Neurol. 2019;15(12):732-745.
[8] Ma Y, Li P, Ju C, et al. Photobiomodulation attenuates neurotoxic polarization of macrophages by inhibiting the Notch1-HIF-1α/NF-κB signalling pathway in mice with spinal cord injury. Front Immunol. 2022;13:816952.
[9] Wang X, Li X, Zuo X, et al. Photobiomodulation inhibits the activation of neurotoxic microglia and astrocytes by inhibiting Lcn2/JAK2-STAT3 crosstalk after spinal cord injury in male rats. J Neuroinflammation. 2021;18(1):256.
[10] Mcculloch DR, Nelson CM, Dixon LJ, et al. ADAMTS metalloproteases generate active versican fragments that regulate interdigital web regression. Dev Cell. 2009;17(5):687-698.
[11] Dupuis LE, Mcculloch DR, Mcgarity JD, et al. Altered versican cleavage in ADAMTS5 deficient mice; a novel etiology of myxomatous valve disease. Dev Biol. 2011;357(1):152-164.
[12] Wight TN, Kang I, Evanko SP, et al. Versican-A critical extracellular matrix regulator of immunity and inflammation. Front Immunol. 2020;11:512.
[13] Ghorbani S, Jelinek E, Jain R, et al. Versican promotes T helper 17 cytotoxic inflammation and impedes oligodendrocyte precursor cell remyelination. Nat Commun. 2022;13(1):2445.
[14] Bradbury EJ, Moon LD, Popat RJ, et al. Chondroitinase ABC promotes functional recovery after spinal cord injury. Nature. 2002;416(6881):636-640.
[15] Silver J, Miller JH. Regeneration beyond the glial scar. Nat Rev Neurosci. 2004;5(2):146-156.
[16] Mckillop WM, Dragan M, Schedl A, et al. Conditional Sox9 ablation reduces chondroitin sulfate proteoglycan levels and improves motor function following spinal cord injury. Glia. 2013;61(2):164-177.
[17] Jahr H, Gunes S, Kuhn AR, et al. Bioreactor-controlled physoxia regulates TGF-β signaling to alter extracellular matrix synthesis by human chondrocytes. Int J Mol Sci. 2019;20(7):1715.
[18] Tew SR, Hardingham TE. Regulation of SOX9 mRNA in human articular chondrocytes involving p38 MAPK activation and mRNA stabilization. J Biol Chem. 2006;281(51):39471-39479.
 #br#
#br#
胡学昱,医学博士,西京医院骨科全军研究所副所长,西京骨科临床研究中心执行主任,博士生导师。长期从事脊髓、周围神经损伤修复以及脊柱疾病相关临床研究,主持国家自然科学基金、军队省部级课题9项,发表学术论文70篇,其中SCI论文45篇,通讯25篇,最高IF=10.68。主译专著2部,参编参译专著6部,获得国家发明专利9项,实用新型专利24项。获国家科技进步二等奖,陕西省科学技术一等奖,军队科技进步一等奖、国家教育部科技奖进步一等奖等10余项奖励。


 #br#
#br#