NRR:中国武汉科技大学脑科学先进技术研究院团队构建了一种可以挖掘阿尔茨海默病血液RNA改变及其临床关联性的数据库
#br#
撰文:胡斐斐,段婷婷
#br#
阿尔茨海默病于老年人群中的发病率极高,占痴呆病例中的60% - 80%,给社会及家庭带来了沉重负担 [1]。早期诊断对于干预病情进展起着至关重要的作用,然而当前的脑脊液和成像生物标志物因成本高昂、具有侵入性以及专业人员短缺等问题,极大地限制了其大规模应用。血液中的循环RNA,特别是外周血单个核细胞来源的RNA,为非侵入性监测阿尔茨海默病病理变化提供了可能。多项研究已证实其在区分阿尔茨海默病患者与对照个体方面具有潜力,例如血液中特定的mRNA(如TREM2)以及miRNA [2-4]。但是,目前阿尔茨海默病和轻度认知障碍中的血液RNA特征的研究仍存在不足。如相关研究缺乏统一的流程以及多组学整合,数据大多处于保密状态难以共享,并且多基于单一测序类型,对临床特征的考量不够全面,未综合分析患者性别、年龄、载脂蛋白E(Apolipoprotein E,ApoE)基因型以及总生存期等因素与血液RNA的关联。另外,现有的数据库专注于大脑组织RNA研究或阿尔茨海默病相关突变,缺乏探索阿尔茨海默病患者血液RNA变化的专用工具,这极大地限制了外周血生物标志物的挖掘以及相关诊断策略的发展。
中国武汉科技大学脑科学先进技术研究院团队在《中国神经再生研究(英文)》(Neural Regeneration
Research)上发表了一篇题为 “RBAD: The
first database dedicated alterations of blood RNA in individuals with
Alzheimer’s disease and their clinical relevance” 的研究。该研究通过整合1468个血液样本的 bulk RNA-seq、miRNA-seq和scRNA-seq数据,历经超过1100万次分析,获得了超过20000个血液特征,并基于这些分析结果构建了一个阿尔茨海默病血液RNA数据库(RBAD,http://www.bioinform.cn/RBAD/)。基于RBAD验证了阿尔茨海默病患者中嗅觉转导途径异常以及红细胞功能障碍,同时还发现了449种与生存相关的血液RNA以及2种与认知衰退相关的mRNA(H4C3和CTU1)。这些发现也表明RBAD为阿尔茨海默病生物标志物挖掘及外周致病机制研究提供了重要的工具。
随着阿尔茨海默病患病率的不断上升,现有诊断标志物受到诸多限制,虽然血液RNA研究已有一定进展,但仍缺乏系统性工具。该研究通过收集人类和小鼠的1468个血液样本的RNA-seq 数据,采用统一的流程进行了大约1120万次比较和相关性分析,构建了一个包含bulk RNA-seq、miRNA-seq、scRNA-seq和Clinical四个模块的RBAD网络服务器(图1)。其中,bulk RNA-seq模块针对血液RNA进行了差异表达分析、通路富集分析、免疫细胞丰度分析以及T细胞受体分析;miRNA-seq模块针对血液miRNA提供差异表达分析和通路富集分析;scRNA-seq模块针对血液单细胞RNA提供细胞注释、标记基因分析、细胞间基因差异分析以及通讯分析;Clinical模块评估血液RNA与临床特征的关联性。各模块协同作用,助力全面剖析阿尔茨海默病血液RNA特征。

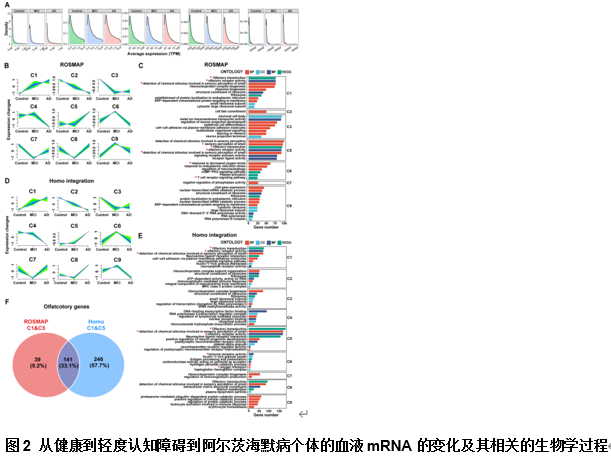
嗅觉衰退是阿尔茨海默病患者的早期症状 [5],但目前在血液中缺乏相关的分子证据。为了探究血液中是否存在可指示阿尔茨海默病患者嗅觉转导异常的生物标志物,该研究利用多个独立的转录组数据集,对比阿尔茨海默病、轻度认知障碍和健康对照血液的mRNA表达谱,进行聚类分析和分子通路富集。发现并验证了阿尔茨海默病或轻度认知障碍患者血液中嗅觉相关基因的mRNA水平显著升高(图2)。为了探究血液中嗅觉相关分子上调的机制,该研究进一步分析了创伤性脑损伤患者血液中神经来源外泌体的RNA-seq数据 [6],发现了嗅觉相关分子的上调。这一发现揭示了阿尔茨海默病患者血液中嗅觉转导相关RNA分子上调的潜在机制。然而,在对自湖北老年记忆队列的199名参与者进行的血浆蛋白组分析中,并未发现嗅觉相关蛋白产物的上调。这进一步强调了血液RNA分子能提供更全面、多样和深入的生物学信息,是阿尔茨海默病诊断的重要生物标志物来源。
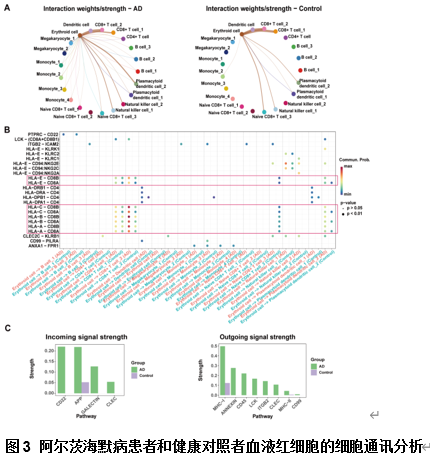
目前已有研究发现红细胞大小、数量和携氧功能的指标在痴呆中发挥着重要作用 [7],但是阿尔茨海默病患者红细胞指标变化的机制并不明确。为了验证阿尔茨海默病患者血液红细胞比例的改变并探究其机制,该研究综合分析了bulk RNA-seq、scRNA-seq以及湖北老年记忆队列的血液检测数据和血浆蛋白组数据,确证了阿尔茨海默病/轻度认知障碍 患者中红细胞的比例及数量低于健康个体,这与以往大规模流行病学研究结果是相符的 [7, 8]。然后,该研究进一步探究了阿尔茨海默病患者血液红细胞减少的机制,发现阿尔茨海默病患者血液红细胞的破损并未增加,表明红细胞减少可能不是由破损增加引起的。那么是否是红细胞生成减少呢?该研究发现阿尔茨海默病患者的红细胞的CD45显著上调了,且红细胞与GZMK+ CD8+ T细胞之间基于MHC-I的相互作用也增加了(图3)。CD45已被报道会中断红细胞分化为成熟红细胞 [9],而CD8+ T细胞可能对红细胞有杀伤作用,这可能是阿尔茨海默病血液中红细胞减少的机制。上述结果表明,红细胞功能障碍和相关的分子或许是阿尔茨海默病诊断的潜在指标,这为理解阿尔茨海默病病理机制补充了新视角.
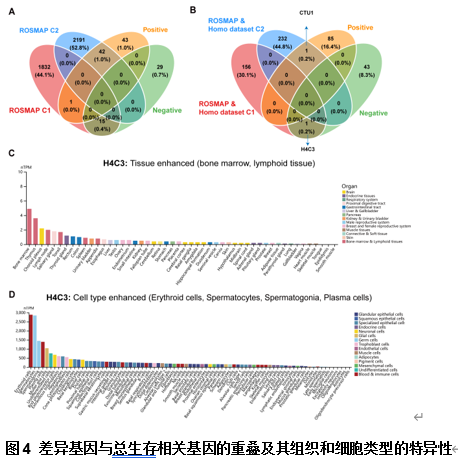
血液mRNA与阿尔茨海默病死亡率的关联尚不清楚。尽管阿尔茨海默病主要影响大脑,但其病理过程通常存在系统性的全身表现。例如,代谢、神经炎症和免疫系统调节提供了有关整体健康状况的信息,可以显著影响疾病轨迹和患者生存 [10]。为了探究血液 mRNA是否影响阿尔茨海默病患者的预后,本研究基于ROSMAP队列的随访数据进行了生存分析,结果表明449个血液mRNA的表达水平与阿尔茨海默病患者的总生存独立相关。这些基因的功能已被报道是与嗅觉系统、代谢过程和免疫反应相关的。其中,H4C3和CTU1还与2-3年后的认知衰退相关,而H4C3是红细胞特异表达基因(图4),这也再次印证了红细胞功能障碍与阿尔茨海默病的关联性。
总之,该研究构建的RBAD数据库是一个与阿尔茨海默病相关的血液RNA特征资源库,为研究基于血液的阿尔茨海默病外周发病机制和生物标志物提供了开创性资源,填补了阿尔茨海默病领域的一个重要空白。然而,研究也存在一定的局限性,如纳入的部分数据集样本量较小,限制了结果的普适性,尤其是在生存分析中高龄样本较多,无法推广至年轻阿尔茨海默病人群;缺乏蛋白质组学、代谢组学和表观遗传组学等多组学的整合,无法全面解析阿尔茨海默病发病机制。因此,在未来的研究中,将会扩大样本量、均衡队列,纳入更多的组学数据,从而深度挖掘阿尔茨海默病分子机制,提升RBAD的效能,为识别阿尔茨海默病血液生物标志物、改善阿尔茨海默病诊疗困境贡献力量。
原文链接:https://doi.org/10.4103/NRR.NRR-D-24-01165
参考文献#br#
[1]
No Authors Listed. 2023 Alzheimer's disease facts and figures. Alzheimers Dement. 2023;19(4):1598-1695.#br#
[2]
Tan YJ, Ng ASL, Vipin A, et al. Higher peripheral TREM2 mRNA levels relate to cognitive deficits and hippocampal atrophy in Alzheimer's disease and amnestic mild cognitive impairment. J Alzheimers Dis. 2017;58(2):413-423.#br#
[3]
Satoh J, Kino Y, Niida S. MicroRNA-Seq Data Analysis Pipeline to Identify Blood Biomarkers for Alzheimer's Disease from Public Data. Biomark Insights. 2015;10:21-31.#br#
[4]
Islam MR, Kaurani L, Berulava T, et al. A microRNA signature that correlates with cognition and is a target against cognitive decline. EMBO Mol Med. 2021;13(11):e13659.#br#
[5]
Hu FF, Cheng GR, Liu D, et al. Population-attributable fractions of risk factors for all-cause dementia in China rural and urban areas: a cross-sectional study. J Neurol. 2022;269(6):3147-3158.#br#
[6]
Bhomia M, Feng Y, Deleon P, et al. Transcriptomic signatures of neuronally derived extracellular vesicles reveal the presence of olfactory receptors in clinical samples from traumatic brain injury patients. Int J Mol Sci. 2024;25(5):2777.#br#
[7]
Qiang YX, Deng YT, Zhang YR, et al. Associations of blood cell indices and anemia with risk of incident dementia: A prospective cohort study of 313,448 participants. Alzheimers Dement. 2023;19(9):3965-3976.#br#
[8]
Faux NG, Rembach A, Wiley J, et al. An anemia of Alzheimer's disease. Mol Psychiatry. 2014;19(11):1227-1234.#br#
[9]
Long H, Jia Q, Wang L, et al. Tumor-induced erythroid precursor-differentiated myeloid cells mediate immunosuppression and curtail anti-PD-1/PD-L1 treatment efficacy. Cancer Cell. 2022;40(6):674-693.e7.#br#
[10]
Zheng X, Wang S, Huang J, et al. Predictors for survival in patients with Alzheimer's disease: a large comprehensive meta-analysis. Transl Psychiatry. 2024;14(1):184.#br#
#br#



