NRR:中国中山大学周治宇团队揭示脊髓损伤氧化应激相关诊断生物标志物及潜在调控机制
#br#
脊髓损伤是中枢神经系统的严重创伤疾病[1-3]。脊髓损伤急性期,损伤组织和血液迅速发生氧化应激反应[4-6]。此外,按照病情严重程度,脊髓损伤具有不同的病情分级[7]。在临床中,脊髓损伤的诊断和病情评估主要依靠磁共振检查和专科查体等检查。然而,部分磁共振检查不适用于体内有金属植入物的患者及不宜转运的危重患者。此外,由于部分患者在伤后会有脊髓休克和脊髓震荡症状,专科查体可能无法准确反映脊髓损伤的严重程度[8, 9]。研究发现,检测脊髓损伤患者血液中生物标志物的变化可能有助于预测病情的严重程度[4]。有研究发现脊髓损伤后红细胞氧化应激的变化可能是脊髓损伤的潜在生物标志物来源,但作为血液重要成分的免疫细胞的氧化应激变化是否也可能成为脊髓损伤的潜在生物标志物来源,目前尚不确定[5]。此外,研究表明,活性氧的过量产生和脂质过氧化是脊髓损伤后氧化应激损伤的关键机制[10, 11]。抑制脊髓损伤后的氧化应激反应有助于缓解继发性脊髓损伤并改善功能恢复[12, 13]。脊髓损伤中氧化应激反应的调控机制尚不完全清楚。
中国中山大学周治宇团队在《中国神经再生研究(英文)》(Neural Regeneration Research)上发表了题为“Integrating bulk and single-cell transcriptome profiling to uncover diagnostic biomarkers and regulatory mechanisms of oxidative stress in spinal cord injury”的研究,结果发现脊髓损伤及其病情严重程度相关的血液氧化应激生物标志物以及相关的特征性免疫变化,并通过进一步研究,揭示了脊髓损伤后氧化应激相关基因的时序表达模式,氧化应激相关的潜在通讯调控机制、转录调控特点、非编码RNA调控特点及相关的干预药物。文章结果为脊髓损伤氧化应激相关的诊断与治疗提供了新的思路和潜在方法。#br#
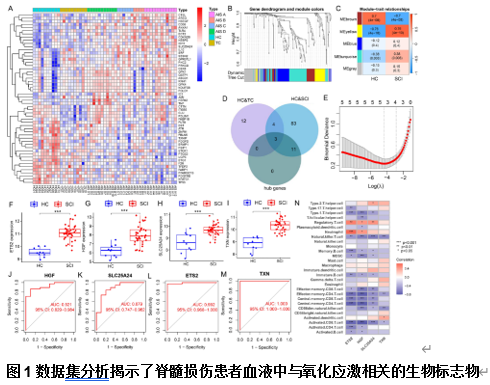
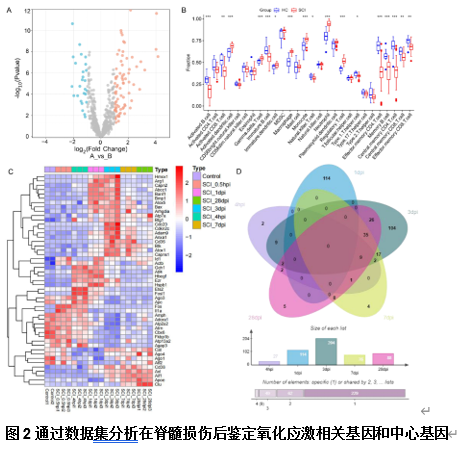
脊髓损伤患者血液中氧化应激相关基因呈现不同的表达特点。周治宇等通过分析脊髓损伤患者血液中氧化应激相关基因的表达特点,鉴定出脊髓损伤的4种个重要的氧化应激相关生物标志物ETS2,HGF,SLC25A24和TXN(图1)。研究还发现ETS2和HGF的表达与中性粒细胞和调节性T细胞含量呈正相关,SLC25A24的表达与调节性T细胞和辅助型T细胞2型呈正相关,而TXN与活化的树突状细胞呈正相关(图1)。鉴于脊髓损伤后血液中中性粒细胞、调节性T细胞和活化的树突状细胞显著增加(图2),检测这些生物标志物和血液中的免疫细胞变化有助于脊髓损伤的诊断。
 #br#
#br#
 #br#
#br#
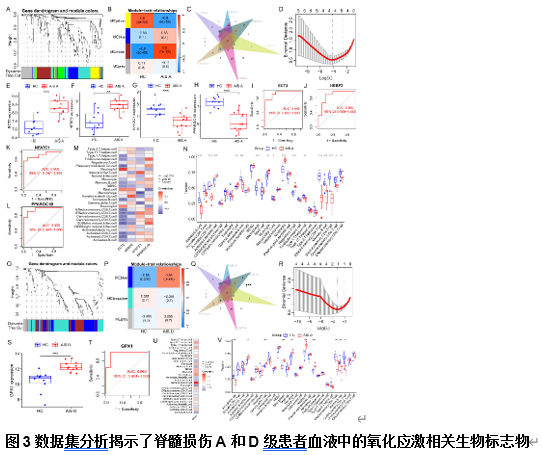
周治宇等也分析鉴定了4种重要的脊髓损伤A级特征性氧化应激相关生物标志物ECT2,HEBP2,NFATC1和PPARGC1B(图3)。研究发现ECT2表达与脊髓损伤A级患者血液中中性粒细胞的含量呈正相关,HEBP2与未成熟的树突状细胞含量呈正相关,NFATC1的表达与自然杀伤性T细胞含量呈正相关,PPARGC1B与CD56暗自然杀伤细胞和T滤泡辅助细胞的含量呈正相关(图3)。此外,脊髓损伤A级患者血液中的中性粒细胞含量显著增加,而自然杀伤性T细胞含量显著减少(图3)。因此,检测ECT2-中性粒细胞和NFATC1-自然杀伤性T细胞在血液中的协同变化可能有助于诊断脊髓损伤A级的病情诊断。也分析鉴定了4种重要的脊髓损伤D级特征性氧化应激相关生物标志物GPX1,且GPX1的表达与γδ T细胞含量呈正相关(图3)。文章发现,脊髓损伤D等级患者血液中γδ T细胞的含量显著增加(图4)。因此,检测血液中GPX1-γδ T细胞的协同变化可能有助于诊断脊髓损伤D级的病情诊断。
 #br#
#br#
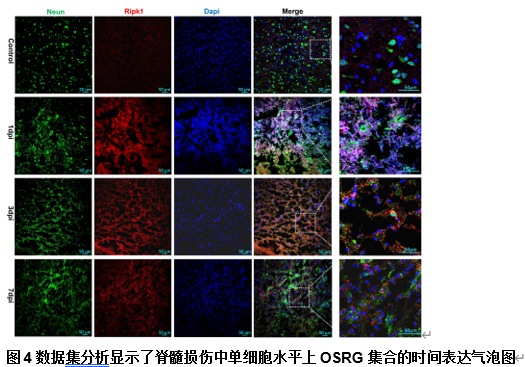
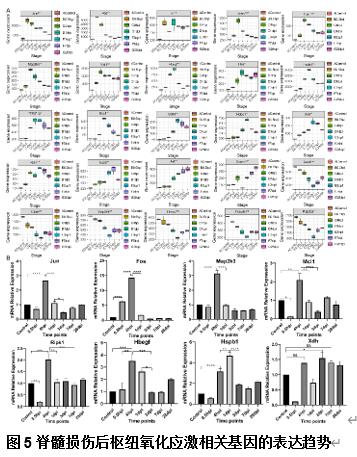
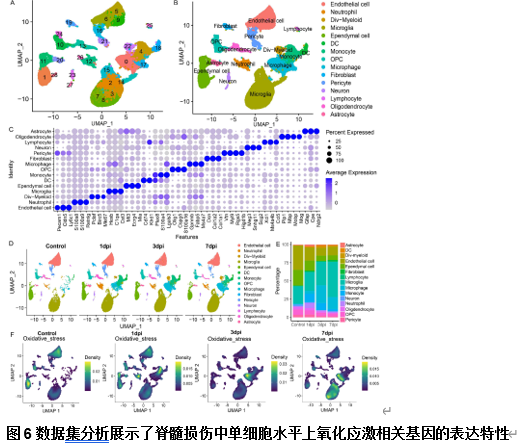
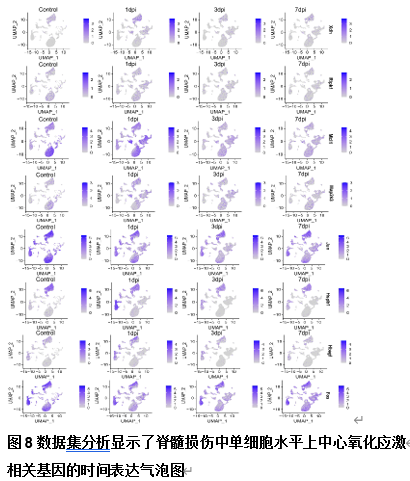
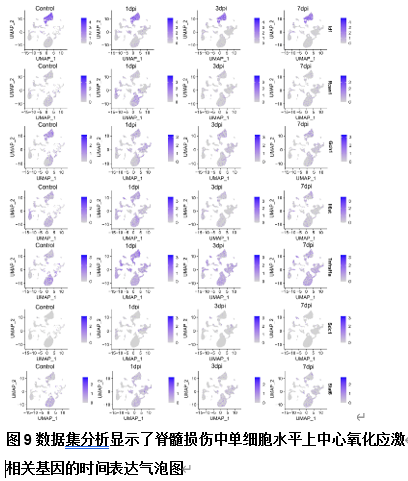
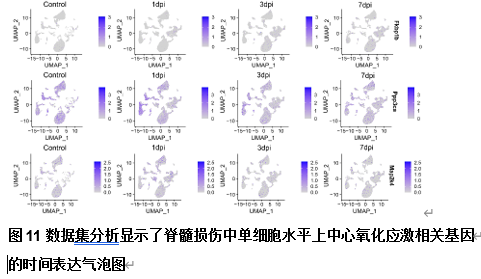
为分析脊髓损伤组织中氧化应激相关基因的时序表达模式,研究人员鉴定了脊髓损伤后的差异表达的氧化应激相关基因及枢纽基因。这些枢纽基因包括Xdh、Ripk1、Mcl1、Map2k3、Jun、Hspb1、Hbegf、Fos、Ucp2、Vcam1、Tnfrsf1a、Stat6、Sdc1、Rcan1、Ppp3ca、Map2k4、Il6st、Id1、Hdac1、Gch1、Fkbp1b、Fbxw7、Cbx6、Axl和Amph。并分析鉴定了这些基因的时序表达模式特点(图5)。并在单细胞水平对枢纽氧化应激相关基因的时序表达特点进一步分析了这些枢纽基因的表达模式(图4和6-11)。以为枢纽氧化应激相关基因的时序干预提供一定的依据。
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
为进一步揭示脊髓损伤后氧化应激的潜在调控机制,周治宇等在单细胞水平分析了不同细胞之间氧化应激相关的细胞通讯特点。对照组鉴定了5种氧化应激相关的通讯调控信号通路及配体受体对,如EGF信号通路(Hbegf-Erbb4, Hbegf-Egfr)、GAS信号通路(Gas-Axl)、OSM信号通路(Osm-(Osmr+Il6st), Osm-(Lifr+Il6st))、PROS信号通路(Pros1-Axl)和TNF信号通路(Tnf-Tnfrsf1a)(图12)。
 #br#
#br#
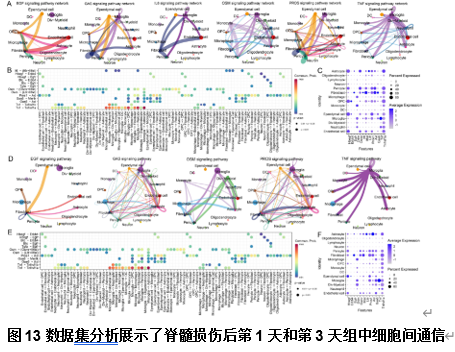
在脊髓损伤后第1天组中,研究人员鉴定了EGF(Hbegf-Erbb4, Hbegf-Egfr)、GAS(Gas-Axl)、IL6(Il6-(Il6r+Il6st))、OSM(Osm-(Osmr+Il6st), Osm-(Lifr+Il6st))、PROS(Pros1-Axl)和TNF(Tnf-Tnfrsf1a)在内的5条在脊髓损伤后具有潜在氧化应激通讯调控相关的信号通路及配体受体对(图7)。在脊髓损伤后第3天组中,研究人员鉴定了包括EGF(Hbegf-Erbb4, Hbegf-Egfr)、GAS(Gas-Axl)、OSM(Osm-(Osmr+Il6st), Osm-(Lifr+Il6st))、PROS(Pros1-Axl)和TNF(Tnf-Tnfrsf1a)在内皮的6条在脊髓损伤后具有潜在氧化应激通讯调控相关的信号通路及配体受体对(图13)。结合配体受体通讯强度及其在不同细胞中的表达水平,发现脊髓损伤后第1天及第3天这些信号通路对应的配体受体对分别在不同的细胞之间发挥着通讯调控作用(图13)。
 #br#
#br#
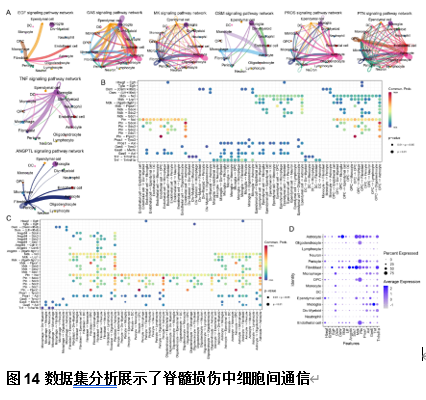
同样,研究人员也在鉴定了脊髓损伤后第7天组中,包括EGF(Hbegf-Erbb4, Hbegf-Egfr)、GAS(Gas-Axl)、OSM(Osm-(Osmr+Il6st), Osm-(Lifr+Il6st))、PROS(Pros1-Axl)、TNF(Tnf-Tnfrsf1a)、ANGPTL(Angptl4-Sdc1)、PTN(Ptn-Sdc1)和MK(Mdk-Sdc1)等8条在脊髓损伤后具有潜在氧化应激通讯调控相关的信号通路及配体受体对(图14)结合配体受体通讯强度及其在不同细胞中的表达水平,同样也发现脊髓损伤后第7天这些信号通路对应的配体受体对分别在不同的细胞之间发挥着通讯调控作用(图14)。
 #br#
#br#
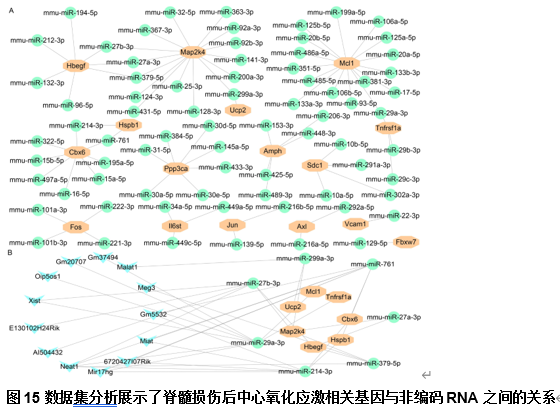
为鉴定脊髓损伤后调节枢纽 氧化应激相关基因的微小RNA和长链非编码RNA,研究人员使用了StarBase网站预测了在脊髓损伤后与枢纽 氧化应激相关基因相互作用的74种微小RNA,其中7种微小RNA因与2种基因同时发生相互作用而被确定为关键微小RNAs(图15)。随后,基于这些关键微小RNA,进一步预测了13种与它们相互作用的长链非编码RNA,并构建了mRNA-微小RNA-长链非编码RNA相互作用网络(图15)。这提示这些微小RNA和长链非编码RNA可能在调节脊髓损伤中氧化应激相关基因的表达中发挥重要作用。
 #br#
#br#
为鉴定脊髓损伤后氧化应激相关基因的转录调控特征,周治宇等检索了KnockTF数据库,并鉴定了与枢纽 氧化应激相关基因相互作用的104种转录因子,并区分了那些对目标基因具有抑制作用的转录因子,并在单细胞水平上鉴定了在对照组和各种受伤组中活性较高的转录因子(图16)。这可能为脊髓损伤中氧化应激的干预提供有价值的见解。
 #br#
#br#
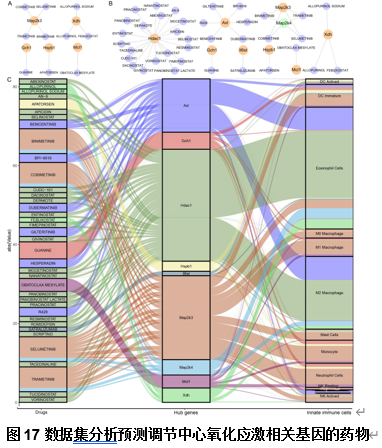
为鉴定脊髓损伤后调节枢纽氧化应激相关基因的药物,周治宇等基于DGIdb数据库筛选了38种抑制枢纽氧化应激相关基因的潜在候选药物。在损伤后4h,10种药物显示出对5种上调基因的抑制作用(图17)。在随后的1,3,7和28d中,38种已识别药物中的一些显示出对8种上调氧化应激相关基因中的特定基因以及1种下调OSRG的抑制作用。同时,研究人员还发现4种不同的药物对2种不同表达的与氧化应激相关的枢纽基因Map2k3和Map2k4产生影响。研究人员进一步分析发现了这些药物与9种枢纽氧化应激相关基因和固有免疫细胞之间的相互关系。上述研究为脊髓损伤中氧化应激的药物干预提供了一定的依据(图17)。
 #br#
#br#
文章确定了与人类脊髓损伤及其病情严重程度相关的氧化应激相关诊断生物标志物,有助于脊髓损伤严重程度的诊断和评估。此外,周治宇等还鉴定了脊髓损伤中的差异表达的氧化应激相关基因及其枢纽基因,揭示了这些枢纽基因在组织和单细胞水平上的时序表达模式。这些发现为脊髓损伤后氧化应激的时序靶向干预提供了一定的思路。周治宇等也发现并总结了脊髓损伤后不同时间点与氧化应激相关的细胞间通讯信号通路及相应的配体-受体对。也分析了调节枢纽基因的微小RNA和长链非编码RNA,并鉴定了脊髓损伤后不同时间点各种细胞中高表达的转录因子,阐明了它们对枢纽基因的影响。这些发现对于进一步了解脊髓损伤中与氧化应激相关的调节机制具有重要帮助。文章还进一步分析并总结了脊髓损伤后不同时间点抑制枢纽基因的药物,为对不同时间点枢纽基因的药物干预提供了一定的依据。因此,此次研究通过鉴定与脊髓损伤严重程度相关的诊断生物标志物,鉴定氧化应激相关基因表达模式,并探索与脊髓损伤中枢纽氧化应激相关基因相关的潜在调节机制和干预药物,为脊髓损伤的诊断和治疗研究提供了重要思路。未来将继续进行实验研究,以深入了解脊髓损伤氧化应激相关的血液诊断生物标志物与潜在的调控机制,为脊髓损伤的诊断与治疗提供更全面的思路和方法依据。
原文链接:https://doi.org/10.4103/NRR.NRR-D-24-00693
#br#
参考文献
[1] Barbiellini Amidei C, Salmaso L,
Bellio S, et al. Epidemiology of traumatic spinal cord injury: a large
population-based study. Spinal Cord. 2022;60(9):812-819.
[2] Quadri SA, Farooqui M, Ikram A, et
al. Recent update on basic mechanisms of spinal cord injury. Neurosurg Rev.
2020;43(2):425-441.
[3] Ahuja CS, Nori S, Tetreault L, et al.
Traumatic spinal cord injury-repair and regeneration. Neurosurgery.
2017;80(3s):S9-S22.
[4] Heller RA, Seelig J, Crowell HL, et
al. Predicting neurological recovery after traumatic spinal cord injury by
time-resolved analysis of monocyte subsets. Brain. 2021;144(10):3159-3174.
[5] Zhang LJ, Chen Y, Wang LX, et al.
Identification of potential oxidative stress biomarkers for spinal cord injury
in erythrocytes using mass spectrometry. Neural Regen Res.
2021;16(7):1294-1301.
[6] Takahashi H, Aoki Y, Saito J, et al.
Serum oxidative stress influences neurological recovery after surgery to treat
acutely worsening symptoms of compression myelopathy: a cross-sectional human
study. BMC Musculoskelet Disord. 2019;20(1):589.
[7] Zrzavy T, Schwaiger C, Wimmer I, et
al. Acute and non-resolving inflammation associate with oxidative injury after
human spinal cord injury. Brain. 2021;144(1):144-161.
[8] Marquis A, Packer RA, Borgens RB, et
al. Increase in oxidative stress biomarkers in dogs with ascending-descending
myelomalacia following spinal cord injury. J Neurol Sci. 2015;353(1-2):63-69.
[9] Li J, Liu X, Wang J, et al.
Identification of immunodiagnostic blood biomarkers associated with spinal cord
injury severity. Front Immunol. 2023;14:1101564.
[10] Catalá A, Díaz M. Editorial: Impact of
lipid peroxidation on the physiology and pathophysiology of cell membranes.
Front Physiol. 2016;7:423.
[11] Lam T, Chen Z, Sayed-Ahmed MM, et al.
Potential role of oxidative stress on the prescription of rehabilitation
interventions in spinal cord injury. Spinal Cord. 2013;51(9):656-662.
[12] Zhang C, Zhai T, Zhu J, et al. Research
progress of antioxidants in oxidative stress therapy after spinal cord injury.
Neurochem Res. 2023;48(12):3473-3484.
[13] Lv R, Du L, Zhang L, et al. Polydatin
attenuates spinal cord injury in rats by inhibiting oxidative stress and
microglia apoptosis via Nrf2/HO-1 pathway. Life Sci. 2019;217:119-127.
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#

 #br#
#br#

 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#