NRR:中科院动物所胡宝洋、王昱凯团队提出一种“现货型”神经细胞微球制剂的一站式制备方案
帕金森病是一种常见于中老年人的中枢神经系统退行性疾病,其主要发病机制是中脑黑质多巴胺能神经元退行性死亡,可导致纹状体多巴胺递质减少,进而造成运动障碍[1]。包括中国科学院动物研究所胡宝洋、王昱凯团队既往研究在内的多项工作表明,人多能干细胞分化来源的中脑多巴胺神经前体细胞可补充帕金森病动物模型缺失的神经细胞,并改善行为功能,这有望为帕金森病的治疗提供新的途径[2, 3]。然而在细胞制备过程中,酶消化和多次的离心吹打等操作带来的机械损伤以及细胞贴壁微环境的改变会严重影响中脑多巴胺神经前体细胞在体内的存活效果,这阻碍了中脑多巴胺神经前体细胞制剂在神经疾病治疗中的应用[4]。因此,如何在不影响细胞分化效率的基础上提高其可操作性,同时实现稳定的细胞制备与冻存,最终提高体内存活能力仍是一个亟待解决的重要问题。
最近胡宝洋、王昱凯团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“One-step cell biomanufacturing platform: porous gelatin microcarrier beads promote human embryonic stem cell-derived midbrain dopaminergic progenitor cell differentiation in vitro and survival after transplantation in vivo”的研究。该研究通过细胞和特定微载体的结合分化,建立了一种新型多巴胺神经细胞微球制剂的一站式制备工艺,并在500 mL体系下完成稳定的制备。细胞在分化完成后,直接以三维微球的形式冻存。该方法避免了对细胞的解离消化,维持了中脑多巴胺神经前体细胞神经纤维的完整性。与传统的细胞悬液相比,该微球制剂可显著提升细胞在注射后的存活能力,并减少移植区域的免疫反应。这一方法可为帕金森病等神经退行性疾病的细胞治疗提供有竞争力的现货型细胞产品。
在帕金森病的细胞治疗研究中,多巴胺神经前体细胞往往经历酶解消化以及多次吹打重悬后才注射至脑内,移植前的机械损伤和移植后的微环境应激均会严重影响细胞在体内的存活[1, 5]。为此,胡宝洋、王昱凯团队开发了一种适合中脑多巴胺神经前体细胞的小孔径明胶微载体(图1),该并尝试在人胚胎干细胞向中脑多巴胺神经前体细胞的分化过程中结合小孔径明胶微载体,最终获得三维细胞微球。
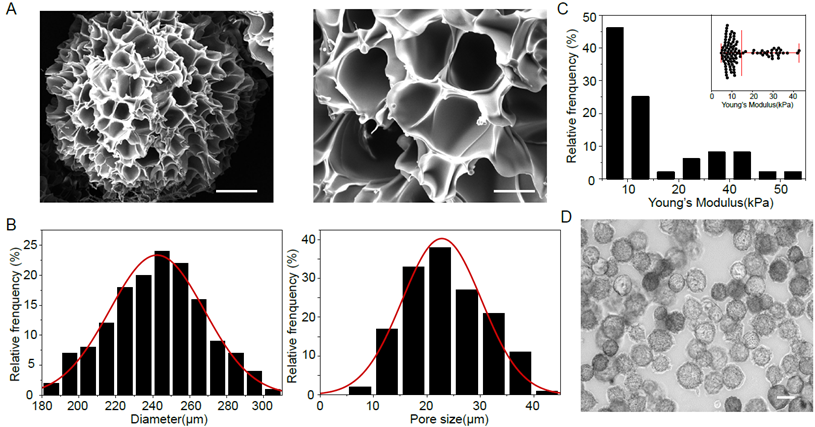
图1 与中脑多巴胺神经前体细胞相匹配的小孔径明胶微载体(图源:Feng et al., Neural Regen Res, 2024)
为优化细胞的三维分化条件,利用摇瓶生物反应器比较了不同的搅拌模式、接种时间点、接种密度等工艺参数(图2)。首先使用二维条件下未产生神经纤维(分化第11和17天)的细胞进行微载体接种和分化培养。分化到第25天时,第11天接种的细胞可见明显的聚团现象,且细胞存活率和分化效率均低于第17天接种的细胞。因此,在后续的三维分化中,选择了接种第17天的中脑多巴胺神经前体细胞至小孔径明胶微载体上。另外,在2种不同搅拌模式(恒定模式:搅拌速度持续保持为60 r/min;延迟模式:静止24h后以60 r/min开始搅拌)下进行了细胞接种,发现恒定模式下细胞的贴壁率明显低于延迟模式,说明接种后24h内设置静止时间可促进细胞黏附。进一步对细胞接种密度进行了探索,发现3-7×105个细胞/mg微载体的接种密度可实现中脑多巴胺神经前体细胞的高效分化,其中5×105密度分化的TH+、TUJ1+的细胞比例最高。通过以上分化工艺的优化,初步建立了基于小孔径明胶微载体的中脑多巴胺神经前体细胞分化体系,通过多个批次的验证确定了该体系的稳定性。

图2 中脑多巴胺神经前体细胞与小孔径明胶微载体结合分化工艺的筛选(图源:Feng et al., Neural Regen Res, 2024)
细胞的长期稳定保存是获得“现货型”细胞产品的重要基础,可使细胞在使用前接受充足的质量检测[6]。通过8种冷冻保存试剂对分化获得的中脑多巴胺神经前体细胞微球进行冻存和复苏,检测细胞存活率,以筛选可用的冻存试剂(图3)。液氮保存4周后,使用CS10和D10冻存的细胞的处理最高,分别达到86.9 ± 1.4%(CS10) 和83.4 ± 0.7%(D10),且细胞主要标志物的表达没有发生明显变化。与单细胞悬液相比,中脑多巴胺神经前体细胞微球的冻存不受细胞密度的影响,且能较好的维持神经细胞轴突的完整性。且这2种冻存试剂均不含血清或动物成分,符合cGMP生产要求,这极大地支持了该细胞产品的应用。

图3 中脑多巴胺神经前体细胞微球冻存体系的建立(图源:Feng et al., Neural Regen Res, 2024)
为评估中脑多巴胺神经前体细胞微球移植后的存活情况,将分化至25d的中脑多巴胺神经前体细胞悬液和中脑多巴胺神经前体细胞微球分别移植到免疫缺陷小鼠大脑纹状体中,3个月后通过脑切片染色比较2种制剂形式的体内表现(图4)。结果显示2组动物中存在存活的移植物,且中脑多巴胺神经前体细胞微球组细胞存活数量显著高于细胞悬液组,并且细胞没有过度生长。此外,与细胞悬液组相比,中脑多巴胺神经前体细胞微球组移植物中可见更多的FOXA2和TH双阳性多巴胺能神经元。免疫组化结果显示,中脑多巴胺神经前体细胞微球移植物周围的Iba1+小胶质细胞、GFAP+星形胶质细胞和CD3+ T细胞的数量均少于细胞悬液组,说明使用小孔径明胶微载体可减少移植部位炎症反应,有助于降低脑内移植物诱导的免疫排斥。
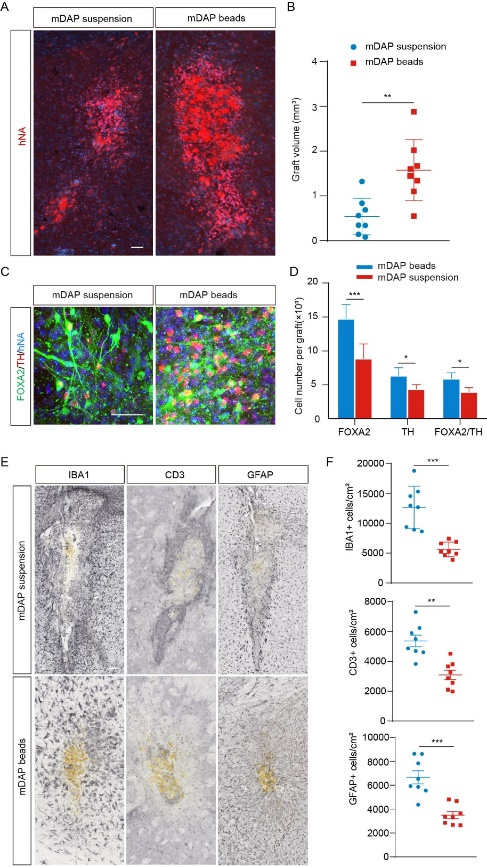
图4 中脑多巴胺神经前体细胞微球体内移植显示出较高的细胞存活率和较低的免疫排斥反应(图源:Feng et al., Neural Regen Res, 2024)
综上所述,基于微载体的神经细胞三维分化体系,能够(1)支持细胞的分化、成熟,并用于生产即用型中脑多巴胺神经前体细胞产品;(2)减少细胞收获带来的机械损伤并维持神经元轴突的完整性;(3)支持液氮冻存及复苏;(4)提高中脑多巴胺神经前体细胞移植物的存活,并降低移植区域的免疫反应。该研究结果将为神经类细胞制剂的开发和应用提供基础。#br#
但是这一实验没有关注生物材料在脑内的降解和残留,将来应考虑使用带有标记的载体来进行移植和体内观察。另外,该研究只评价了中脑多巴胺神经前体细胞微球移植后的存活情况,并没有进行细胞有效性的探究。接下来,需要利用帕金森病动物模型来检测中脑多巴胺神经前体细胞微球移植对疾病的治疗效果,以进一步评估该细胞制剂用于细胞替代疗法的治疗潜力。
原文链接:https://doi.org/10.4103/1673-5374.377412
参考文献
[1] Barker RA, Drouin-Ouellet J, Parmar M. Cell-based therapies for Parkinson disease-past insights and future potential. Nat Rev Neurol. 2015;11(9):492-503.
[2] Skidmore S, Barker RA. Challenges in the clinical advancement of cell therapies for Parkinson's disease. Nat Biomed Eng. 2023. doi: 10.1038/s41551-022-00987-y.
[3] Wang YK, Zhu WW, Wu MH, et al. Human clinical-grade parthenogenetic ESC-derived dopaminergic neurons recover locomotive defects of nonhuman primate models of Parkinson's disease. Stem Cell Reports. 2018;11(1):171-182.
[4] Trounson A, Dewitt ND. Pluripotent stem cells progressing to the clinic. Nat Rev Mol Cell Biol. 2016;17(3):194-200.
[5] Khaing ZZ, Ehsanipour A, Hofstetter CP, et al. Injectable hydrogels for spinal cord repair: a focus on swelling and intraspinal pressure. Cells Tissues Organs. 2016;202(1-2):67-84.
[6] Jang TH, Park SC, Yang JH, et al. Cryopreservation and its clinical applications. Integr Med Res. 2017;6(1):12-18.

第一作者:冯琳,中科院动物所博士。

第一作者:李达,中科院动物所工程师。

通讯作者:胡宝洋,中科院动物所研究员。

通讯作者:王昱凯,中科院动物所副研究员。
该团队主要从事干细胞与再生医学领域研究,重点关注多能干细胞向神经谱系的分化机制、人类神经发育和细胞分化的独特性以及干细胞医药学应用的系统化评估等科学问题。
此项研究得到国家重点研发计划、国家自然基金、中国科学院稳定支持基础研究领域青年团队计划、北京市科技重大专项的支持。







