NRR:同济大学的黄莺团队揭示有氧运动改善记忆和海马突触可塑性的新作用机制
撰写:来自颖,何晓倩
有氧运动促进突触可塑性,从而改善学习和记忆等认知功能。5-羟色胺(5-hydroxytryptamine,5-HT)系统因其与心理情绪表现和认知的功能联系而被广泛研究 [1]。5-羟色胺系统调节齿状回(dentate gyrus ,DG)的结构和神经元可塑性,与认知和情绪障碍有关[2]。在5-羟色胺受体家族中,5-羟色胺3受体是唯一配体门控的阳离子通道[3],并且特异性地表达在海马的胆囊收缩素/血管活性肠多肽含中间神经元中,调节快速突触传递[4]。此外,5-羟色胺3受体是运动诱导的海马神经发生必要条件[5]。并且抗精神病药物对5-羟色胺3受体的拮抗作用会阻碍接受抗精神病药物治疗的精神分裂症患者运动促进海马可塑性的治疗作用[6, 7]。既往研究表明5-羟色胺3受体在运动改善认知记忆中具有重要作用,但关于5-羟色胺3受体在运动促进海马突触可塑性的作用及机制研究仍不清晰。
近期,同济大学医学院黄莺团队在《中国神经再生研究(英文)》(Neural Regeneration Research)发表的研究发现,5-羟色胺3受体在运动促进小鼠海马CA3区突触可塑性和记忆中发挥关键作用。运动增加了海马齿状回中的神经发生和星形胶质细胞增殖以及脑源性神经营养因子的表达,从而促进了CA3中的长时程增强和记忆,该作用依赖于5-羟色胺3受体。本研究提供了5-羟色胺3受体在运动改善空间记忆和探索性记忆中的关键作用的证据,考虑到运动对神经退行性疾病的有益作用,5-羟色胺3受体可能成为治疗这些疾病的潜在靶点。何晓倩和来自颖为论文共同第一作者,黄莺教授为论文通讯作者
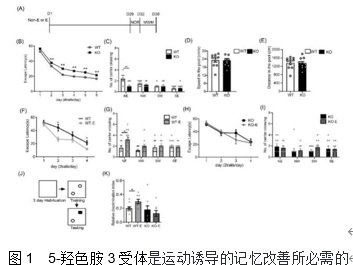
5-羟色胺系统在运动促进大脑功能中起着关键作用[5]。到目前为止,已经确定了14种5-羟色胺受体亚型。然而,究竟是哪一种5-羟色胺受体介导了这些运动诱导的神经元效应尚不清楚。5-羟色胺3受体在情绪和记忆中发挥重要作用[8],此前已有研究报道5-羟色胺3受体对跑步轮运动诱导的抗抑郁作用至关重要,但对学习和记忆却没有增强作用 [5]。研究者通过跑步机运动发现5-羟色胺3受体是有氧运动改善小鼠海马可塑性以及空间和探索性记忆所必需(图1)。研究的不同结果可能是由于实验中使用的不同运动模式和强度。
神经干细胞持续存在于成年哺乳动物的神经系统中[9],解剖和电生理学研究证明,这些细胞的持续产生、成熟和整合到海马回路中,对学习和记忆至关重要[10]。此外,广泛的研究已经证实,运动可以增强神经发生和认知[11]。5-羟色胺与运动对成年海马齿状回神经发生的影响相似[12]。研究者进一步以免疫荧光染色发现跑步机运动以5-羟色胺3受体依赖的方式增强了成年小鼠海马齿状回的神经发生。此外,作者还发现跑步机运动也通过5-羟色胺3受体促进了齿状回中星形胶质细胞的增殖,这可能是由于运动诱导的脑源性神经营养因子释放增加以及含有5-羟色胺3受体的GABA能中间神经元与星形胶质细胞之间的相互作用(图2)。
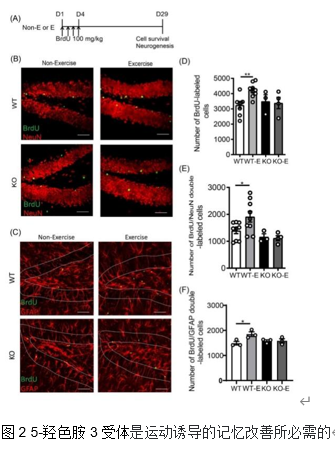
齿状回是海马中发生成人神经发生的主要区域。运动诱导的齿状回神经发生导致齿状回神经元释放更多脑源性神经营养因子[13-15]。增加的脑源性神经营养因子可以顺行运输并从CA3的轴突末端释放,为CA3锥体神经元提供营养支持[16],并促进CA3的突触可塑性。因此,研究者进一步通过膜片钳技术对海马CA3区进行场电位记录,发现运动诱导的CA3区长时程增强的增强依赖于5-羟色胺3受体(图3)。作者还检测了海马中突触可塑性相关蛋白突触后致密物-95、突触生长蛋白、脑源性神经营养因子的表达,发现运动可上调突触后致密物-95和脑源性神经营养因子的表达水平,而5-羟色胺3受体在运动增加脑源性神经营养因子水平中发挥重要作用(图4)。
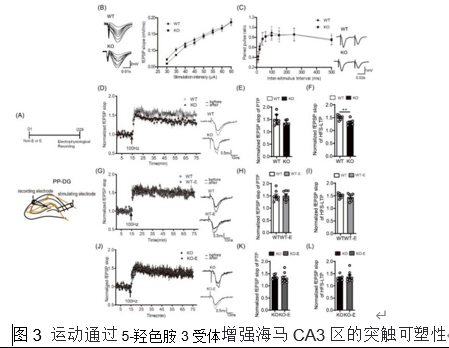
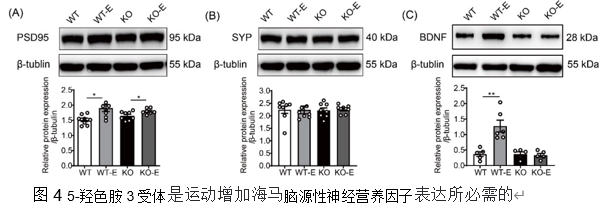
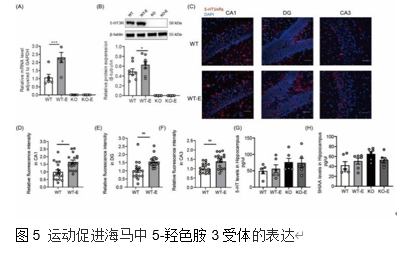
海马CA3的5-羟色胺能轴突密度最高,齿状回较低,CA1最低[17]。运动后大脑5-羟色胺水平增加[18, 19],这是运动诱导的成人海马神经发生所必需的[20]。研究者发现运动后海马中5-羟色胺3受体的表达增加,这将提高5-羟色胺激活5-羟色胺3受体的作用。
综上所述,该研究发现运动通过上调海马的5-羟色胺3受体增强海马齿状回的神经发生、星形胶质细胞增殖和脑源性神经营养因子的释放,促进海马长时程增强和记忆。更有趣的是,该研究发现5-羟色胺3受体对于运动增强CA3区的长时程增强至关重要,但在海马CA1或齿状回则不是必需的。然而,为了更详细地阐明5-羟色胺3受体调控运动诱导的CA3长时程增强的机制,在区域特异性条件敲除5-羟色胺3受体的小鼠中进行进一步的研究值得在未来的研究中进行。#br#
#br#
参考文献#br#
1. Pajonk FG, Wobrock T, Gruber O, et al. Hippocampal plasticity in response to exercise in schizophrenia. Arch Gen Psychiatry. 2010;67:133-143.#br#
2. Zhao C, Deng W, Gage FH. Mechanisms and functional implications of adult neurogenesis. Cell. 2008;132:645-660.#br#
3. Göthert M. Serotonin discovery and stepwise disclosure of 5-HT receptor complexity over four decades. Part I. General background and discovery of serotonin as a basis for 5-HT receptor identification. Pharmacol Rep. 2013;65:771-786.#br#
4. Férézou I, Cauli B, Hill EL, et al. 5-HT3 receptors mediate serotonergic fast synaptic excitation of neocortical vasoactive intestinal peptide/cholecystokinin interneurons. J Neurosci. 2002;22:7389-7397.#br#
5. Kondo M, Nakamura Y, Ishida Y, et al. The 5-HT3 receptor is essential for exercise-induced hippocampal neurogenesis and antidepressant effects. Mol Psychiatry. 2015;20:1428-1437.#br#
6. Rammes G, Eisensamer B, Ferrari U, et al. Antipsychotic drugs antagonize human serotonin type 3 receptor currents in a noncompetitive manner. Mol Psychiatry. 2004;9:846-858, 818.#br#
7. Kim DD, Barr AM, Honer WG, et al. Exercise-induced hippocampal neurogenesis: 5-HT(3) receptor antagonism by antipsychotics as a potential limiting factor in Schizophrenia. Mol Psychiatry. 2018;23:2252-2253#br#
8. Kelley SP, Bratt AM, Hodge CW. Targeted gene deletion of the 5-HT3A receptor subunit produces an anxiolytic phenotype in mice. Eur J Pharmacol. 2003;461:19-25.#br#
9. Urbán N, Blomfield IM, Guillemot F. Quiescence of Adult Mammalian Neural Stem Cells: A Highly Regulated Rest. Neuron. 2019;104:834-848.#br#
10. Cameron HA, Glover LR. Adult neurogenesis: beyond learning and memory. Annu Rev Psychol. 2015;66:53-81.#br#
11. Hong M, Kim M, Kim TW, et al. Treadmill exercise improves motor function and short-term memory by enhancing synaptic plasticity and neurogenesis in photothrombotic stroke mice. Int Neurourol J. 2020;24:S28-38.#br#
12. Micheli L, Ceccarelli M, D'Andrea G, et al. Depression and adult neurogenesis: Positive effects of the antidepressant fluoxetine and of physical exercise. Brain Res Bull. 2018;143:181-193.#br#
13. Kraemer RR, Kraemer BR. The effects of peripheral hormone responses to exercise on adult hippocampal neurogenesis. Front Endocrinol (Lausanne). 2023;14:1202349.#br#
14. Quesseveur G, David DJ, Gaillard MC, et al. BDNF overexpression in mouse hippocampal astrocytes promotes local neurogenesis and elicits anxiolytic-like activities. Transl Psychiatry. 2013;3:e253.#br#
15. Lee J, Duan W, Mattson MP. Evidence that brain-derived neurotrophic factor is required for basal neurogenesis and mediates, in part, the enhancement of neurogenesis by dietary restriction in the hippocampus of adult mice. J Neurochem. 2002;82:1367-1375.#br#
16. Smith MA, Zhang LX, Lyons WE, et al. Anterograde transport of endogenous brain-derived neurotrophic factor in hippocampal mossy fibers. Neuroreport. 1997;8:1829-1834.#br#
17. Mamounas LA, Mullen CA, O'Hearn E, et al. Dual serotoninergic projections to forebrain in the rat: morphologically distinct 5-HT axon terminals exhibit differential vulnerability to neurotoxic amphetamine derivatives. J Comp Neurol. 1991;314:558-586.#br#
18. Yang DS, Liu XL, Qiao DC. Dynamic changes of 5-HT, DA and their metabolin in rat striatum during exhaustive exercise and recovery. Zhongguo Ying Yong Sheng Li Xue Za Zhi. 2011;27:432-436.#br#
19. Béquet F, Gomez-Merino D, Berthelot M, et al. Exercise-induced changes in brain glucose and serotonin revealed by microdialysis in rat hippocampus: effect of glucose supplementation. Acta Physiol Scand. 2001;173:223-230.#br#
20. Klempin F, Beis D, Mosienko V, et al. Serotonin is required for exercise-induced adult hippocampal neurogenesis. J Neurosci. 2013;33:8270-8275.#br#




