NRR:中南大学江冰团队报道Rheb分子在视网膜神经元存活和轴突再生中的机制
撰文:蒋继宽
视网膜神经节细胞作为中枢神经系统的一部分很容易受到多种病理条件的影响,从而导致不可逆的视力丧失。成年哺乳动物的视神经节细胞再生能力非常有限,因此,探索保护视网膜神经节细胞存活和促进视神经损伤后再生的策略是目前研究的热点。Rheb是一种定位于溶酶体膜的小分子GTPase,激活的Rheb能够活化下游的雷帕霉素靶蛋白复合体(mTORC1)并介导蛋白质翻译、脂质核酸代谢等生理过程。既往研究表明,Rheb在神经极性[1]以及神经凋亡[2]方面有调控作用。过表达Rheb能够在多巴胺能神经元损伤模型中发挥保护作用[3-6],且有助于促进脊髓损伤后感觉神经轴突的再生[7],但其具体作用机制尚未完全阐明。
来自中国中南大学江冰团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“Phosphorylated S6K1 and 4E-BP1 play different roles in constitutively active Rheb-mediated retinal ganglion cell survival and axon regeneration after optic nerve injury”的研究。该研究发现,Rheb/mTOR通路在视神经损伤模型中具有保护作用,其不仅增加了视神经节细胞的存活率,而且促进了受损的视神经再生,进而改善了视功能。这些保护作用与mTORC1下游效应子S6K1和4E-BP1有关,且后二者在介导神经保护作用中扮演着不同的角色。这提示,Rheb可能作为一个神经保护的靶点,在未来视神经损伤的治疗中起关键作用。
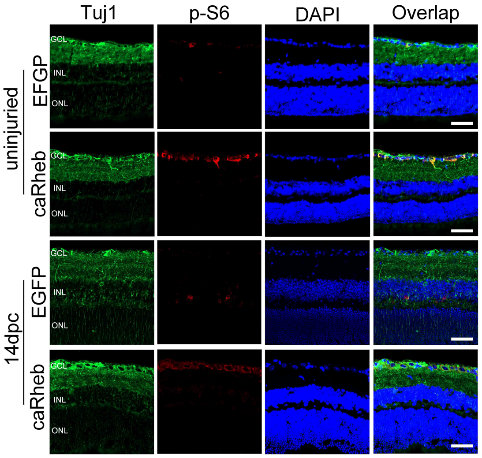
视神经损伤后,视网膜神经节细胞内源性再生能力下降,其中mTOR通路活性也显著下调[8]。因此,江冰等首先通过玻璃体腔注射AAV2的方式转染持续激活型Rheb突变型Rheb(S16H)和增强绿色荧光蛋白到视网膜节细胞后发现,p-S6阳性节细胞百分比从约30%增加到70%左右,甚至在夹伤14d后仍保持较高水平(图1),这表明Rheb能够诱导视网膜神经节细胞中mTOR通路持续激活。且发现,无论是在夹伤后急性期(14d),亦或是慢性期(21和42d),Rheb过表达都能够增加视网膜神经节细胞的存活率(图2)。α视网膜神经节细胞是一种高内源性mTOR活性的视网膜神经节细胞亚型,既往研究表明其对损伤具有较强的抗性,且有潜在的再生能力[9, 10]。实验使用特异性抗体标记存活的α视网膜神经节细胞后发现,Rheb过表达对α视网膜神经节细胞存活率的影响并不显著,而能增加非α视网膜神经节细胞数量(图3)。这一结果表明,通过外源性激活mTOR活性主要对低内源性mTOR活性的视网膜神经节细胞亚型起作用,从而验证mTOR活性对于视网膜神经节细胞存活的重要性。
 #br#
#br#
图1 Rheb过表达可持续性激活视网膜神经节细胞中mTOR通路(图源:Jiang et al., Neural Regen Res, 2023)
 #br#
#br#
图2 Rheb过表达可增加视神经夹伤后视网膜神经节细胞的存活率(图源:Jiang et al., Neural Regen Res, 2023)
 #br#
#br#
图3 Rheb的保护作用主要体现在非α视网膜神经节细胞上(图源:Jiang et al., Neural Regen Res, 2023)
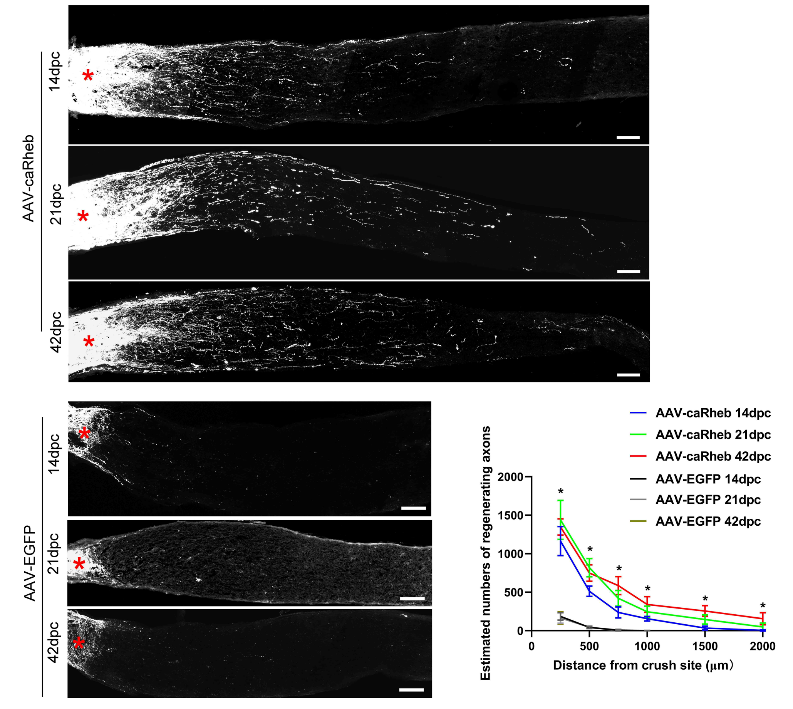
接下来,江冰等继续探究Rheb是否也能诱导视神经损伤后再生。通过玻璃体腔内注射偶联荧光基团的霍乱毒素B亚基(CTB)来标记穿越病变部位的再生轴突。定量结果显示,Rheb过表达组在视神经夹伤后第14,21和42天时均诱导了显著的轴突再生,而对照组几乎未见再生现象(图4)。同时闪光刺激视觉诱发电位检查也发现,与增强绿色荧光蛋白对照组相比,Rheb能够改善视功能,并显著增加P1波幅(图5)。这说明了Rheb对损伤后视神经再生和视功能恢复有显著的保护作用。
 #br#
#br#
图4 Rheb可促进损伤视神经的再生(图源:Jiang et al., Neural Regen Res, 2023)
 #br#
#br#
图5 Rheb可促进视神经夹伤后视功能的恢复(图源:Jiang et al., Neural Regen Res, 2023)
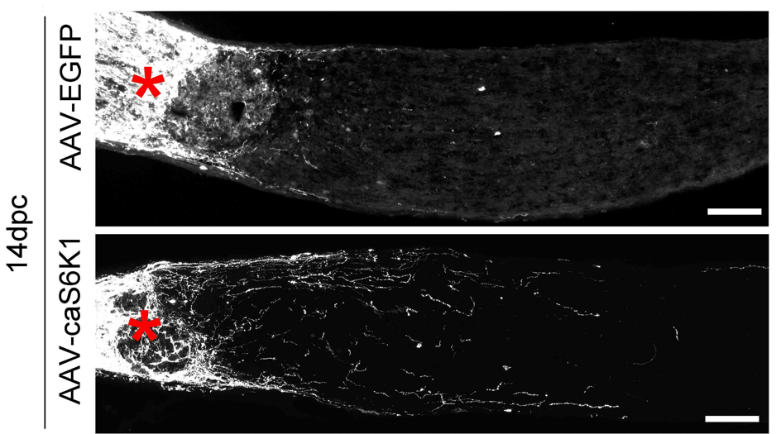
作为Rheb-mTOR通路的重要效应分子,S6K1在其中的作用是此次实验的重点之一。既往研究显示,S6K1在神经再生中存在双重作用:激活S6K1一方面可诱导神经极性并延伸神经细胞轴突[11],另一方面其又会反馈性抑制PI3K/Akt通路,并在一些条件下表现出对轴突生长的抑制作用[12]。为此,江冰等构建了以AAV2为载体的S6K1显性失活突变体(DN-S6K1)和AAV2-S6K1持续激活型突变体(AAV2-caS6K1)。结果可见,与单独AAV-Rheb相比,混合注射AAV-DN-S6K1和AAV-Rheb可明显减少再生轴突的数量(图6)。然而,即便有减少,其再生轴突数量仍然远多于增强绿色荧光蛋白对照组。单独注射caS6K1同样可诱导中等数量的再生轴突(图7)。另外,与单独注射AAV-Rheb相比,混合AAV-caS6K1和AAV-Rheb后的再生数量略有增加(图6)。这些结果表明,S6K1的活性对视神经节细胞轴突再生起积极作用,且是Rheb发挥作用的重要下游效应物,但S6K1的显性失活突变体并不能完全阻断Rheb诱导的再生,因此推测还其可能存在其他下游效应物。
 #br#
#br#
图6 Rheb诱导的轴突再生需要S6K1激活和4E-BP1抑制(图源:Jiang et al., Neural Regen Res, 2023)
 #br#
#br#
图7 S6K1的激活能够单独诱导轴突再生(图源:Jiang et al., Neural Regen Res, 2023)
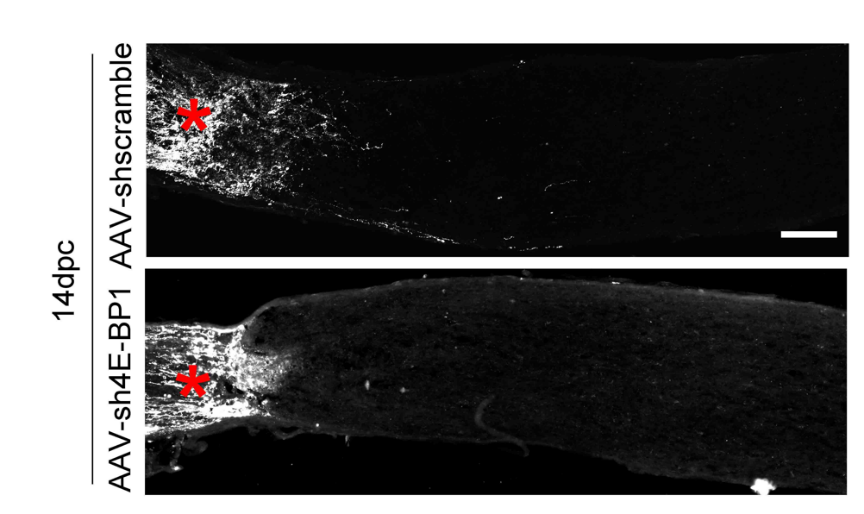
4E-BP1也可能作为另一个潜在的下游效应子参与轴突伸长,其功能受到mTORC1的抑制。为研究4E-BP1在视神经夹伤中的作用,江冰等接下来使用了携带4E-BP1-4A(一种对mTORC1不敏感的突变体)的AAV2病毒载体。与单独使用AAV-caRheb相比,混合4E-BP1-4A后,再生轴突数量明显减少,甚至近乎完全消除了轴突的生长,以至与对照组的结果相当(图6)。这表明,4E-BP1的磷酸化/抑制是caRheb诱导轴突再生的必要条件。然而,通过sh4E-BP1特异性敲低视网膜神经节细胞中4E-BP1后,却并没有观察到再生的出现(图8),这说明4E-BP1的抑制并不具备单独诱导再生的能力。
 #br#
#br#
图8 敲低4E-BP1不足以单独诱导轴突再生(图源:Jiang et al., Neural Regen Res, 2023)
明确了S6K1和4E-BP1在轴突再生中的作用后,江冰等继续探究了二者在视网膜神经节细胞存活中的作用。实验对分别转染了S6K1两种突变体的小鼠建立了视神经夹伤模型。视神经夹伤2周后,caS6K1组存活的视网膜神经节细胞数量显著高于增强绿色荧光蛋白组,而DN-S6K1组和增强绿色荧光蛋白组则没有显著差异(图9)。这说明S6K1的激活也有利于视网膜神经节细胞的存活。由于此前已阐明了4E-BP1的磷酸化可在轴突再生中起关键作用,因此预计4E-BP1对视网膜神经节细胞存活也有类似的影响。然而AAV介导的4E-BP1敲低(AAV-sh4E-BP1)的结果却意外的表明,与AAV-EGFP组相比,敲低组存活的视网膜神经节细胞数量减少;而4E-BP1-4A在视网膜中的过表达却进一步增加了存活的视网膜神经节细胞数量(图9)。这些结果表明,与轴突再生不同,4E-BP1的功能可能对视网膜神经节细胞的存活起积极作用。
 #br#
#br#
图9 视网膜神经节细胞的存活需要S6K1和4E-BP1的活性(图源:Jiang et al., Neural Regen Res, 2023)
鉴于上述发现,江冰等认为4E-BP1过表达可能通过独立于Rheb/mTOR的不同通路发挥保护作用。因此,实验进一步对比了混合注射AAV-Rheb和AAV-4E-BP1-4A是否比单独注射AAV-Rheb对视网膜神经节细胞生存具有更大的益处。结果显示,与单独注射caRheb相比,共表达caRheb和4E-BP1-4A对视网膜神经节细胞存活确实有着更强的保护作用(图10)。这些结果说明,caRheb表达后,内源性4E-BP1失活可通过外源性4E-BP1过表达来补偿,并进一步促进视网膜神经节细胞的存活。
 #br#
#br#
图10 Rheb和4E-BP1的互补调节可显著提高视网膜神经节细胞的生存率(图源:Jiang et al., Neural Regen Res, 2023)
这一实验在视神经夹伤小鼠模型中验证了Rheb/mTOR通路在视网膜神经节细胞保护和视神经再生中的作用及机制。其发现通过在视网膜神经节细胞中特异性过表达Rheb能够显著减少其死亡并有效诱导损伤轴突的再生,同时也对夹伤后小鼠视功能有一定程度的改善。Rheb对神经的保护作用主要通过影响下游S6K1和4E-BP1来实现的。而S6K1和4E-BP1磷酸化对轴突再生起到有益的作用,但二者在促进视网膜神经节细胞存活方面的作用并不一致。S6K1磷酸化可促进视网膜神经节细胞的存活,而4E-BP1磷酸化的作用刚好相反。鉴于神经存活和轴突再生的细胞和分子机制的复杂性,实验提供了一种针对Rheb及其下游效应子的神经保护新策略。但是由于AAV的转染通常需要至少2周时间,而损伤早期即发生了视网膜神经节细胞的死亡,因而AAV介导的基因治疗在急性损伤后的改善效果有限,这限制了其临床应用。实验也只使用了一种视神经损伤模型,Rheb基因治疗在其他模型中的有效性还有待进一步研究。
原文链接:https://doi.org/10.4103/1673-5374.371372
参考文献
[1] Nie D, Di Nardo A, Han JM, et al. Tsc2-Rheb signaling regulates EphA-mediated axon guidance. Nat Neurosci. 2010;13(2):163-172.
[2] Shu Q, Xu Y, Zhuang H, et al. Ras homolog enriched in the brain is linked to retinal ganglion cell apoptosis after light injury in rats. J Mol Neurosci. 2014;54(2):243-251.
[3] Nam JH, Leem E, Jeon MT, et al. Induction of GDNF and BDNF by hRheb(S16H) transduction of SNpc neurons: neuroprotective mechanisms of hRheb(S16H) in a model of Parkinson's disease. Mol Neurobiol. 2015;51(2):487-499.
[4] Jeong KH, Nam JH, Jin BK, et al. Activation of CNTF/CNTFRα signaling pathway by hRheb(S16H) transduction of dopaminergic neurons in vivo. PLoS One. 2015;10(3):e0121803.
[5] Kim SR, Kareva T, Yarygina O, et al. AAV transduction of dopamine neurons with constitutively active Rheb protects from neurodegeneration and mediates axon regrowth. Mol Ther. 2012;20(2):275-286.
[6] Kim SR, Chen X, Oo TF, et al. Dopaminergic pathway reconstruction by Akt/Rheb-induced axon regeneration. Ann Neurol. 2011;70(1):110-120.
[7] Wu D, Klaw MC, Connors T, et al. Expressing constitutively active rheb in adult neurons after a complete spinal cord injury enhances axonal regeneration beyond a chondroitinase-treated glial scar. J Neurosci. 2015;35(31):11068-11080.
[8] Park KK, Liu K, Hu Y, et al. Promoting axon regeneration in the adult CNS by modulation of the PTEN/mTOR pathway. Science. 2008;322(5903):963-966.
[9] Duan X, Qiao M, Bei F, et al. Subtype-specific regeneration of retinal ganglion cells following axotomy: effects of osteopontin and mTOR signaling. Neuron. 2015;85(6):1244-1256.
[10] Daniel S, Clark AF, Mcdowell CM. Subtype-specific response of retinal ganglion cells to optic nerve crush. Cell Death Discov. 2018;4:7.
[11] Na EJ, Nam HY, Park J, et al. PI3K-mTOR-S6K signaling mediates neuronal viability via collapsin response mediator protein-2 expression. Front Mol Neurosci. 2017;10:288.
[12] Al-Ali H, Ding Y, Slepak T, et al. The mTOR Substrate S6 Kinase 1 (S6K1) Is a negative regulator of axon regeneration and a potential drug target for central nervous system injury. J Neurosci. 2017;37(30):7079-7095.
 #br#
#br#
中南大学湘雅二医院眼科江冰教授课题组全家福
第一作者:蒋继宽,男,湘雅医学院临床医学八年制在读,主要从事眼科学研究,博士生导师为江冰教授。
通讯作者:江冰,湘雅二医院眼科主任,教授,知名青光眼专家,中华医学会眼科学分会神经眼科学组委员,湖南省医学会眼科学专业委员会青光眼学组副组长
基金支持:国家自然科学基金项目(No. 82070967, 81770930)和湖南省自然科学基金项目(No. 2020jj4788)。
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#
 #br#
#br#