NRR:空军军医大学西京医院张西京团队报道了分子伴侣介导的自噬参与神经保护作用
撰文:贾琪,李谨,郭晓峰,李仪,吴优,彭宇亮,方宗平,张西京
分子伴侣介导的自噬(chaperone-mediated autophagy, CMA)是自噬的3种类型之一,其特征是选择性降解体内的蛋白质。CMA有助于维持能量平衡及细胞内稳态,同时也能为细胞生存提供营养和支持。包括神经元在内几乎所有细胞中都可以检测到CMA。由于神经元对环境变化极其敏感,因此维持神经元稳态对神经元的生长和存活至关重要。既往研究已证明,神经元损伤和细胞死亡通常伴随着CMA功能障碍。此外,CMA功能障碍与中枢神经系统疾病也密切相关。
中国空军军医大学西京医院张西京团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表的题为“Neuroprotective effects of chaperone-mediated autophagy in neurodegenerative diseases”的最新综述,回顾了CMA在神经退行性疾病、脑损伤、神经胶质瘤和自身免疫性疾病中的变化。此外还总结了CMA调节的最新研究进展,并讨论了CMA作为治疗靶点的潜力。蛋白质稳态在细胞的生长和发育中起着不可或缺的作用。泛素-蛋白酶体系统和自噬-溶酶体途径是细胞内两个主要的蛋白水解系统,通过降解受损、错误折叠和异常聚集的蛋白质来维持细胞稳定。自噬有三种形式:大自噬、微自噬和CMA。与其他两种类型的自噬相比,CMA可以通过识别具有特定基序的蛋白质而进行选择性降解[1]。基于这种选择性降解的特征,CMA可用于靶向特定蛋白质进行降解,在疾病治疗中具有巨大前景。
张西京等首先总结了CMA的作用机制、生理作用与调控方式。CMA可降解具有KFERQ样五肽基序的蛋白质,在哺乳动物蛋白质组中约30%的蛋白质含有这种基序[2]。携带KFERQ基序的蛋白质被70kDa的热休克同源伴侣蛋白(heat shock-cognate chaperones of 70 kDa, HSC70)识别,并相互结合形成底物-蛋白质-伴侣复合物[3]。随后,蛋白质通过溶酶体膜蛋白2A (lysosomal membrane protein 2A, LAMP2A)进入溶酶体中进行降解(图1)。
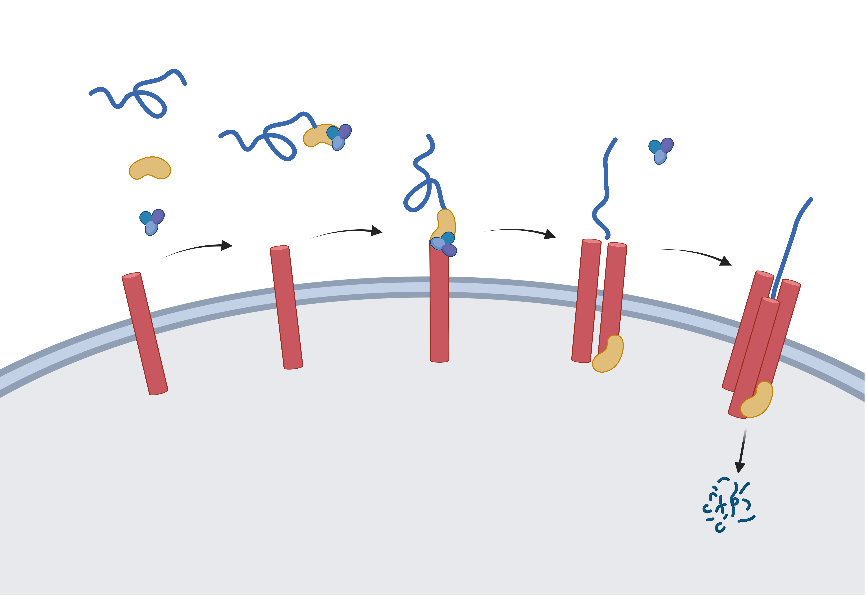
图1CMA的机制(图源:Jia et al., Neural Regen Res, 2024)
LAMP2A复合物的稳定性受到多种蛋白质的调节。胶质原纤维酸性蛋白和延伸因子1α是已知的具有调节作用的蛋白质[4]。胶质原纤维酸性蛋白有助于稳定LAMP2A复合物,但磷酸化胶质原纤维酸性蛋白与胶质原纤维酸性蛋白的结合导致稳定作用丧失。通常情况下,磷酸化胶质原纤维酸性蛋白和延伸因子1α与溶酶体膜结合,而当GTP浓度升高时,延伸因子1α从膜上释放出来,胶质原纤维酸性蛋白和磷酸化胶质原纤维酸性蛋白结合成二聚体,降低了复合物的稳定性最终导致复合物解离。因此,GTP浓度的增加可能影响了复合物的稳定性,随后抑制了CMA的活性[5](图2)。
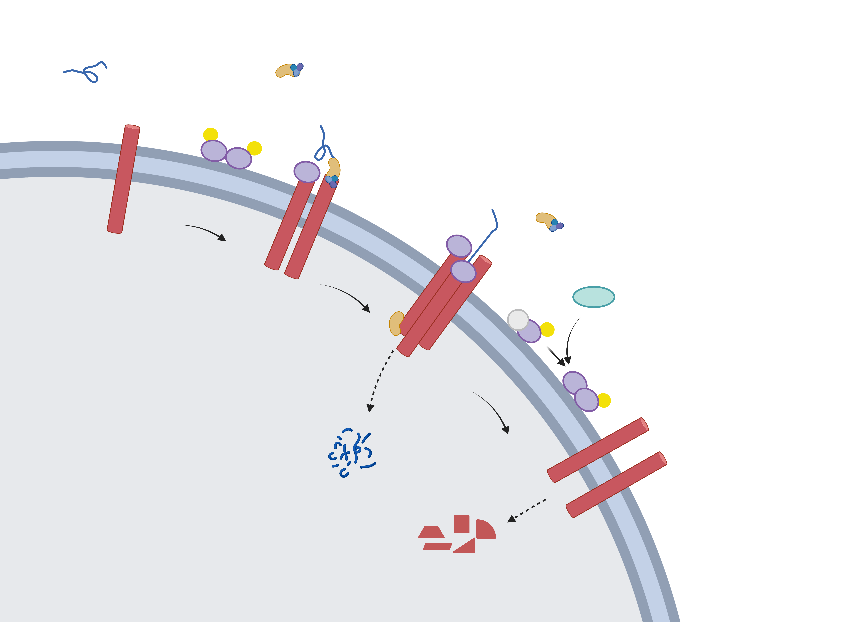
图2胶质原纤维酸性蛋白对CMA的调节过程(图源:Jia et al., Neural Regen Res, 2024)
接下来,张西京等总结了CMA在不同疾病中调节的最新研究进展,包括神经退行性疾病、脑损伤、脊髓损伤、胶质瘤与自身免疫性疾病。近年来,一些研究致力于阐明自噬与神经退行性疾病发病机制之间的关系。通过上调CMA,可以逆转异常聚集的蛋白质导致的神经毒性[6]。既往研究也证明CMA对创伤性脑损伤和脊髓损伤也具有一定的保护作用[7, 8](图3)。
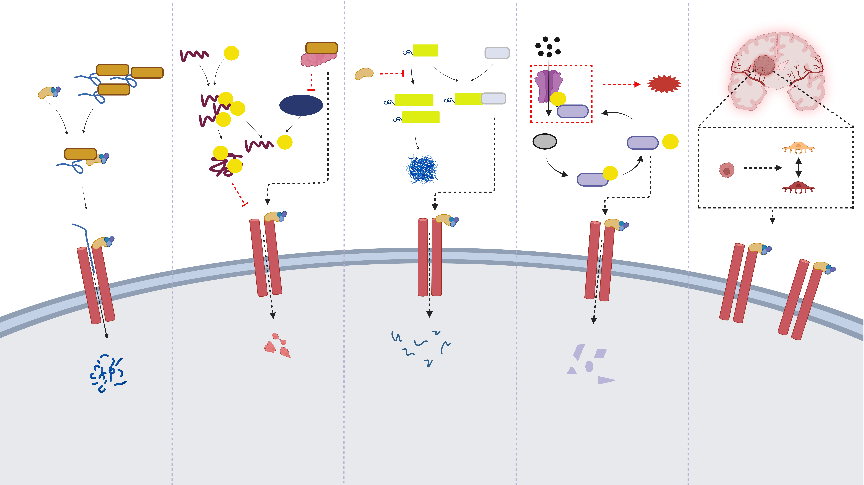
图3不同疾病中CMA的变化及作用机制(图源:Jia et al., Neural Regen Res, 2024)
张西京等重点概述了CMA在各种疾病中的相关机制和调节的研究进展。这些发现加强了对CMA在神经保护作用的理解,并为疾病治疗提供了新的靶点。作者认为,在未来的研究中应该阐明以下几点:首先,阐明CMA在不同疾病中改善神经损伤的机制以及靶向调节CMA活性的方式,对于避免神经退行性变和实现神经保护尤为重要。其次,需要更多的证据来证明CMA的调节对神经胶质瘤和周围神经损伤疾病具有神经保护作用。最后,明确能否在神经退行性疾病的早期阶段应用药物改善CMA活性,对疾病起到预防作用。阐明CMA在相关疾病中的机制,寻找靶向CMA底物蛋白的技术,开发增强CMA活性的药物,将是神经保护研究的重大进展,为未来的临床治疗提供新的途径。
原文链接:https://doi.org/10.4103/1673-5374.385848
参考文献
[1] Kaushik S, Cuervo AM. Chaperone-mediated autophagy: a unique way to enter the lysosome world. Trends Cell Biol. 2012;22(8):407-417.
[2] Kaushik S, Cuervo AM. The coming of age of chaperone-mediated autophagy. Nat Rev Mol Cell Biol. 2018;19(6):365-381.
[3] Ferreira JV, Da Rosa Soares A, Ramalho J, et al. LAMP2A regulates the loading of proteins into exosomes. Sci Adv. 2022;8(12):eabm1140.
[4] Bandyopadhyay U, Sridhar S, Kaushik S, et al. Identification of regulators of chaperone-mediated autophagy. Mol Cell. 2010;39(4):535-547.
[5] Endicott SJ, Ziemba ZJ, Beckmann LJ, et al. Inhibition of class I PI3K enhances chaperone-mediated autophagy. J Cell Biol. 2020;219(12):e202001031.
[6] Kuo SH, Tasset I, Cuervo AM, et al. Misfolded GBA/β-glucocerebrosidase impairs ER-quality control by chaperone-mediated autophagy in Parkinson disease. Autophagy. 2022;18(12):3050-3052.
[7] Zhang T, Liu C, Li W, et al. Targeted protein degradation in mammalian cells: a promising avenue toward future. Comput Struct Biotechnol J. 2022;20:5477-5489.
[8] Handa K, Kanno H, Matsuda M, et al. Chaperone-mediated autophagy after spinal cord injury. J Neurotrauma. 2020;37(15):1687-1695.

空军军医大学西京医院张西京团队
贾琪、李谨和郭晓峰为论文共同第一作者,张西京教授和方宗平教授为论文通讯作者。



