NRR:中国南京医科大学王彤和刘文涛课题组提出可采用重复经脊磁刺激治疗神经病理性疼痛#br#
#br#
神经病理性疼痛(neuropathic pain)是临床最为难治的慢性疼痛疾病,影响了全球约10%的成年人,是21世纪全球的主要健康问题之一[1]。神经病理性疼痛严重影响患者的日常生活,至今仍缺乏无创且副作用小的临床特效治疗手段。生物电磁刺激已在临床用于治疗神经病理性疼痛,其中植入式脊髓电刺激治疗顽固性躯干和四肢神经病理性疼痛的有效率可达80%,但是价格昂贵、有创、副作用多和机制不明限制它的临床应用[2]。因此,探寻神经病理性疼痛无创脊髓生物电磁刺激治疗方式并阐明其作用机制具有重要临床意义。#br#
脊髓神经炎症持续存在是神经病理性疼痛迁延难愈的核心病理生理机制,抑制脊髓神经炎症可有效缓解神经病理性疼痛[3, 4]。而如何无创抑制脊髓神经炎症是目前面临的一个科学难题。生物电磁刺激可以抑制炎症[5],是治疗神经病理性疼痛的重要手段。但以往对神经病理性疼痛的无创生物电磁刺激主要关注高级中枢(如重复经颅磁刺激)和周围神经(如经皮神经电刺激),忽视了感觉由外周向中枢传递的中继站—脊髓[6]。重复经脊磁刺激(repetitive trans-spinal magnetic stimulation)是一种利用高强度时变的脉冲磁场作用于脊髓,通过在脊髓内产生的感应电流,从而影响脊髓代谢和神经电生理活动的一种磁刺激技术。重复经脊磁刺激在脊髓损伤动物模型治疗中表现出强大的脊髓组织抗炎功能,受到越来越多研究者的关注[7, 8]。然而,应用重复经脊磁刺激治疗神经病理性疼痛的研究很少,应用重复经脊磁刺激治疗神经病理性疼痛的效果及机制是否与神经炎症调节有待进一步的探究。#br#
中国南京医科大学的王彤和刘文涛团队在《中国神经再生研究(英文)》》上发表了题为“Trans-spinal magnetic stimulation upregulates microglial SOCS3 to attenuate neuroinflammation in chronic constriction injury–induced neuropathic pain”的研究。文章发现,非侵入性靶向脊髓的重复经脊磁刺激可有效缓解慢性坐骨神经结扎诱导的神经病理性疼痛大鼠机械性痛觉超敏并缓解脊髓神经炎症。进一步研究发现,重复经脊磁刺激通过上调脊髓小胶质细胞中SOCS3水平,随后抑制受控皮质冲击损伤模型诱导的p38和STAT3磷酸化以及核因子κB p65核转位,从而抑制神经炎症。而重复经脊磁刺激对SOCS3上调可能是通过小胶质细胞中CaMKKβ/AMPK信号通路的激活实现。提示局部重复经脊磁刺激可通过激活脊髓小胶质细胞CaMKKβ/AMPK/SOCS3信号通路抑制脊髓神经炎症并缓解神经病理性疼痛,提供了在临床前受控皮质冲击损伤模型大鼠模型中重复经脊磁刺激治疗效果的证据,并提出了将其转化为临床应用的可能性。#br#
#br#
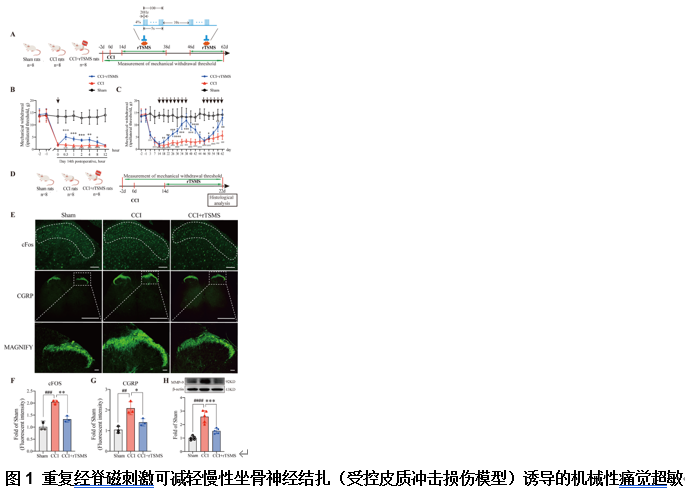
王彤和刘文涛等推测重复经脊磁刺激可能是一种具有前景的慢性疼痛镇痛策略。首先探究了重复经脊磁刺激用于神经病理性疼痛的治疗效果。对受控皮质冲击损伤模型造模14d后的神经病理性疼痛大鼠行腰骶部重复经脊磁刺激(20 Hz,0.14 T,4000脉冲),发现单次重复经脊磁刺激可显著减轻受控皮质冲击损伤模型诱导的机械痛敏,且行多次连续治疗(每天2次,每周5d)治疗效果可累积,24d后受控皮质冲击损伤模型+重复经脊磁刺激组大鼠的机械缩足阈值(mechanical withdrawal threshold)显著增加至接近于假手术组。停止干预后机械缩足阈值回退,但再行干预时,受控皮质冲击损伤模型+重复经脊磁刺激组机械缩足阈值升高到假手术组水平用时缩短至16d(图1)。c-FOS(神经元兴奋性的特异性标志物)、降钙素基因相关肽和基质金属蛋白酶9在神经病理性疼痛的中枢敏化中具有公认的作用[9, 10],实验发现受控皮质冲击损伤模型显著升高了脊髓中c-FOS、降钙素基因相关肽和基质金属蛋白酶9的水平,与大鼠神经病理性疼痛相关行为学的发生模式一致,而连续8d的重复经脊磁刺激可明显抑制脊髓中的这些生物标志物。这些行为学和分子生物学数据表明,局部重复经脊磁刺激能有效缓解受控皮质冲击损伤模型诱导的机械痛敏感性(图1)。
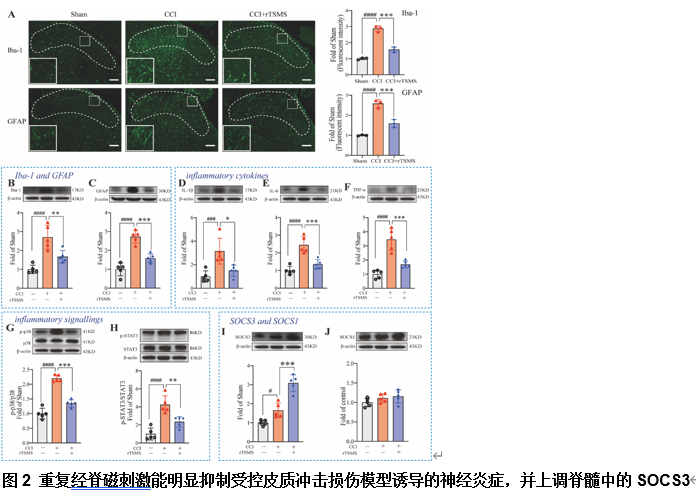
主要由神经胶质细胞活化(尤其是小胶质细胞活化)引起的神经炎症在维持神经病理性疼痛的中枢敏化中起关键作用。因此,王彤和刘文涛等进行了免疫荧光和蛋白印迹分析,以探讨重复经脊磁刺激对受控皮质冲击损伤诱导的神经炎症的影响。结果显示,受控皮质冲击损伤大鼠脊髓中离子钙结合适配分子1(Iba-1)和胶质纤维酸性蛋白的水平明显升高,表明脊髓中的小胶质细胞和星形胶质细胞被激活,而重复经脊磁刺激则可逆转这种激活(图2)。蛋白印迹分析显示,重复经脊磁刺激显著抑制了受控皮质冲击损伤诱导的促炎细胞因子白细胞介素1β、白细胞介素6和肿瘤坏死因子α的上调(图2)。越来越多的证据表明,p38丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)和信号转导及激活转录因子3(signal transducer and activator of transcription 3,STAT3)通路通过诱导神经炎症而导致神经损伤后的痛敏[5, 11],这也与此次实验的结果相符,即受控皮质冲击损伤可激活p38 AMPK和STAT3,而重复经脊磁刺激则抑制了它们。研究进一步探究了不同疾病中细胞因子信号转导因子的内源性负调控因子细胞因子信号转导抑制因子,结果发现重复经脊磁刺激能显著提高脊髓中SOCS3的蛋白水平,但不能提高SOCS1的蛋白水平。因此推测重复经脊磁刺激在脊髓中的抗神经炎症作用可能取决于SOCS3。
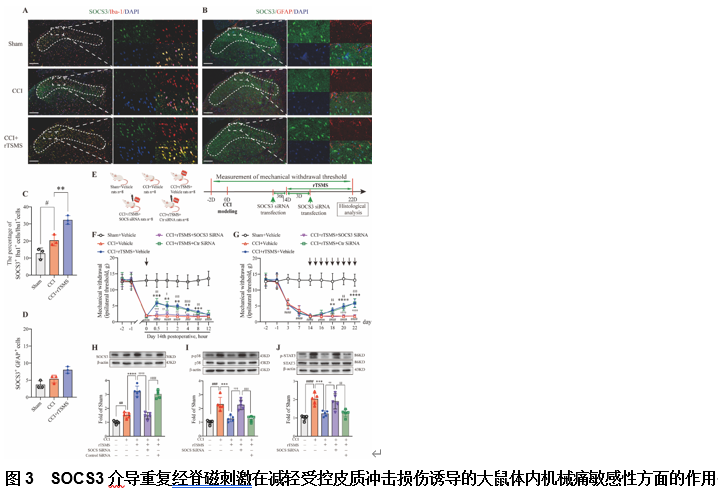
王彤和刘文涛等还对脊髓进行了共聚焦显微镜扫描,以分析重复经脊磁刺激治疗后SOCS3的表达情况。结果表明,经重复经脊磁刺激处理后,脊髓I-III层SOCS3与Iba-1的共定位显著增加,但SOCS3与胶质纤维酸性蛋白的共定位则没有显著变化。此外,SOCS3还与脊髓背角的神经元共标记。因而研究质疑SOCS3是否是重复经脊磁刺激介导的受控皮质冲击损伤引起的机械痛敏感性减弱所必需的,以及脊髓中SOCS3敲除是否能逆转重复经脊磁刺激的镇痛效应。结果发现,鞘内注射SOCS3小干扰RNA能显著逆转局部重复经脊磁刺激诱导的脊髓中SOCS3的上调,并减弱重复经脊磁刺激对机械痛敏的缓解作用。此外,在敲除SOCS3后,重复经脊磁刺激无法抑制p38和STAT3的磷酸化,这进一步表明重复经脊磁刺激在脊髓中的抗神经炎症作用可能取决于SOCS3(图3)。
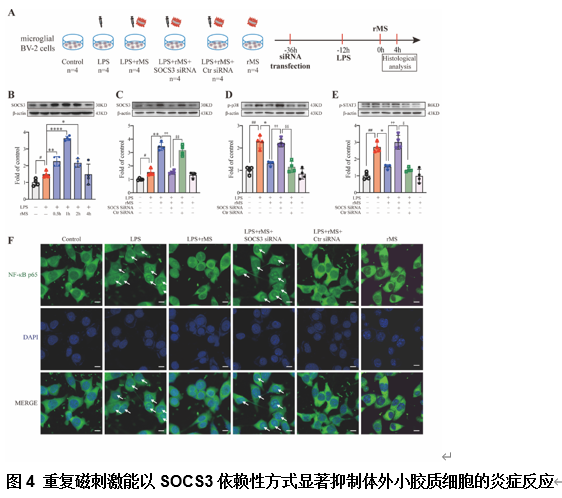
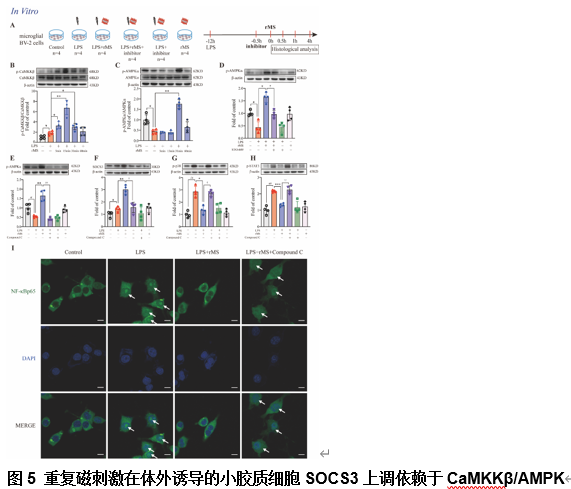
接下来,王彤和刘文涛等利用永生的小鼠小胶质细胞BV-2细胞系来揭示重复经脊磁刺激与脊髓神经炎症之间的潜在关系。在单次重复磁刺激(repetitive magnetic stimulation,10 Hz,0.035 T,1200脉冲)之前,先用脂多糖预处理BV2细胞12h。结果发现,与脂多糖组相比,单次重复磁刺激后,BV2细胞中SOCS3蛋白水平先升高后下降,而SOCS1蛋白表达则无明显增加。然后利用SOCS3小干扰RNA下调小胶质细胞系中的SOCS3,以研究重复磁刺激的抗炎作用是否依赖于小胶质细胞中的SOCS3。蛋白印迹结果表明,SOCS3小干扰RNA能减弱重复磁刺激对SOCS3上调的影响。此外,SOCS3敲除还能消减重复磁刺激抑制的p38和STAT3磷酸化。既往研究表明,小胶质细胞中p38/核因子κB信号的激活会导致神经炎症的爆发[12]。实验发现,脂多糖增加了p38的磷酸化,并导致核因子κB p65从细胞质转位到细胞核。在脂多糖预处理的BV-2细胞中,重复磁刺激显著抑制了p38的磷酸化,并抑制了核因子κB p65的核转位,而SOCS3小干扰RNA则逆转了这些效应。总之,这些数据表明,重复磁刺激可通过诱导小胶质细胞SOCS3的上调来抑制p38和STAT3的磷酸化以及核因子κB p65的核转位,从而缓解神经炎症(图4)。
单磷酸腺苷激活蛋白激酶(AMPK)是一种关键的细胞能量传感器和能量平衡调节器,据报道其激活可缓解不同类型的疼痛[13-15]。于是推测,磁刺激在受控皮质冲击损伤模型中的生物效应可能是由AMPK激活诱导的。体外实验发现,重复磁刺激可激活BV-2细胞中的钙调蛋白激酶激酶β(CaMKKβ)。此外,p-AMPKα在重复磁刺激后显著增加,而用CaMKKβ抑制剂STO-609预处理可消除重复磁刺激对AMPK的激活。因此,重复磁刺激可激活小胶质细胞中的AMPK。既往研究表明,AMPK激活会诱导microRNA-30a-5p抑制,从而直接靶向SOCS3[16]。此次实验也发现,在重复磁刺激前给予AMPK抑制剂可抑制重复磁刺激诱导的AMPK激活、SOCS3上调以及p38和STAT3磷酸化。此外,进一步体内实验评估了在受控皮质冲击损伤模型中重复经脊磁刺激的SOCS3镇痛效应是否依赖于AMPK激活(图5)。实验发现,受控皮质冲击损伤模型后脊髓中的p-AMPKα/AMPKα比值下降,而病灶重复经脊磁刺激在受控皮质冲击损伤模型处理大鼠的脊髓中表现出更强的AMPK激活效应。同时,在重复经脊磁刺激前鞘内注射AMPK抑制剂Compound C可抑制重复经脊磁刺激缓解的受控皮质冲击损伤模型中的机械痛。这些结果表明,局部重复经脊磁刺激对机械痛觉的缓解依赖于AMPK的激活。此外,在重复经脊磁刺激前鞘内注射Compound C可消除重复经脊磁刺激诱导的AMPK激活、小胶质细胞SOCS3上调以及p38和STAT3磷酸化(图6),这也与体外结果一致。这些体外和体内研究结果共同支持了实验假设,即重复经脊磁刺激诱导的SOCS3依赖性神经炎症抑制和受控皮质冲击损伤大鼠机械痛的缓解是通过激活CaMKKβ/AMPK通路实现的。
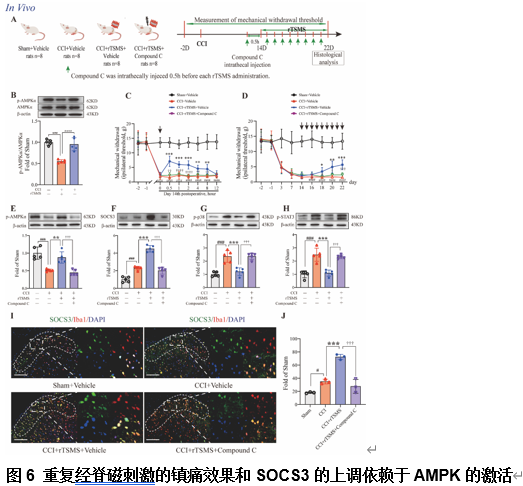
综上所述,重复经脊磁刺激是缓解受控皮质冲击损伤诱导的大鼠机械痛敏的一种有效的非侵入性治疗方法。它通过上调小胶质细胞SOCS3来抑制大鼠脊髓中p38/核因子κB和STAT3依赖性神经炎症,从而缓解受控皮质冲击损伤模型诱导的机械痛敏。且重复经脊磁刺激通过激活CaMKKβ/AMPK信号传导增加SOCS3。该研究创新性地证明了非侵入性重复经脊磁刺激可激活小胶质细胞CaMKKβ/AMPK/SOCS3以抑制神经炎症,从而治疗神经病理性疼痛。研究还发现,重复经脊磁刺激对神经病理性疼痛的治疗效果取决于细胞能量传感器AMPK的激活。这项研究提供了在临床前啮齿类动物模型中证实了重复经脊磁刺激对神经病理性疼痛的治疗效果,并提出了将其转化为临床应用的可能性。#br#
研究也存在一定的局限性。首先尽管体外实验显示重复磁刺激激活CaMKKβ,但研究者并未对其潜在机制进行进一步的研究。此外,研究使用SOCS3小干扰RNA下调SOCS3的表达,而没有对小胶质细SOCS3进行特异性敲除/敲低,因此不能断言重复经脊磁刺激对小胶质细胞有特异性作用,且未能排除重复经脊磁刺激也可能通过神经元上表达的SOCS3对受控皮质冲击损伤诱导的机械痛觉产生有益影响。
#br#
原文链接:https://doi.org/10.4103/NRR.NRR-D-24-00912
#br#
参考文献#br#
[1] Bouhassira D. Neuropathic pain: Definition, assessment and epidemiology. Rev Neurol (Paris). 2019;175(1-2):16-25.#br#
[2] Sommer C, Leinders M, Üçeyler N. Inflammation in the pathophysiology of neuropathic pain. Pain. 2018;159(3):595-602.#br#
[3] Guan Z, Kuhn JA, Wang X, et al. Injured sensory neuron-derived CSF1 induces microglial proliferation and DAP12-dependent pain. Nat Neurosci. 2016;19(1):94-101.#br#
[4] Baker BJ, Akhtar LN, Benveniste EN. SOCS1 and SOCS3 in the control of CNS immunity. Trends Immunol. 2009;30(8):392-400.#br#
[5] Qian C, Fan Y, Zong L, et al. Opening K(ATP) channels induces inflammatory tolerance and prevents chronic pain. Brain Behav Immun. 2023;107:76-86.#br#
[6] Hu Z, Deng N, Liu K, et al. CNTF-STAT3-IL-6 axis mediates neuroinflammatory cascade across Schwann cell-neuron-microglia. Cell Rep. 2020;31(7):107657.#br#
[7] Yu C, Li P, Wang YX, et al. Sanguinarine attenuates neuropathic pain by inhibiting P38 MAPK activated neuroinflammation in rat model. Drug Des Devel Ther. 2020;14:4725-4733.#br#
[8] Sun M, Sun Y, Ma J, et al. YY1 promotes SOCS3 expression to inhibit STAT3‑mediated neuroinflammation and neuropathic pain. Mol Med Rep. 2021;23(2):103.#br#
[9] Pan C, Wang C, Zhang L, et al. Procyanidins attenuate neuropathic pain by suppressing matrix metalloproteinase-9/2. J Neuroinflammation. 2018;15(1):187.#br#
[10] He W, Long T, Pan Q, et al. Microglial NLRP3 inflammasome activation mediates IL-1β release and contributes to central sensitization in a recurrent nitroglycerin-induced migraine model. J Neuroinflammation. 2019;16(1):78.#br#
[11] Liu Y, Feng L, Ren S, et al. Inhibition of lncRNA DILC attenuates neuropathic pain via the SOCS3/JAK2/STAT3 pathway. Biosci Rep. 2020;40(6):BSR20194486.#br#
[12] Wang X, Sun X, Niu M, et al. RAGE silencing ameliorates neuroinflammation by inhibition of p38-NF-κB signaling pathway in mouse model of Parkinson's disease. Front Neurosci. 2020;14:353.#br#
[13] Asiedu MN, Dussor G, Price TJ. Targeting AMPK for the Alleviation of Pathological Pain. Exp Suppl. 2016;107:257-285.#br#
[14] Xiang HC, Lin LX, Hu XF, et al. AMPK activation attenuates inflammatory pain through inhibiting NF-κB activation and IL-1β expression. J Neuroinflammation. 2019;16(1):34.#br#
[15] Zheng T, Wang Q, Bian F, et al. Salidroside alleviates diabetic neuropathic pain through regulation of the AMPK-NLRP3 inflammasome axis. Toxicol Appl Pharmacol. 2021;416:115468.#br#
[16] Wan L, Jia RM, Ji LL, et al. AMPK-autophagy-mediated inhibition of microRNA-30a-5p alleviates morphine tolerance via SOCS3-dependent neuroinflammation suppression. J Neuroinflammation. 2022;19(1):25.#br#
#br#
#br#
#br#
#br#
#br#





