NRR:首都医科大学附属北京朝阳医院海涌团队报道牵张性脊髓损伤动物模型的神经生理学、组织学以及行为学特征
撰文:韩渤、梁伟时、孙端、丁红涛、杨逸寒、海涌、尹鹏
脊髓损伤往往由于脊髓挫伤、脱位以及牵张所引起,常伴随高致残率,严重影响患者的生活质量[1, 2]。其中,脊髓受到一定程度的纵向牵张力后,可出现牵张性脊髓损伤。尽管手术技术和脊柱内固定技术已快速发展,但在脊柱畸形矫正过程中,牵张性脊髓损伤仍时有发生。严重脊柱畸形患者中牵张性脊髓损伤的发生率约为0.8%[3]。脊髓损伤的病理生理过程包括由机械因素(牵张、损伤等)引发的原发性损伤以及相关的继发性损伤。其中,原发性损伤不可逆,且可在最初几小时内直接导致轴突损伤和血脊髓屏障的破坏[4]。继发性损伤包括脊髓缺血、细胞肿胀、自由基介导的炎症以及细胞凋亡,最早可发生于初始损伤后几分钟内[5]。不同类型的脊髓损伤在不同形式的机械力作用下,其组织病理学表现和损伤机制不同;然而不同类型脊髓损伤的相关特征仍缺乏深入而全面的总结。
最近,来自中国首都医科大学附属北京朝阳医院骨科海涌团队在《中国神经再生(英文版)》(Neural Regeneration Research)上发表了题为“Neurophysiological, histological, and behavioral characterization of animal models of distraction spinal cord injury: a systematic review”的文章。该综述对牵张性脊髓损伤动物模型的神经生理学、组织学以及行为学特征进行了系统回顾。其纳入了22篇相关研究,阐明了该特殊脊髓损伤类型动物模型的相关特征,论证了牵张过程中,牵张速率和时间对于脊髓组织损伤的影响。这一综述为牵张性脊髓损伤动物模型建立以及药物干预治疗提供了线索。
脊柱畸形矫正过程中无法彻底避免脊髓牵张,部分严重脊柱畸形患者在术后会出现牵张性脊髓损伤[3]。根据既往研究,脊髓损伤的病理生理过程包括由于机械因素引发的原发性损伤以及脊髓缺血、炎症等因素引发的继发性损伤[4, 5]。目前,很少有研究聚焦于牵张性脊髓损伤的相关特征。因此海涌等收集了牵张性脊髓损伤影响动物神经功能以及运动能力的证据,系统回顾了涉及牵张性脊髓损伤后动物模型的实验研究,总结了该类动物模型的神经生理,组织学以及行为学特征,进一步探明了有关于牵张性脊髓损伤的病理生理机制。
海涌等系统检索了927篇文献,最终纳入了22篇文献进行分析(图1),其中有17篇随机对照研究,5篇观察性研究。研究共纳入了537只牵张性脊髓损伤模型动物。结果评估分为4类:神经生理学、组织学、行为学评估,以及其他结果。评价方法分为组织学、组织形态学、X射线影像、荧光显微镜、行为测试和磁共振成像。
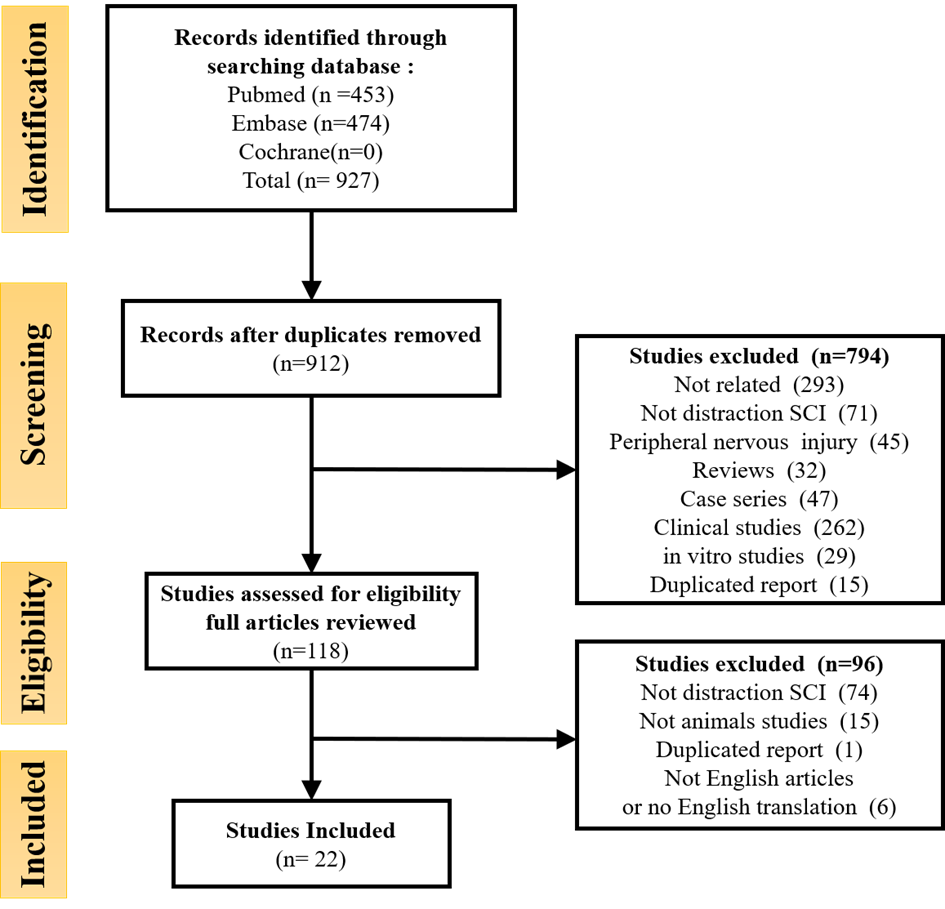
图1 PRISMA流程图(图源:Han et al., Neural Regen Res, 2024)
在纳入的研究中,大鼠是最常见的实验动物(60.1%)。实验中最常见的牵张性脊髓损伤造模部位是胸椎区(185例,34.4%),其次是颈椎区(98例,18.2%)、胸腰椎区(115例,21.4%%)、腰椎区(84例,15.5%)、颈胸区(50例,9.3%)和未知区(8例,1.4%)。对于实验动物而言,牵引器常被用于手术造模中。通常通过拉伸脊髓来模拟脊髓在损伤期间所经历的张力,从而实现牵张性脊髓损伤动物模型的构建。截骨伴连续性牵张的造模方法从各个方面更接近临床中牵张性脊髓损伤的发生。
海涌等以SYRCLE偏倚风险工具对纳入研究的偏倚风险进行评估,发现风险最高的是分配隐藏(选择偏倚)和盲法(表现偏倚),而不完整数据(消耗偏移)和选择性报告(报告偏差)则风险最小。
其中15项研究详细描述了神经生理学的评估方法,8项研究使用受控电生理参数作为分组标准,同时评估建模是否成功。此外7项研究记录了诱发电位来评估神经功能。有研究比较了脊髓诱发反应改变组和脊髓诱发反应消失组的脊髓血流量,发现牵张刺激在引起脊髓诱发反应丢失前就会发生严重的脊髓缺血[6]。Skinner等[7]认为牵张性刺激可引起同侧后肢运动诱发电位和经颅运动诱发电位在肌电图上的损失。有研究也报道了经颅运动诱发电位水平的恢复程度与脊髓牵张过程中截骨锥体的牵拉程度成负相关[8]。
纳入的研究采用了光镜或电镜、免疫组织化学、免疫印迹、免疫荧光和组织形态测量方法对于动物模型进行组织病理学评估。其中有20项纳入研究中进行了组织病理学评估。有研究报道了牵张性脊髓损伤后主要变化为脊髓组织的出血、水肿、神经细胞体和轴突变性[9]。2项研究对脊髓旁区Ranvier淋巴结进行了形态测量学分析,观察到牵张性脊髓损伤后8周,病变侧约4mm处牵张损伤可导致Ranvier淋巴结变长[10, 11]。有3篇研究利用苏木精-伊红和神经元核染色进行组织学评价,发现脊髓组织损失与脊髓牵张程度成正相关[12-14]。Shimizu等[15]发现利鲁唑预处理牵张性脊髓损伤动物后,其细胞核明显大于对照组,表明利鲁唑预处理可减少牵张性脊髓损伤急性期的腹侧运动神经元损伤。Wu等[16]利用墨水灌注和腐蚀铸造技术观察到,当脊髓束立即发生功能改变和结构损伤时,脊髓微血管只是部分充盈,并在扩大牵张下出现痉挛直至破裂出血。
在纳入的研究中,有多篇研究涉及对牵张性脊髓损伤动物模型行为学的评估,且采取了多种量表和评估方式证明了牵张性脊髓损伤动物模型运动能力受到影响。Seifert等[14]通过BBB运动评分量表的结果来作为分级损伤的特征。Maiman等[17]指出牵张性脊髓损伤动物模型的Tarlov评分下降并且伴随着神经功能的减退。Liu 等[18]研究表明,皮质躯体感觉诱发电位降低50%和70%组在Gale联合行为评分中存在显著差异。通过CatWalk系统和梯阶行走测试评估了牵张性脊髓损伤动物模型组和脊髓挫伤动物模型组的行走功能,发现在损伤后2周,牵张性脊髓损伤动物模型组的步列持续时间、对角线支撑、前肢强度、前肢工作周期和前爪角度受到的影响比脊髓挫伤组更明显[19, 20]。
在神经病理学,组织学以及行为学特征后,海涌等对纳入研究中还对于其他数据进行了分析。有2项研究监测到牵张性脊髓损伤动物模型脊髓损伤中心区氧分压显著下降[15, 21]:在牵张性脊髓损伤动物模型损伤中心的氧分压水平一直在波动,且在牵张15min后都没有恢复到基线水平。在牵张过程中,测量到牵拉张力峰值范围为24.1-43.9 N[10, 11]。此外,有研究指出牵张过程中应力是导致椎间盘和其他软组织损伤的主要原因[10]。有实验发现,当牵张距离为20.2±4.7 mm(占胸腰椎长度的3.6%)时,即可使实验猪发生牵张性脊髓损伤,且牵张距离与胸腰椎长度相关(R=0.632,P<0.01)[8]。在山羊模型中,安全的牵张距离为11.8±3.65 mm[22]。研究指出,在牵张性脊髓损伤巴马猪模型中,T2-磁共振成像显示,在损伤区域出现相对增强的损伤信号,这一现象的出现可能与脊髓损伤后损伤区域出现水肿、炎症、脱髓鞘、轴突增生以及星形胶质细胞增生相关[12]。
牵张性脊髓损伤被认为是由于血管损伤和直接牵张导致的脊髓缺血引起的。牵张距离和牵张速度是影响牵张性脊髓损伤原发性损伤的物理因素。在动物模型中,牵张距离为相邻椎节的10%被认为是安全的牵张距离。有实验研究了牵张距离对于牵张性脊髓损伤程度的影响,在实验动物L1-L3间进行牵张,牵张距离为该长度的0(对照组)、10%、20%和30%。结果表明,随着牵张距离的增加,脊髓表面的血容量逐渐减少,且神经根处的动脉变细直至破裂。这证明了牵张距离的增加可引起更严重的牵张性脊髓损伤。且有学者指出,牵张的极限安全距离与手术前后截骨段高度中对应的脊髓体积的差值密切相关。
多项研究对于不同程度的牵张性脊髓损伤进行了分组研究,结果表明行为运动上的受限和组织的缺损将随着牵张性脊髓损伤的加重而增强。事实上,除单独衡量各项研究的特征外,该研究还评估了行为与组织学参数间的关联以期探究牵张性脊髓损伤的发生机制。有多项研究显示,在牵张性脊髓损伤动物模型中,多项组织学参数与行为评分间存在显著相关性。有研究发现,具有相似后肢行为结果的损伤组与运动功能障碍组出现了相同的组织损伤。这有助于了解牵张性脊髓损伤结构与功能之间的关系。
由于牵张性脊髓损伤造模的特殊性和复杂性,很少有研究进一步研究牵张性脊髓损伤的继发损伤机制。海涌等[12, 13]进行了2项研究对于牵张性脊髓损伤亚急性期继发性损伤的潜在机制进行了论证和总结(图2)。
 #br#
#br#
图2牵张性脊髓损伤亚急性期小胶质细胞/巨噬细胞诱导的神经元炎症机制及潜在的凋亡机制(图源:Han et al., Neural Regen Res, 2024)
牵张性脊髓损伤刺激小胶质细胞/巨噬细胞后,经典炎症TLR4/NF-κB/MAPK通路被激活,发现相关蛋白表达水平也明显增加。TLR4/NF-κB/MAPK通路的激活过程与经典通路一致。IKK磷酸化的IκBα可将NF-κB复合物二聚体(包括p65/p50二聚体)转运到细胞核。P38 MAPK、JNK和ERK的激活以及进一步激活Caspase-1可促进促炎细胞因子的产生[13]。同时,脊髓组织中促凋亡的P53、Bax和Caspase-3蛋白表达增加,而抗凋亡的Bcl-2蛋白表达减少。神经元凋亡的这一过程可能涉及DNA损伤、线粒体功能障碍以及起始配体肿瘤坏死因子α和凋亡蛋白Caspase-8和Caspase-9的促进作用[12]。
海涌等通过归纳和梳理,明确了牵张性脊髓损伤动物模型的神经生理学特征、组织学特征以及行为学特征,认识到牵张性脊髓损伤原发性损伤和继发性损伤的相关机制,同时在原发性损伤中明确了牵张强度和时间的不同给脊髓损伤带来的影响。该文为牵张性脊髓损伤的造模以及相关基础研究提供新的思路,也为临床的诊断和治疗提供有力的支持。
但是此次综述总体上缺乏对牵张性脊髓损伤相关基因表达和调控的探究,且牵张性脊髓损伤在基因水平上的发生机制尚未得到完全验证。其次,纳入的动物模型物种不一,因此会影响对于脊髓组织水肿、缺血、细胞凋亡以及轴突变形相关组织学参数的对比与研究。此外,根据纳入研究的偏倚调查显示,大多数研究存在较高的偏倚风险,特别是在样本选择方面,应当在样本选择和盲法设置上选择更为合适的实验方法。
原文链接:https://doi.org/10.4103/1673-5374.380871
参考文献
[1] Anjum A, Yazid MD, Fauzi Daud M, et al. Spinal cord injury: pathophysiology, multimolecular interactions, and underlying recovery mechanisms. Int J Mol Sci. 2020;21(20):7533.
[2] Fouad K, Popovich PG, Kopp MA, et al. The neuroanatomical-functional paradox in spinal cord injury. Nat Rev Neurol. 2021;17(1):53-62.
[3] Schwartz DM, Auerbach JD, Dormans JP, et al. Neurophysiological detection of impending spinal cord injury during scoliosis surgery. J Bone Joint Surg Am. 2007;89(11):2440-2449.
[4] Ahuja CS, Nori S, Tetreault L, et al. Traumatic spinal cord injury-repair and regeneration. Neurosurgery. 2017;80(3s):S9-S22.
[5] Pinchi E, Frati A, Cantatore S, et al. Acute spinal cord injury: a systematic review investigating miRNA families involved. Int J Mol Sci. 2019;20(8):1841.
[6] Dolan EJ, Transfeldt EE, Tator CH, et al. The effect of spinal distraction on regional spinal cord blood flow in cats. J Neurosurg. 1980;53(6):756-764.
[7] Skinner SA, Transfeldt EE. Electromyography in the detection of mechanically induced spinal motor tract injury: observations in diverse porcine models. J Neurosurg Spine. 2009;11(3):369-374.
[8] Yang JH, Suh SW, Modi HN, et al. Effects of vertebral column distraction on transcranial electrical stimulation-motor evoked potential and histology of the spinal cord in a porcine model. J Bone Joint Surg Am. 2013;95:835-842, S1-2(9).
[9] Wu J, Xue J, Huang R, et al. A rabbit model of lumbar distraction spinal cord injury. Spine J. 2016;16(5):643-658.
[10] Chen K, Liu J, Assinck P, et al. Differential histopathological and behavioral outcomes eight weeks after rat spinal cord injury by contusion, dislocation, and distraction mechanisms. J Neurotrauma. 2016;33(18):1667-1684.
[11] Choo AM, Liu J, Liu Z, et al. Modeling spinal cord contusion, dislocation, and distraction: characterization of vertebral clamps, injury severities, and node of Ranvier deformations. J Neurosci Methods. 2009;181(1):6-17.
[12] Han B, Liang W, Hai Y, et al. Elucidating the potential mechanisms underlying distraction spinal cord injury-associated neuroinflammation and apoptosis. Front Cell Dev Biol. 2022;10:839313.
[13] Liang W, Han B, Hai Y, et al. The role of microglia/macrophages activation and TLR4/NF-κB/MAPK pathway in distraction spinal cord injury-induced inflammation. Front Cell Neurosci. 2022;16:926453.
[14] Seifert JL, Bell JE, Elmer BB, et al. Characterization of a novel bidirectional distraction spinal cord injury animal model. J Neurosci Methods. 2011;197(1):97-103.
[15] Shimizu EN, Seifert JL, Johnson KJ, et al. Prophylactic riluzole attenuates oxidative stress damage in spinal cord distraction. J Neurotrauma. 2018;35(12):1319-1328.
[16] Wu D, Zheng C, Wu J, et al. The pathologic mechanisms underlying lumbar distraction spinal cord injury in rabbits. Spine J. 2017;17(11):1665-1673.
[17] Maiman DJ, Myklebust JB, Ho KC, et al. Experimental spinal cord injury produced by axial tension. J Spinal Disord. 1989;2(1):6-13.
[18] Liu L, Chi LT, Tu ZQ, et al. Observation and establishment of an animal model of tractive spinal cord injury in rats. Chin J Traumatol. 2004;7(6):372-377.
[19] Guo Y, Hu H, Wang J, et al. Walking function after cervical contusion and distraction spinal cord injuries in rats. J Exp Neurosci. 2019;13:1179069519869615.
[20] Wang J, Zhang M, Guo Y, et al. Quantification of surviving neurons after contusion, dislocation, and distraction spinal cord injuries using automated methods. J Exp Neurosci. 2019;13:1179069519869617.
[21] Bell JES, Seifert JL, Shimizu EN, et al. Atraumatic spine distraction induces metabolic distress in spinal motor neurons. J Neurotrauma. 2017;34(12):2034-2044.
[22] Qiu F, Yang JC, Ma XY, et al. Influence of vertebral column distraction on spinal cord volume: an experimental study in a goat model. Arch Orthop Trauma Surg. 2015;135(9):1201-1210.
 #br#
#br#
通讯作者海涌(右)和第一作者韩渤(左)
 #br#
#br#
首都医科大学附属北京朝阳医院海涌团队

 #br#
#br#
 #br#
#br#
 #br#
#br#