NRR:遵义医科大学附属医院熊柳林团队提出人胎盘绒毛膜间充质干细胞移植有望治疗新生儿缺氧缺血性脑病
撰文:薛璐璐,孙奕飞,杜若兰,毕宁,肖秋霞,牛瑞泽,檀雅欣,陈丽,刘佳,王廷华,熊柳林
新生儿缺氧缺血性脑病是新生儿死亡和严重神经功能障碍的主要原因。出生时窒息的新生儿通常难以启动和维持呼吸,导致终身脑瘫、神经感觉缺陷和认知障碍[1]。氙气治疗、褪黑素、促红细胞生成素和低温等多种治疗方法对缺氧缺血损伤引起的神经功能障碍显示出一定的临床疗效,但许多幸存下来的婴儿表现出严重的长期并发症[2-4],如脑瘫。基于干细胞的治疗能够促进抗炎环境和减轻损伤后的炎症反应,且临床研究表明,静脉注射脐带干细胞和自体脐带血细胞可逆转新生儿缺氧缺血性脑病的神经功能障碍,减轻认知障碍,增强情绪反应和锥体外功能[5]。胎盘作为分娩后的废物,没有侵入性获取过程,与传统的骨髓间充质干细胞相比,具有更强的增殖能力[6]。具有来源充足、免疫原性低、病毒污染率低、无社会伦理争议等优点。研究表明,含有粒细胞-巨噬细胞集落刺激因子和白细胞介素3的细胞因子混合物可改善创伤性脑损伤和帕金森病,且白细胞介素3促进穹窿毛横断大鼠的神经元存活,并显著预防海马CA1区神经元死亡和缺血诱导的学习障碍[7]。然而,人胎盘绒毛膜来源的间充质干细胞及白细胞介素3在缺氧缺血诱导的长期并发症中的作用及其潜在机制知之甚少。
最近,中国遵义医科大学附属医院熊柳林团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“Transplantation of human placental chorionic plate-derived mesenchymal stem cells for repair of neurological damage in neonatal hypoxic-ischemic encephalopathy”的研究。他们发现,人胎盘绒毛膜来源的间充质干细胞移植可减轻缺氧缺血诱导的长期神经损伤。继而蛋白芯片分析发现,白细胞介素3在缺氧缺血损伤中发挥了重要的作用,而人胎盘绒毛膜来源的间充质干细胞治疗后可降低白细胞介素3表达。进一步通过构建干扰白细胞介素3片段和转基因敲除大鼠,发现抑制白细胞介素3可加重缺氧缺血导致的神经和行为损伤。作为该干细胞的临床前效应评价,其在大鼠体内的治疗效果将为将来更好地应用于临床缺氧缺血性脑病患儿提供一定的理论依据。
缺氧缺血引起的脑损伤经历2个阶段:急性脑损伤和长期神经功能障碍。一般来说,急性缺氧缺血损伤后会发生晚期神经退行性变,包括继发性细胞死亡、细胞毒性水肿、进行性线粒体衰竭、延迟性癫痫发作和脑瘫[8]。尽管缺氧缺血性脑病新生儿脑瘫的发生率有所下降,但在低温治疗后脑瘫的发生率仍有报道[9, 10]。熊柳林等采用缺氧缺血模型诱导7d龄新生SD大鼠急性脑梗死模型(图1)。
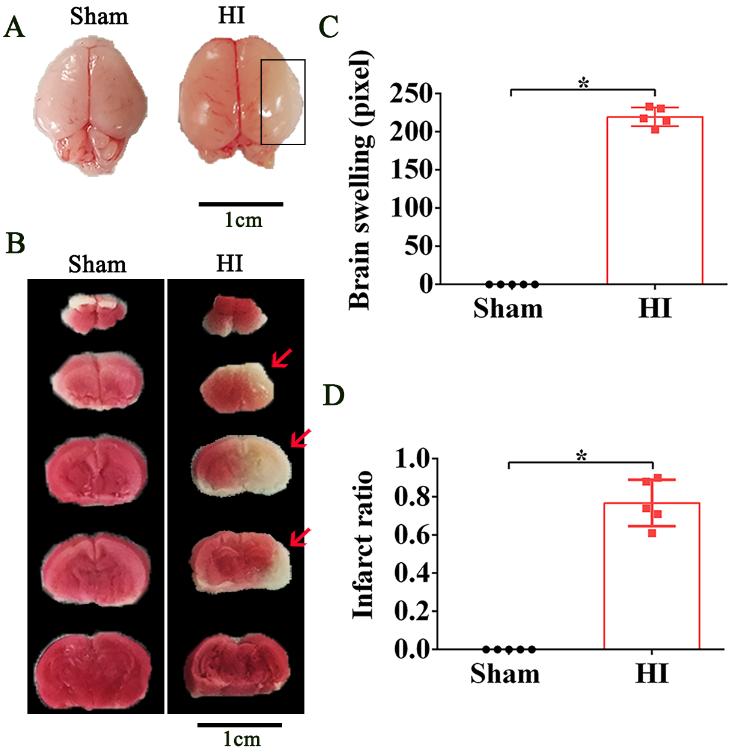
图1成功构建缺氧缺血模型(图源:Xue et al., Neural Regen Res, 2024)
另一项研究证实,人胎盘绒毛膜来源的间充质干细胞是干细胞的新来源,并向成骨和神经源性谱系分化[11]。熊柳林等体外培养了人胎盘绒毛膜来源的间充质干细胞,免疫荧光染色显示细胞表达CD44+CD90+CD45-,符合间充质干细胞的特征。此外,我们的数据显示,在缺氧缺血损伤后1和2个月接受人胎盘绒毛膜来源的间充质干细胞治疗的大鼠,缺氧缺血诱导的认知、运动和焦虑样行为障碍在很大程度上恢复(图2和3)。该研究首次发现人胎盘绒毛膜来源的间充质干细胞在缺氧缺血引起的长期行为障碍中的治疗作用。
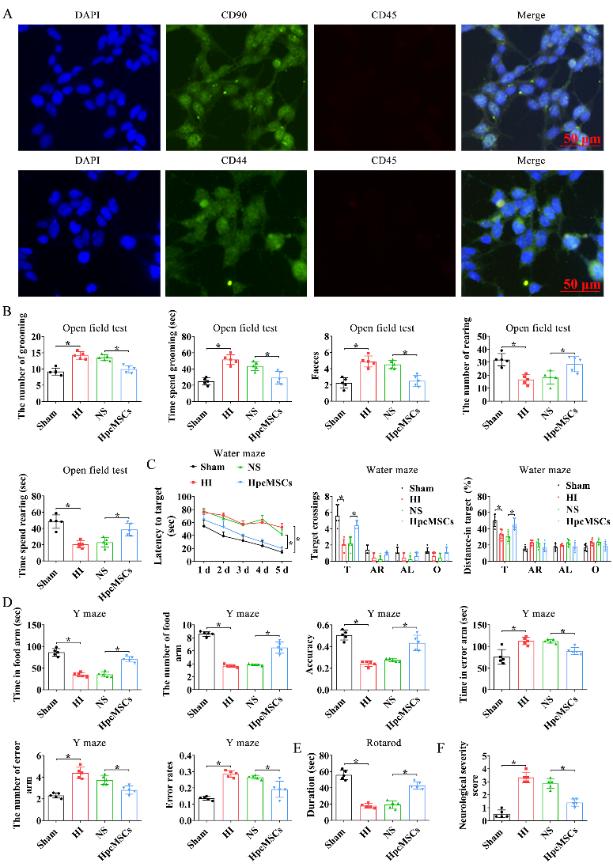
图2人胎盘绒毛膜来源的间充质干细胞移植后1个月对缺氧缺血大鼠的神经学评价(图源:Xue et al., Neural Regen Res, 2024)
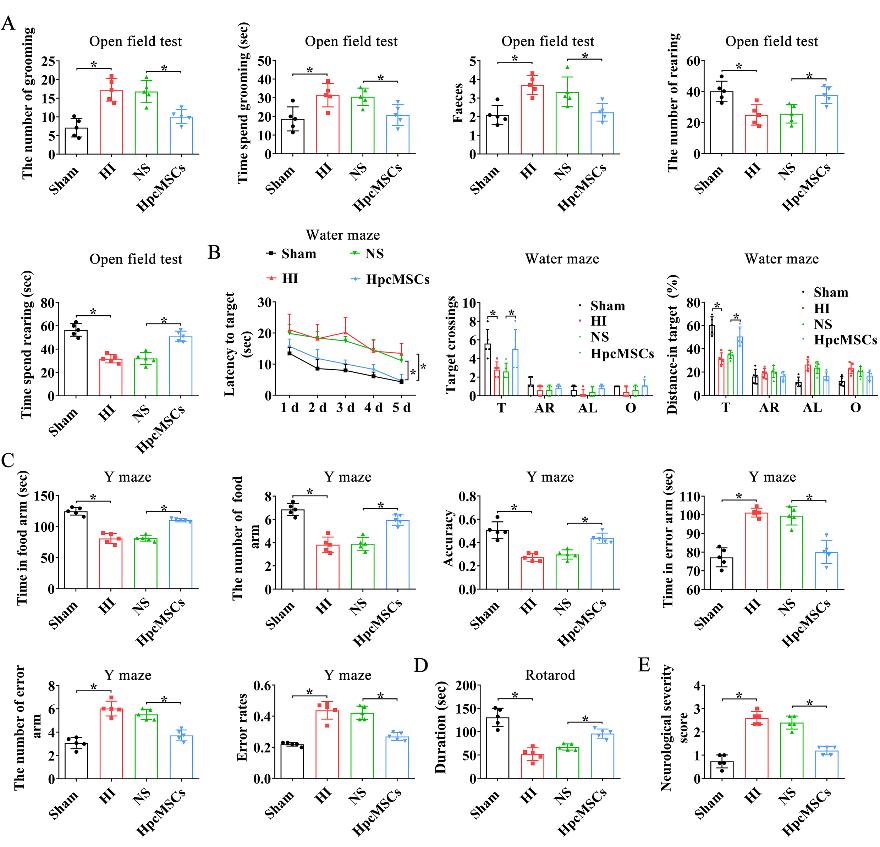
图3人胎盘绒毛膜来源的间充质干细胞移植后2个月对缺氧缺血大鼠的神经学评价(图源:Xue et al., Neural Regen Res, 2024)
为了进一步探讨人胎盘绒毛膜来源的间充质干细胞在缺氧缺血性脑病中的作用机制,对假手术组和缺氧缺血组右侧皮质和海马进行了蛋白芯片检测,结果显示白细胞介素3在缺氧缺血组中的相对表达量显著高于假手术组,提示白细胞介素3可能在缺氧缺血损伤中发挥重要作用,且人胎盘绒毛膜来源的间充质干细胞治疗后可明显降低白细胞介素3的表达(图4)。
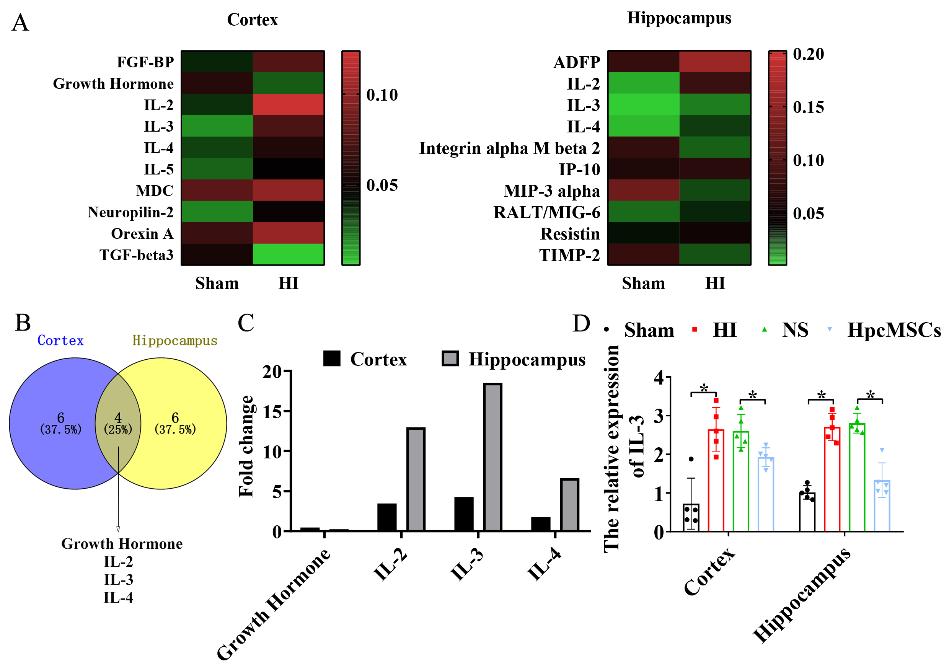
图4缺氧缺血损伤后脑中差异表达蛋白的筛选和人胎盘绒毛膜来源的间充质干细胞治疗后白细胞介素3的表达(图源:Xue et al., Neural Regen Res, 2024)
此前有报道称,通过反转录聚合酶链反应,白细胞介素3 mRNA在原代培养的海马神经元和混合胶质细胞中检测到[12]。然而,在过表达白细胞介素3转基因小鼠中,小胶质细胞被激活,并诱导白质病变[13]。因此,脑内白细胞介素3的高表达或低表达可能导致细胞功能异常。熊柳林等在缺氧缺血损伤大鼠的皮质和海马中检测到白细胞介素3的上调。与神经元和星形胶质细胞共定位的白细胞介素3阳性染色细胞存在于海马和大脑皮层,但数量较少(图5)。

图5两侧皮质和海马中白细胞介素3和NeuN或胶质纤维酸性蛋白的免疫荧光双标染色(图源:Xue et al., Neural Regen Res, 2024)
有证据支持神经系统和免疫系统之间存在重要的功能联系[14]。一项研究提出,淋巴组织可以促进交感神经突的生长,这种作用可能部分依赖于白细胞介素3的存在[15]。此次实验结果显示,抑制白细胞介素3可加重氧糖剥夺诱导的神经元损伤(图6)。相应地,白细胞介素3缺失对缺氧缺血大鼠行为功能恢复的负面影响,提示神经功能障碍可能是由免疫应答中的某些细胞因子介导的。在此次研究中白细胞介素3在缺氧缺血大鼠中升高,且在人胎盘绒毛膜来源的间充质干细胞治疗后轻度降低。白细胞介素3 敲低可加重缺氧缺血大鼠的行为功能障碍(图7)。这可能是因为缺氧缺血后白细胞介素3水平较高,而缺氧缺血大鼠在白细胞介素3敲低后表现出严重的神经行为障碍,而人胎盘绒毛膜来源的间充质干细胞治疗后白细胞介素3表达维持在中等水平,可更好地保护缺氧缺血大鼠的神经损伤。

图6下调白细胞介素3可抑制氧糖剥夺后SH-SY5Y细胞的活性和生长能力(图源:Xue et al., Neural Regen Res, 2024)
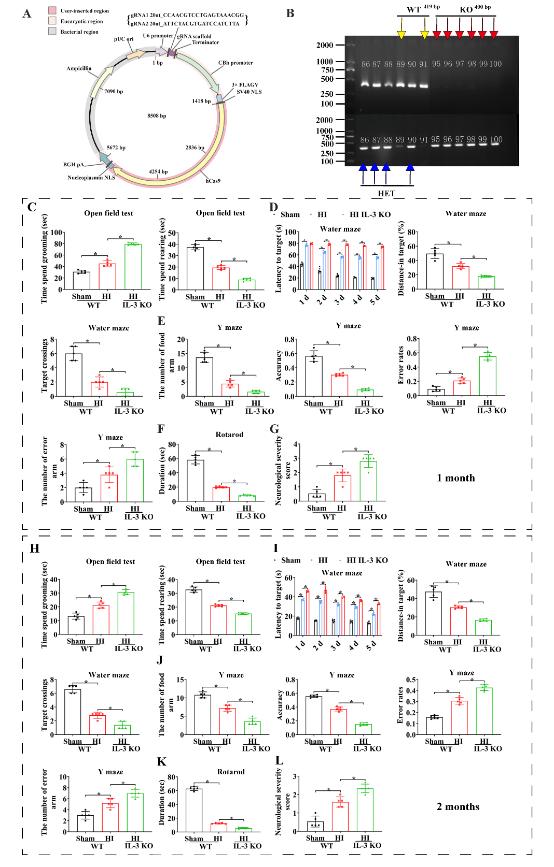
图7白细胞介素3 敲低对缺氧缺血大鼠行为功能的影响(图源:Xue et al., Neural Regen Res, 2024)
综上所述,鉴于人胎盘绒毛膜来源的间充质干细胞移植在缺氧缺血诱导的长期神经系统并发症中的作用,人胎盘绒毛膜来源的间充质干细胞为基础的治疗可能在临床上广泛应用于预防或治疗足月或早产新生儿缺氧缺血。人胎盘绒毛膜来源的间充质干细胞移植可能通过白细胞介素3介导神经元存活和神经行为功能改善 ,起到减轻缺氧缺血损伤的作用,作为该干细胞的临床前疗效评价,在大鼠身上的治疗效果将为今后在临床患者中的更好应用提供一定的理论依据。
然而,这些研究结果只是初步揭示了人胎盘绒毛膜来源的间充质干细胞可以显著改善缺氧缺血诱导的长期神经功能障碍,但人胎盘绒毛膜来源的间充质干细胞在脑内的存活、迁移和分化以及神经回路的形成还需要进一步的研究和分析。此外,白细胞介素3调控人胎盘绒毛膜来源的间充质干细胞的体内外功能实验也有待进一步探索。
原文链接:https://doi.org/10.4103/1673-5374.3909520
参考文献
[1] Huang J, U KP, Yang F, et al. Human pluripotent stem cell-derived ectomesenchymal stromal cells promote more robust functional recovery than umbilical cord-derived mesenchymal stromal cells after hypoxic-ischaemic brain damage. Theranostics. 2022;12(1):143-166.
[2] Sun M, An Z, Wei H, et al. Xenon attenuates hypoxic-ischemic brain damage by inhibiting autophagy in neonatal rats. Neuroreport. 2023;34(5):273-279.
[3] Weiss MD, Carloni S, Vanzolini T, et al. Human-rat integrated microRNAs profiling identified a new neonatal cerebral hypoxic-ischemic pathway melatonin-sensitive. J Pineal Res. 2022;73(2):e12818.
[4] Wu YW, Comstock BA, Gonzalez FF, et al. Trial of erythropoietin for hypoxic-ischemic encephalopathy in newborns. N Engl J Med. 2022;387(2):148-159.
[5] Cotten CM, Murtha AP, Goldberg RN, et al. Feasibility of autologous cord blood cells for infants with hypoxic-ischemic encephalopathy. J Pediatr. 2014;164:973-979.e1(5).
[6] Fukuchi Y, Nakajima H, Sugiyama D, et al. Human placenta-derived cells have mesenchymal stem/progenitor cell potential. Stem Cells. 2004;22(5):649-658.
[7] Edgar JM, Michaels YS, Zandstra PW. Multi-objective optimization reveals time- and dose-dependent inflammatory cytokine-mediated regulation of human stem cell derived T-cell development. NPJ Regen Med. 2022;7(1):11.
[8] Fang M, Liu J, Zhang Z, et al. Chloroquine protects hypoxia/ischemia-induced neonatal brain injury in rats by mitigating blood-brain barrier disruption. ACS Chem Neurosci. 2023;14(10):1764-1773.
[9] Zhou KQ, Dhillon SK, Bennet L, et al. Targeting persistent neuroinflammation after hypoxic-ischemic encephalopathy-is exendin-4 the answer? Int J Mol Sci. 2022;23(17):10191.
[10] Robertsson Grossmann K, Eriksson Westblad M, Blennow M, et al. Outcome at early school age and adolescence after hypothermia-treated hypoxic-ischaemic encephalopathy: an observational, population-based study. Arch Dis Child Fetal Neonatal Ed. 2023;108(3):295-301.
[11] Xie B, Gu P, Wang W, et al. Therapeutic effects of human umbilical cord mesenchymal stem cells transplantation on hypoxic ischemic encephalopathy. Am J Transl Res. 2016;8(7):3241-3250.
[12] Konishi Y, Kamegai M, Takahashi K, et al. Production of interleukin-3 by murine central nervous system neurons. Neurosci Lett. 1994;182(2):271-274.
[13] Feng L, Li C, Zeng LW, et al. MARCH3 negatively regulates IL-3-triggered inflammatory response by mediating K48-linked polyubiquitination and degradation of IL-3Rα. Signal Transduct Target Ther. 2022;7(1):21.
[14] Williams JM, Peterson RG, Shea PA, et al. Sympathetic innervation of murine thymus and spleen: evidence for a functional link between the nervous and immune systems. Brain Res Bull. 1981;6(1):83-94.
[15] Kannan-Hayashi Y, Okamura K, Hattori S, et al. Neuritogenic effects of T cell-derived IL-3 on mouse splenic sympathetic neurons in vivo. J Immunol. 2008;180(6):4227-4234.

左侧为第一作者薛璐璐,右侧为通讯作者熊柳林
通讯作者简介:熊柳林,四川大学华西医院麻醉学博士,澳大利亚南澳大学生物医学博士,昆明理工大学灵长类国家转化医学重点实验室博士后,教授,研究生导师。现任遵义医科大学附属医院Ibrain编辑部副主任,遵义医科大学未来科技菁英,贵州省优青。主要从事临床麻醉学/神经疾病损伤修复及干细胞干预治疗。主持国家自然科学基金2项,省部级等项目6项。在Experimental Molecular Medicine(IF:12.7)、Nature Communications(IF:17.694)等发表SCI论文30余篇;主编科学出版社等著作4部,副主编1部。作为主要完成人获省科学技术进步奖二等奖2项、省自然科学二等奖1项、中华医学科技奖、中国中西与结合学会心血管病专业委员会科学技术奖等各1项。获得1项发明专利,8项实用新型专利,3次受邀在国际大会上做特邀报告。任中国研究型医院学会神经再生与修复专业委员会青年委员,中国高校科技期刊研究会英文期刊专业委员会委员,《遵义医科大学学报》青年编委。
第一作者简介:薛璐璐,四川大学生物治疗国家重点实验室在读博士。以第一作者或共同第一作者发表 SCI 论文 12余 篇,作为参与作者发表SCI论文11篇。主持校级创新基金1项,参与省级和市级项目多项。获得云南省政府奖学金和“三好学生”称号(2019年)。作为副主编编写科学出版社专著1部,作为编委参编科学出版社等专著5部。参与发明专利1项。







