NRR:同济大学附属同济医院海舰团队构建了一种用于治疗脑缺血新型缓释血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜
神经血管单元由神经元、胶质细胞、血管细胞和细胞外基质组成[1]。神经元的结构和功能可由相邻的星形胶质细胞和脑微血管内皮细胞所调节[2, 3]。由于脑细胞和血管系统之间复杂的相互作用,脑缺血的病理生理和治疗理念已经从单纯的神经保护转变为对神经血管单元的保护[4]。纳米纤维材料能够负载治疗性蛋白,保持蛋白的构象结构和稳定性以及其生物活性。作为对脑缺血的反应,半暗带中的血管内皮生长因子A和碱性成纤维细胞生长因子增加,并通过增加血管体积、减少损伤体积以及增强神经细胞增殖和分化,而发挥神经保护作用[5]。然而,由于血管内皮生长因子A和碱性成纤维细胞生长因子的内源性升高水平和持续时间不足,其有益效果是有限和暂时的[6]。这个问题可通过外源性补充来解决,尤其是局部应用[7]。因此,构建负载血管内皮生长因子A和碱性成纤维细胞生长因子的纳米纤维膜双生长因子缓释递送系统,并探索其对神经血管单元的影响,这有望成为治疗脑缺血的新思路。#br#
最近,来自中国同济大学附属同济医院海舰团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“Sustained release of vascular endothelial growth factor A and basic fibroblast growth factor from nanofiber membranes reduces oxygen/glucose deprivation-induced injury to neurovascular units”的文章。该研究采用逐层自组装和静电纺丝技术制备了不同层数的负载血管内皮生长因子A和碱性成纤维细胞生长因子的纳米纤维膜。可见10层的缓释血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜具有理想的超微结构,能高效且稳定地释放生长因子超过1个月。同时发现,这种纳米纤维膜有助于促进脑微血管内皮细胞的成管和增殖能力,抑制神经元凋亡,上调紧密连接蛋白水平,并提高氧糖剥夺时神经血管单元各组分细胞的活性。这种纳米纤维膜还能降低氧糖剥夺后神经元中JAK2和STAT3的磷酸化和促凋亡蛋白(Bax/Bcl-2和cleaved caspase-3)的表达水平。这提示这种新型纳米纤维膜可通过抑制JAK2/STAT3通路对氧糖剥夺诱导的神经血管单元损伤发挥保护作用。
脑缺血时,氧气和葡萄糖的供应不足会损伤神经血管单元。大量研究表明,蛋白修饰的纳米纤维材料可影响神经血管单元的重塑。血管内皮生长因子A和碱性成纤维细胞生长因子可在脑缺血时调节血管生成、神经元存活和神经再生。海舰等将这2种生长因子负载到纳米纤维膜上,并分析其对氧糖剥夺神经血管单元的影响以及相关机制。
结果显示,利用静电逐层自组装技术将血管内皮生长因子A和碱性成纤维细胞生长因子沉积在聚己内酯纳米纤维表面,可成功构建具有明显三维结构的负载血管内皮生长因子A和碱性成纤维细胞生长因子的纳米纤维膜。扫描电镜显示,5和10层的血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜比15和20层的结构更清晰,直径更小(图1)。进一步酶联免疫吸附实验分析了不同负载层数的纳米纤维膜血管内皮生长因子A和碱性成纤维细胞生长因子的释放模式。可见血管内皮生长因子A和碱性成纤维细胞生长因子持续释放时间都超过30d。且其中,5层膜释放速度最快,最先达到平台期,其次是10层膜。由于高孔隙率能为细胞生长和黏附提供足够的空间,结合不同的缓释效率,实验最终选择了10层血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜进行后续实验。

图1血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜的表征(图源:Wu et al., Neural Regen Res, 2024)
对构建的神经血管单元中细胞与负载血管内皮生长因子A和(或)碱性成纤维细胞生长因子的纳米纤维膜共培养,而后以无葡萄糖培养基在37℃,95% N2,5% CO2条件下培养4h,构建氧糖剥夺损伤模型。成管实验、免疫荧光染色和MTT测试研究了血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜对氧糖剥夺后脑微血管内皮细胞的影响。如图2所示,这种纳米纤维膜改善了氧糖剥夺诱导的血管生成抑制,促进了脑微血管内皮细胞的增殖。

图2血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜可促进脑微血管内皮细胞的成管和增殖(图源:Wu et al., Neural Regen Res, 2024)
继续分析缓释血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜的神经保护作用,结果显示,其有助于神经元附着和生长,并改善氧糖剥夺诱导的原代海马神经元的凋亡(图3)。

图3血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜可促进神经元生长,并抑制氧糖剥夺诱导的细胞凋亡(图源:Wu et al., Neural Regen Res, 2024)
为研究血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜对体外神经血管单元的保护作用,对三维共培养系统中原代海马神经元、脑微血管内皮细胞和星形胶质细胞进行免疫荧光染色。发现这种纳米纤维膜可提高神经血管单元中各细胞组分的活性,避免氧糖剥夺造成的致命损伤(图4)。

图4 血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜可缓解氧糖剥夺诱导的神经血管单元细胞组分的损伤(图源:Wu et al., Neural Regen Res, 2024)
免疫荧光结果显示,血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜对于氧糖剥夺诱导的脑微血管内皮细胞紧密连接破坏具有协同改善作用(图5)。

图5血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜可上调紧密连接蛋白表达(图源:Wu et al., Neural Regen Res, 2024)
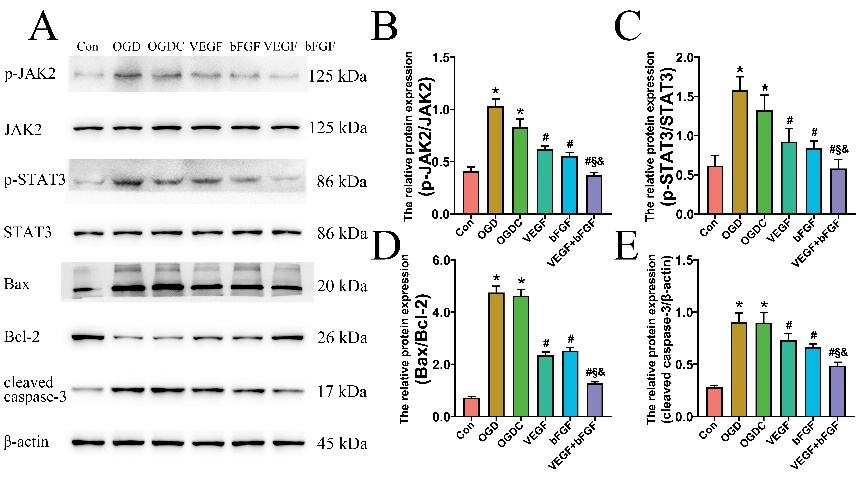
以往的研究表明,JAK2/STAT3信号转导通路可被缺血损伤迅速激活,与炎症反应、神经元凋亡等重要病理过程的调控密切相关[8, 9]。通过Western Blot研究神经血管单元模型中神经元JAK2/STAT3通路的潜在改变。如图6所示,血管内皮生长因子A+碱性成纤维细胞生长因子组磷酸化水平较低。进一步检测了凋亡和抗凋亡相关基因的蛋白表达水平,发现血管内皮生长因子A+碱性成纤维细胞生长因子组中Bax/Bcl-2比率和cleaved caspase-3的表达水平均显著下降。表明血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜可通过抑制JAK2/STAT3通路激活以及细胞凋亡,发挥协同神经保护作用。
 #br#
#br#
图6血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜抑制JAK2/STAT3通路,对神经元发挥抗凋亡作用(图源:Wu et al., Neural Regen Res, 2024)
总之,海舰等成功地建立了一个双生长因子缓释递送系统,该系统由负载有血管内皮生长因子A和碱性成纤维细胞生长因子的纳米纤维膜组成,可以可控的方式持续缓慢地释放血管内皮生长因子A和碱性成纤维细胞生长因子。得益于这2种生长因子的协同作用,这种新型纳米纤维膜通过抑制JAK2/STAT3通路对氧糖剥夺损伤后神经血管单元产生直接的神经保护作用,这可能为缺血性脑血管病提供一种新的治疗策略。
尽管海舰等研究了血管内皮生长因子A/碱性成纤维细胞生长因子纳米纤维膜在氧糖剥夺损伤期间对原代脑微血管内皮细胞、海马神经元和神经血管单元模型的保护作用和潜在机制,但仍需要进一步体内动物研究来证实其结果,尤其是需要使用JAK2/STAT3通路的干预剂。由于聚己内酯纳米纤维材料通常需要超过2年才能在体外完全降解[10],虽体内降解速度会快于体外,但也需要进一步观察其在体内的降解效果。
原文链接:https://doi.org/10.4103/1673-5374.382252
参考文献
[1] Segarra M, Aburto MR, Cop F, et al. Endothelial Dab1 signaling orchestrates neuro-glia-vessel communication in the central nervous system. Science. 2018;361(6404):eaao2861.
[2] Chow BW, Nuñez V, Kaplan L, et al. Caveolae in CNS arterioles mediate neurovascular coupling. Nature. 2020;579(7797):106-110.
[3] Attwell D, Buchan AM, Charpak S, et al. Glial and neuronal control of brain blood flow. Nature. 2010;468(7321):232-243.
[4] Lu H, Li S, Dai D, et al. Enhanced treatment of cerebral ischemia-Reperfusion injury by intelligent nanocarriers through the regulation of neurovascular units. Acta Biomater. 2022;147:314-326.
[5] Geiseler SJ, Morland C. The Janus face of VEGF in stroke. Int J Mol Sci. 2018;19(5):1362.
[6] Xing C, Lo EH. Help-me signaling: Non-cell autonomous mechanisms of neuroprotection and neurorecovery. Prog Neurobiol. 2017;152:181-199.
[7] Barker R, Ashby EL, Wellington D, et al. Pathophysiology of white matter perfusion in Alzheimer's disease and vascular dementia. Brain. 2014;137(Pt 5):1524-1532.
[8] Zhong Y, Yin B, Ye Y, et al. The bidirectional role of the JAK2/STAT3 signaling pathway and related mechanisms in cerebral ischemia-reperfusion injury. Exp Neurol. 2021;341:113690.
[9] Yu L, Zhang Y, Chen Q, et al. Formononetin protects against inflammation associated with cerebral ischemia-reperfusion injury in rats by targeting the JAK2/STAT3 signaling pathway. Biomed Pharmacother. 2022;149:112836.
[10] Zhang P, Han F, Chen T, et al. "Swiss roll"-like bioactive hybrid scaffolds for promoting bone tissue ingrowth and tendon-bone healing after anterior cruciate ligament reconstruction. Biomater Sci. 2020;8(3):871-883.
孙俊和吴一芳为论文共同第一作者,王大鹏和海舰教授为论文共同通讯作者。
 #br#
#br#
海舰,男,主任医师,教授,同济大学附属同济医院神经外科主任,博士生导师。上海市医学会第八、九届神经外科专业委员会委员;上海市医学会第一届脑卒中专业委员会委员。承担国家自然科学基金、上海市卫生局等多项科研课题,在国内外专业性核心期刊上发表学术论文70余篇。2010年获教育部自然科学二等奖。《中华医学杂志(英文版)》、《中华创伤杂志》和多家国际期刊的特约审稿人,国家自然科学基金项目和上海市科委重点项目评审专家。





 #br#
#br#
 #br#
#br#