NRR:浙江大学附属第一医院潘文明和楼险峰团队提出一种适用于脊髓损伤早期治疗的药物:鹰嘴豆芽素A
撰文:李喜功,符菁,管明,石海飞,潘文明,楼险峰
脊髓损伤患者的核心临床症状是由脊髓损伤引起的运动功能障碍[1],其病理变化机制主要分为原发性和继发性损伤机制[2]。脊髓损伤的组织学和神经学损伤主要与继发性损伤有关,包括神经元凋亡、坏死、水肿、炎症反应、活性氧产生等[3, 4]。研究显示,抑制NLRP3炎症小体可减弱脊髓损伤[5],同时,过度氧化应激也是脊髓损伤的关键发病机制,可激活小胶质细胞中的促炎症因子、NLRP3炎症小体和热化作用[6]。甲基强的松龙已被证明可改善急性脊髓损伤的神经系统结果[7],但其存在全身性的副作用,包括脑出血、脑膜炎、可逆性膀胱功能障碍和麻痹[8]。因此,有必要寻找安全、有效、多靶点的抗脊髓损伤药物。
鹰嘴豆芽素A是一种来自豆科植物,如鹰嘴豆和红车轴草的甲氧基异黄酮,具有雌激素样作用[9]。研究表明,鹰嘴豆芽素A可通过抑制细胞凋亡起到神经保护作用[10],也能够抑制Toll样受体4/核因子κB信号通路,从而减轻脂多糖引起的急性肺损伤[11]。Toll样受体4/核因子κB途径与NLRP3炎症小体的合成有关[12]。另外,Nrf2/血红素加氧酶1信号通路的激活可以增强神经细胞对氧化应激的抵抗力,从而保护神经功能[13, 14]。
最近,来自中国浙江大学附属第一院潘文明和楼险峰团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“Biochanin A attenuates spinal cord injury in rats during early stages by inhibiting oxidative stress and inflammasome activation”的研究。文章报道了鹰嘴豆芽素A能够改善脊髓挫伤损伤大鼠的运动功能障碍、脊髓水肿和组织损伤,抑制组织炎症、氧化应激、细胞凋亡和焦亡。鹰嘴豆芽素A能够抑制NLRP3炎症小体及细胞凋亡标志物表达,影响Toll样受体4/核因子κB和Nrf2/血红素加氧酶1信号通路,促进自噬标志物表达。这将为脊髓损伤早期治疗药物的开发提供科学基础和思路。
脊髓损伤的组织学和神经损伤主要与继发性损伤有关,包括神经元凋亡、坏死、水肿、炎症反应和活性氧的产生[3, 4]。因此,潘文明和楼险峰等通过斜面实验和BBB评分法观察脊髓损伤大鼠的运动功能障碍,通过湿干重法观察脊髓水肿,通过酶联免疫吸附法观察脊髓组织炎症因子水平和氧化应激水平。研究结果表明,鹰嘴豆芽素A具有与甲基强的松龙相似的作用,能够改善脊髓损伤大鼠运动功能障碍,减轻脊髓组织水肿,并抑制炎症和氧化应激水平(图1)。另外通过苏木精-伊红、TUNEL和尼氏染色观察组织损伤,结果表明,鹰嘴豆芽素A能够保护神经元,改善组织损伤,并抑制细胞调亡(图2和3)。通过免疫荧光观察组织自噬通量,通过免疫组化观察NLRP3炎症小体、焦亡和抗氧化水平,结果表明鹰嘴豆芽素A可促进脊髓损伤脊髓组织自噬通量和抗氧化水平,抑制NLRP3炎症小体和焦亡(图4和5)。组织实时荧光PCR和Western blot实验结果证明,鹰嘴豆芽素A抑制NLRP3炎症小体、凋亡和焦亡相关蛋白表达,同时促进Toll样受体4/核因子κB和Nrf2/血红素加氧酶1信号通路蛋白的表达(图6和7)。近年来研究表明,Nrf2作为调节细胞氧化应激的保护性转录因子与抗氧化蛋白血红素加氧酶1一起能够增强神经元细胞抗氧化应激的能力[13, 14]。另外Toll样受体4/核因子κB信号通路作为重要的炎症通路之一,能够促进细胞调亡[15]。除此以外,炎症小体的激活促进细胞焦亡,证据表明自噬能够拮抗炎症小体的激活和相关炎症因子的释放和细胞焦亡[16, 17]。该研究结果提示,鹰嘴豆芽素A通过影响Toll样受体4/核因子κB和Nrf2/血红素加氧酶1信号通路参与其保护脊髓损伤后大鼠早期神经细胞的作用。
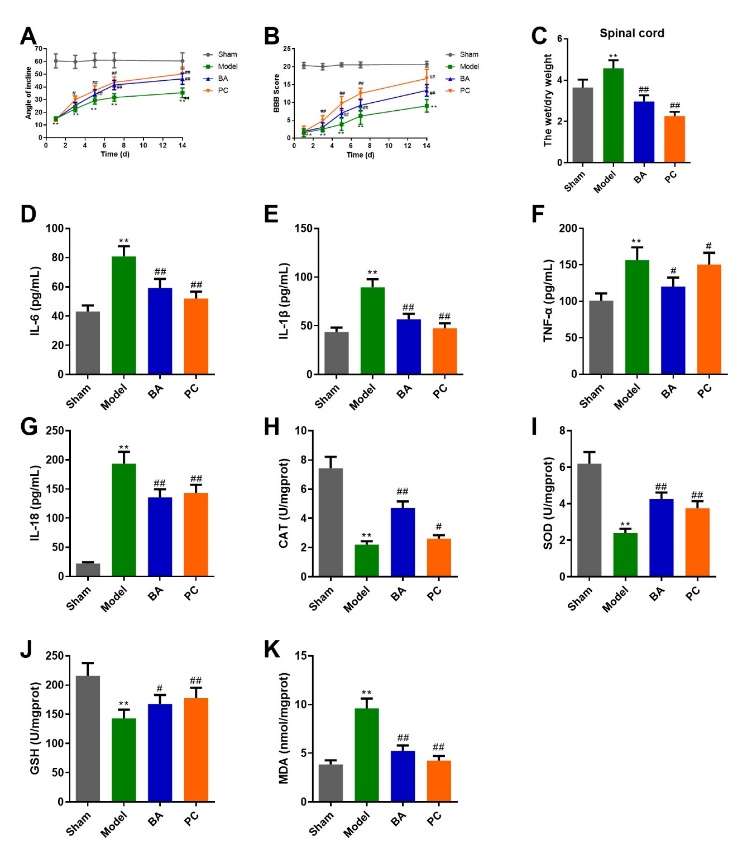
图1鹰嘴豆芽素A对脊髓损伤大鼠后肢运动功能恢复程度、水肿、炎症因子和氧化应激的影响(图源:Li et al., Neural Regen Res, 2024)
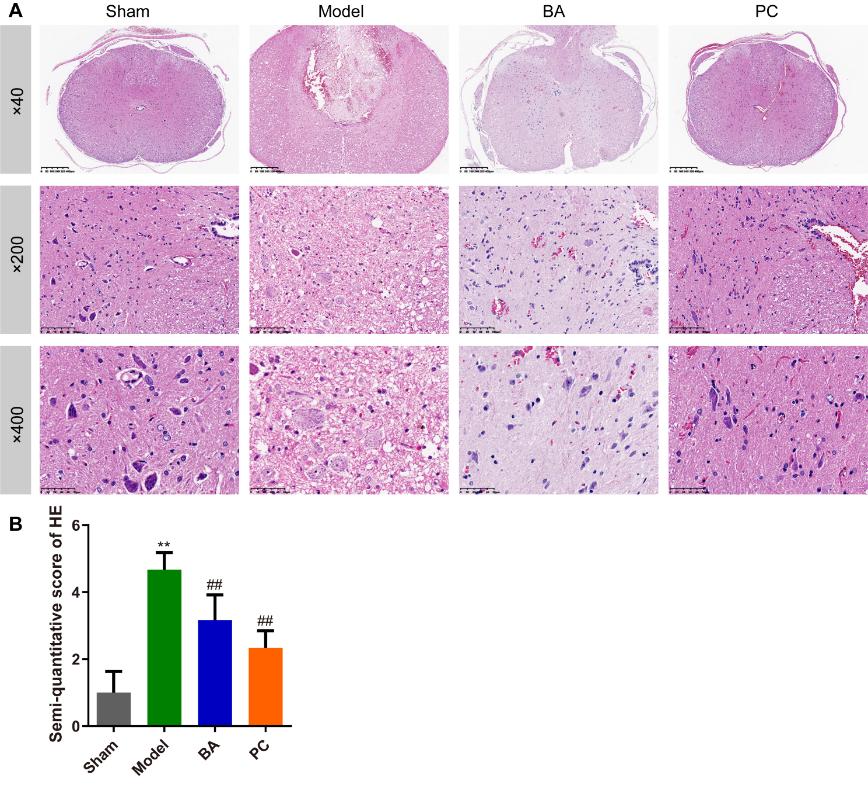
图2 鹰嘴豆芽素A改善脊髓损伤大鼠脊髓的组织病理学损伤(图源:Li et al., Neural Regen Res, 2024)
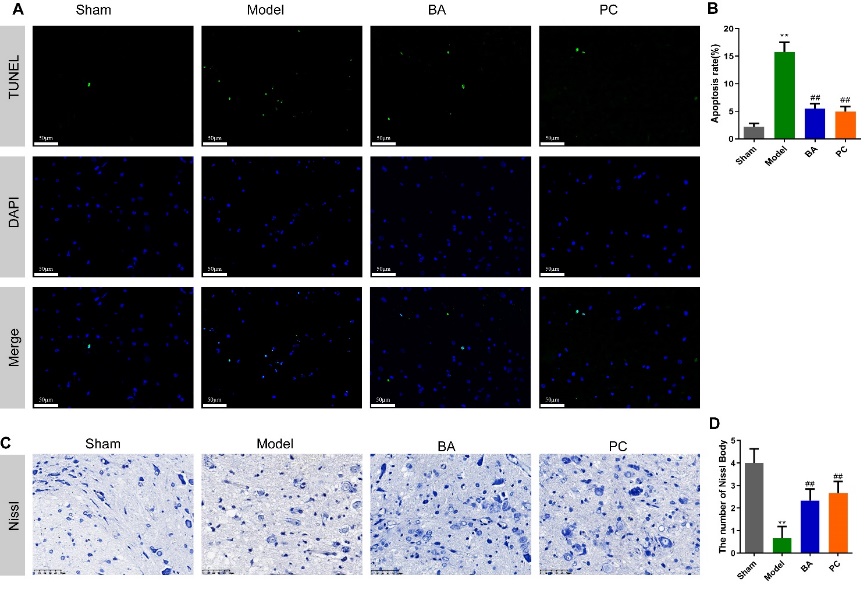
图3鹰嘴豆芽素A对脊髓损伤大鼠细胞凋亡和神经元数量的影响(图源:Li et al., Neural Regen Res, 2024)
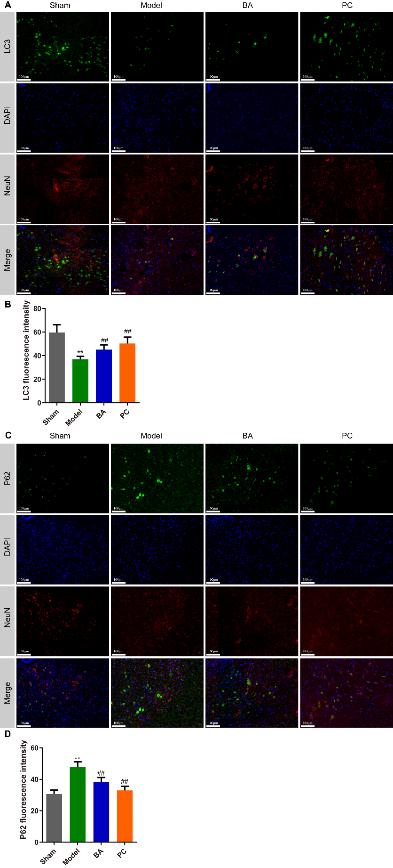
图4 鹰嘴豆芽素A促进脊髓损伤大鼠脊髓组织的神经元自噬(图源:Li et al., Neural Regen Res, 2024)
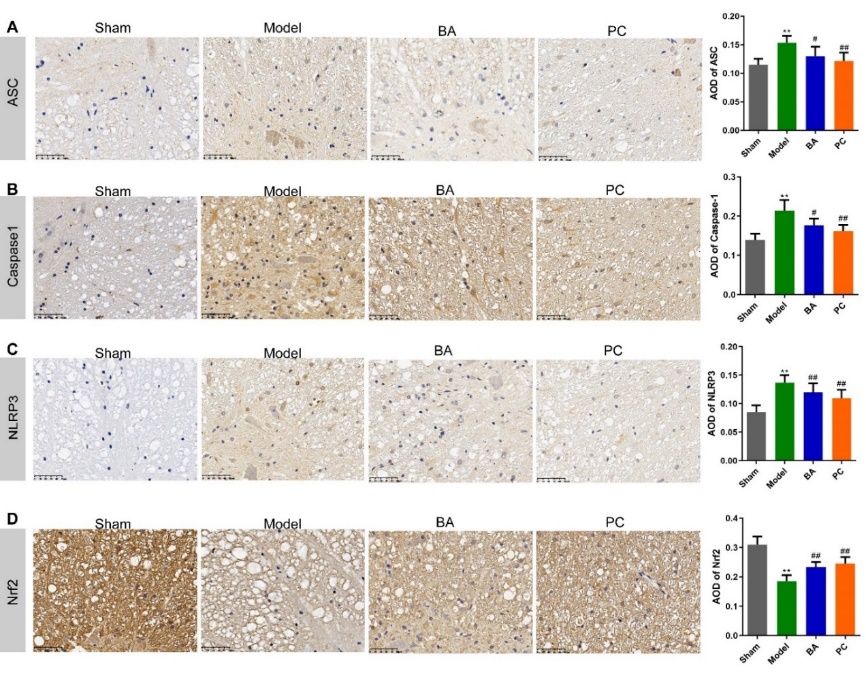
图5鹰嘴豆芽素A抑制脊髓损伤大鼠焦亡,促进脊髓抗氧化(图源:Li et al., Neural Regen Res, 2024)
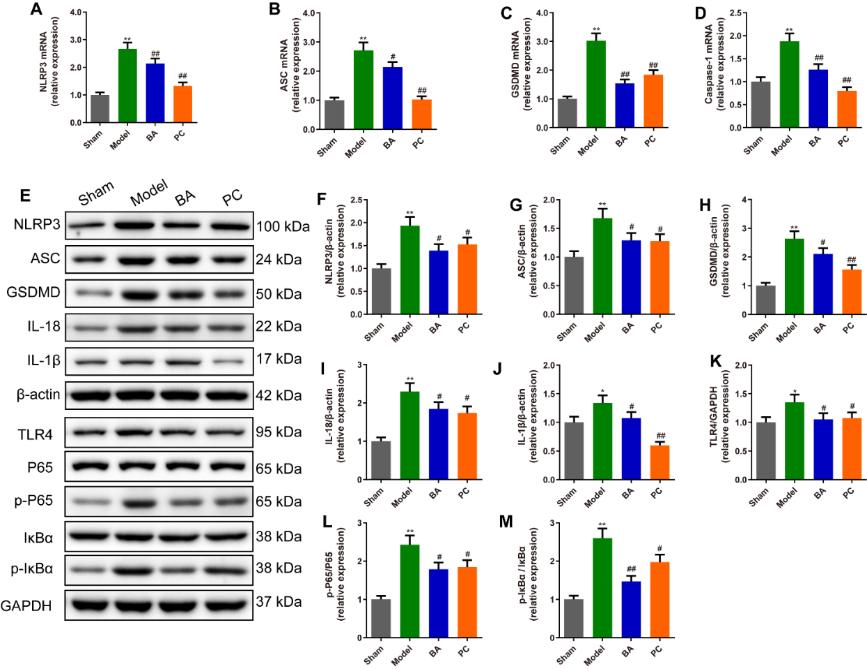
图6 鹰嘴豆芽素A减轻脊髓损伤大鼠脊髓组织中的凋亡和炎症(图源:Li et al., Neural Regen Res, 2024)
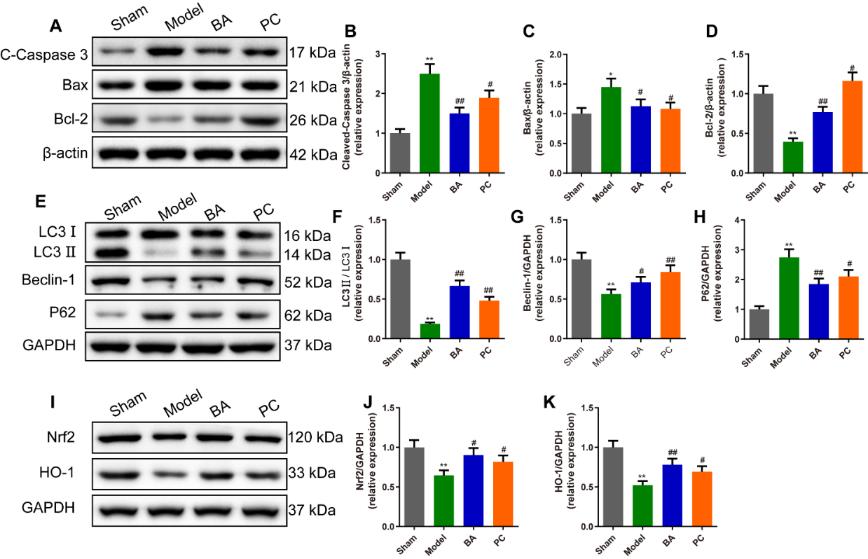
图7 鹰嘴豆芽素A抑制脊髓损伤大鼠脊髓组织中的细胞凋亡和氧化应激,并促进自噬(图源:Li et al., Neural Regen Res, 2024)
总之,鹰嘴豆芽素A对脊髓受损后早期神经损伤的改善是有益的,此作用可能与Toll样受体4/核因子κB和Nrf2/血红素加氧酶1信号通路的调节相关。潘文明和楼险峰等的研究表明鹰嘴豆芽素A治疗脊髓损伤的潜在作用,为临床脊髓损伤药物的开发提供了研究基础和方向。然而临床使用甲基强的松龙治疗脊髓损伤存在全身副作用,限制了其疗效和应用 [7]。因此进一步探究不同剂量鹰嘴豆芽素A的副作用或者其对甲基强的松龙副作用的改善作用是必要的。在脊髓损伤后的早期鹰嘴豆芽素A具有治疗效果,然而临床患者常是长期收到脊髓损伤的困扰,鹰嘴豆芽素A干预的最佳时间节点需要更多研究结果支持。目前大部分对于鹰嘴豆芽素A神经保护作用的研究都局限于细胞实验,此研究提供了鹰嘴豆芽素A在脊髓损伤大鼠模型中发挥保护作用的证据,提示了中药提取物及其中的有效成分在脊髓损伤领域的开发潜力,为鹰嘴豆芽素A改善脊髓损伤提供科学依据。鹰嘴豆芽素A具有进一步探究其给药方式和改良剂型的价值。
原文链接:https://doi.org/10.4103/1673-5374.390953
参考文献
[1] Hurlbert RJ, Hadley MN, Walters BC, et al. Pharmacological therapy for acute spinal cord injury. Neurosurgery. 2013;72 Suppl 2:93-105.
[2] Gu J, Jin ZS, Wang CM, et al. Bone marrow mesenchymal stem cell-derived exosomes improves spinal cord function after injury in rats by activating autophagy. Drug Des Devel Ther. 2020;14:1621-1631.
[3] Zhao SJ, Zhou W, Chen J, et al. Bioinformatics analysis of the molecular mechanisms underlying traumatic spinal cord injury. Mol Med Rep. 2018;17(6):8484-8492.
[4] Ramer LM, Ramer MS, Bradbury EJ. Restoring function after spinal cord injury: towards clinical translation of experimental strategies. Lancet Neurol. 2014;13(12):1241-1256.
[5] Jiang W, Li M, He F, et al. Targeting the NLRP3 inflammasome to attenuate spinal cord injury in mice. J Neuroinflammation. 2017;14(1):207.
[6] Liu Z, Yao X, Jiang W, et al. Advanced oxidation protein products induce microglia-mediated neuroinflammation via MAPKs-NF-κB signaling pathway and pyroptosis after secondary spinal cord injury. J Neuroinflammation. 2020;17(1):90.
[7] Bracken MB. Steroids for acute spinal cord injury. Cochrane Database Syst Rev. 2012;1(1):CD001046.
[8] Canseco JA, Karamian BA, Bowles DR, et al. Updated review: the steroid controversy for management of spinal cord injury. World Neurosurg. 2021;150:1-8.
[9] Sarfraz A, Javeed M, Shah MA, et al. Biochanin A: a novel bioactive multifunctional compound from nature. Sci Total Environ. 2020;722:137907.
[10] Guo MM, Qu SB, Lu HL, et al. Biochanin A alleviates cerebral ischemia/reperfusion injury by suppressing endoplasmic reticulum stress-induced apoptosis and p38MAPK signaling pathway in vivo and in vitro. Front Endocrinol (Lausanne). 2021;12:646720.
[11] Hu X, Qin H, Li Y, et al. Biochanin A protect against lipopolysaccharide-induced acute lung injury in mice by regulating TLR4/NF-κB and PPAR-γ pathway. Microb Pathog. 2020;138:103846.
[12] Majidpoor J, Khezri Z, Rostamzadeh P, et al. The expressions of NLRP1, NLRP3, and AIM2 inflammasome complexes in the contusive spinal cord injury rat model and their responses to hormonal therapy. Cell Tissue Res. 2020;381(3):397-410.
[13] Xu Y, Lu X, Zhang L, et al. Icaritin activates Nrf2/Keap1 signaling to protect neuronal cells from oxidative stress. Chem Biol Drug Des. 2021;97(1):111-120.
[14] Lin W, Chen W, Liu K, et al. Mitigation of microglia-mediated acute neuroinflammation and tissue damage by heme oxygenase 1 in a rat spinal cord injury model. Neuroscience. 2021;457:27-40.
[15] Xie XK, Xu ZK, Xu K, et al. DUSP19 mediates spinal cord injury-induced apoptosis and inflammation in mouse primary microglia cells via the NF-kB signaling pathway. Neurol Res. 2020;42(1):31-38.
[16] Liu Z, Yao X, Sun B, et al. Pretreatment with kaempferol attenuates microglia-mediate neuroinflammation by inhibiting MAPKs-NF-κB signaling pathway and pyroptosis after secondary spinal cord injury. Free Radic Biol Med. 2021;168:142-154.
[17] Biasizzo M, Kopitar-Jerala N. Interplay between NLRP3 inflammasome and autophagy. Front Immunol. 2020;11:591803.






