NRR: 首都医科大学李晓光团队总结新生神经元治疗中枢神经系统疾病的重要作用
中枢神经系统疾病, 如脑创伤、脑卒中、脊髓损伤和神经退行性疾病等, 严重影响人类健康和社会发展, 已成为全球范围内严重的公共卫生问题。中枢神经系统疾病不能治愈的原因,一方面在于中枢神经系统结构的复杂性,更重要的原因在于成年中枢神经系统的神经元缺乏自我再生能力。近年来研究发现,包括人类在内的成年中枢神经系统终生存在内源性神经干细胞(neural stem cells, NSCs)。在生理条件下,内源性NSCs可以不断生成新的功能性神经元,这个过程即为成年神经发生。越来越多的证据表明,内源性NSCs可以对中枢神经系统损伤作出应答反应,表现为NSCs的激活、增殖、异位迁移及分化。遗憾的是,成年中枢神经系统神经发生区占比很小(约全脑的0.01%),并且受损伤局部微环境的影响,损伤本身引起的内源性神经发生反应十分有限,极少量的新生神经元不足以治疗中枢神经系统损伤。因此,如何模拟胚胎发育期、改善损伤局部的微环境、诱导内源性NSCs高比例分化为神经元,是解决中枢神经系统再生的关键科学问题。
近期,首都医科大学基础医学院李晓光教授、杨朝阳教授和暨南大学粤港澳中枢神经再生研究院院长、中国科学院院士苏国辉教授在《中国神经再生研究(英文版)》(Neural Regeneration Research)上2024年XX期发表了题为“Core scientific problem for the treatment of central nervous system diseases: newborn neurons”的综述。该篇文章总结了成年内源性神经发生及其调节机制;讨论了中枢神经系统损伤后内源性神经发生的改变;综述了靶向内源性神经发生和新生神经元治疗中枢神经系统损伤的几种策略,为中枢神经系统损伤的再生修复提供了新的思路。该文章强调了内源性神经发生,尤其是神经元新生在治疗中枢神经系统疾病中的重要作用。首都医科大学基础医学院郝鹏为论文的第一作者,李晓光教授、杨朝阳教授和苏国辉院士为论文的共同通讯作者。
1.成年内源性神经发生
1.1侧脑室室下区神经发生
侧脑室室下区(subventricular zone, SVZ)NSCs主要位于侧脑室侧壁,紧邻纹状体尾状核,终生具有产生神经元的能力。SVZ神经发生过程始于放射状胶质样细胞,即神经干细胞,其通过不对称分裂产生暂时扩大祖细胞,其快速增殖分裂产生成神经细胞(图2)。成神经细胞沿着喙侧迁移流迁移到嗅球,定向分化为嗅球颗粒细胞和球周细胞。

图1. 成年SVZ新生神经元的发育过程。
1.2海马神经发生
海马NSCs位于齿状回颗粒细胞下层,生理条件下,成年海马新生神经元来自放射状胶质样细胞(I型细胞)。I型细胞为静息状态,一旦被激活产生中间祖细胞(2型细胞)。在啮齿类,2型细胞一般存活2周。2周后,存活的2型细胞进一步分化为成神经细胞(3型细胞),3型细胞经过几周甚至几个月的成熟过程,逐渐分化为海马齿状回颗粒细胞(图2)。
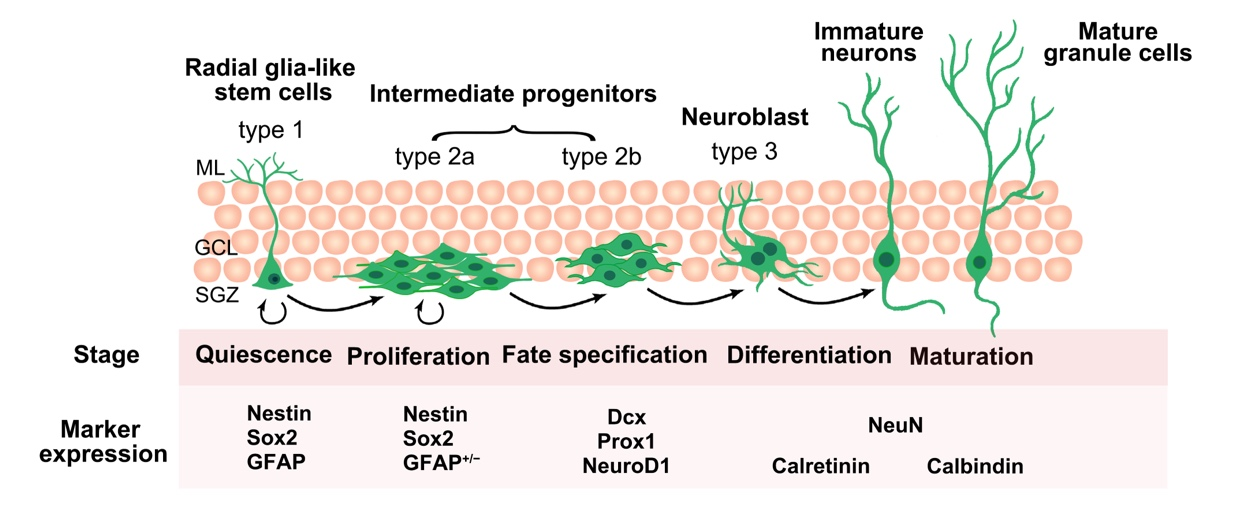
图2 成年海马齿状回新生神经元的发育过程。
1.3成年非人灵长类/人类神经发生
1998年,Eriksson等[1]首次证明成年人脑中存在神经发生。2013年,Spalding等[2]利用14C观察到在人脑海马中存在大量的神经发生,支持了Eriksson等[1]的研究。然而,人脑海马是否存在神经发生在最近又一次受到质疑。2018年Sorrells等[3发现:成年猕猴及人脑内的神经发生数量随着年龄的增长急剧下降,到儿童时期几乎检测不到]。几周后,Boldrini等[4]的研究结果得出相反结论:人脑在整个生命周期都存在着持续的神经发生。在2018-2019年间,科学家对于海马神经发生的方法学研究提出了质疑,上述研究几乎都是应用形态学方法进行观察,然而,应用于啮齿类动物的神经发生相关标记物是否同样适用于灵长类,仍然是存在疑问的。近期,研究者应用单细胞/单核RNA测序方法再一次证明了灵长类脑内存在成体海马神经发生[5-7]。
2.神经发生的调节
2.1内源性因素
NSCs位于神经发生巢,具有特定的分子和细胞特征。成年NSCs巢包括室管膜细胞、血管、未成熟和成熟的NSCs谱系。与非神经发生区相比,成年神经发生区的血管系统具有独特的结构特征,内皮细胞本身及其分泌的因子通过血液运输影响NSCs[8-9]。
NSCs巢内信号的转导触发级联反应,激活细胞内的调节机制,包括转录因子、表观遗传学和代谢。转录因子在调节NSCs 增殖和干性维持、决定 NSCs 命运分化以及神经元发育成熟等方面都发挥着重要的作用。目前研究已发现,影响成年神经发生的一些关键转录因子主要有神经源性碱性转录因子bHLH、Sox、Ascl1、Tlx、CREB等,这些转录因子与其邻近的 DNA 位点相结合,引起转录的激活或抑制,从而调控成年神经发生进程[10]。DNA甲基化、组蛋白翻译后修饰和染色质重塑等表观遗传机制是通过调节基因表达来确定成人神经元分化的重要参与者[11]。
2.2外源性因素
已知报道的明确影响成年神经发生的外源性因素包括丰富环境、衰老和炎症等。Kempermann等[12]首先发现丰富环境可促进成年海马神经发生,同时提高了海马依赖的空间学习记忆能力。相反,衰老对神经发生产生负面影响,导致NSCs急剧且持续地下降[4]。
3.神经发生与中枢神经系统损伤
3.1脑外伤
不同程度的脑外伤对成年神经发生的影响不同,轻度脑外伤对神经发生无明显影响,中度脑外伤促进NSCs增殖而不增加神经发生,重度脑外伤在促进NSCs增殖的同时也增加神经发生[13]。对人类脑外伤患者手术标本进行分析,发现新生神经元相关标记的增加[14],说明脑外伤也可能增强成年人脑的神经发生。
虽然有大量的研究表明脑外伤可以增强内源性神经发生,但其在脑损伤和修复中的作用仍是有争议的。研究发现,脑外伤诱导的海马新生细胞大部分分化为齿状回颗粒细胞,并整合到现有的海马回路中,接受原有神经元的突触输入,改善了大鼠的认知障碍[15]。然而,也有研究报道,脑外伤诱导的内源性增殖反应会耗尽NSCs池,并且新生的增殖细胞表现出各种形态和电生理异常[16]。
3.2脑卒中
3.2.1侧脑室SVZ内源性神经发生的改变
大量研究表明缺血性脑卒中对纹状体神经发生的影响。脑卒中后SVZ细胞增殖显著增加,缺血诱导的成神经细胞迁移到纹状体的严重受损区域,分化为成熟的纹状体神经元,新形成的神经元可以整合到已有的神经网络中[17](图3)。
一些研究发现,脑缺血后大脑皮层可能具有再生能力。成年大鼠皮层缺血性损伤后,SVZ成神经细胞增加,并从SVZ迁移到梗死区周围皮层[18] (图3)。除了动员SVZ NSCs,缺血还诱导新皮质中静止的NSCs的增殖,进而增加了梗死周围区成神经细胞的数量[19]。但目前没有证据显示皮层缺血可诱导产生成熟神经元。

图3. 生理条件下及脑损伤后内源性神经发生的改变。
3.2.2海马DG内源性神经发生的改变
缺血性脑卒中也会增强成年海马神经发生,其特征是海马齿状回中NSCs数量的增加和成熟神经元产生的增多[20]。不伴有海马结构损伤的小区域皮层梗死也能显著促进海马神经发生[21]。与SVZ不同,局灶性脑缺血后,海马中的新生神经元没有向梗死区/缺血半暗带迁移的能力,因此缺血性脑卒中后产生的新生神经元无法替补缺血丢失的神经元。尽管脑缺血后海马神经源性的增强可能是一种代偿性反应,但有相当一部分新生神经元表现出异常特性,并异常地整合到已有的海马回路中[22]。
3.3脊髓损伤
脊髓中央管室管膜细胞具有多能性,被认为是脊髓中潜在的NSCs。脊髓损伤后,成年室管膜细胞快速分裂和增殖,迁出中央管到达损伤区,产生大量的星形胶质细胞参与瘢痕形成,同时产生少量的少突胶质细胞参与轴突髓鞘化[23]。然而,受损伤局部微环境的影响,现有的研究证明单纯的脊髓损伤不能诱导内源性脊髓中央管室管膜细胞分化为神经元[24]。
4.增强内源性神经发生修复中枢神经系统损伤:靶向新生神经元
虽然CNS损伤可以在一定程度上激活内源性神经发生,但其效果十分有限,受损伤局部微环境的影响,激活的NSCs几乎全部分化为胶质细胞,而不是神经元。因此,损伤诱导的内源性神经发生反应不足以修复受损的神经功能。迫切需要一些其他的干预措施来增强内源性修复机制(图4)。

图4. 增强内源性神经发生治疗中枢神经系统损伤的策略示意图。
4.1神经营养因子
4.1.1神经营养因子修复脑损伤
神经营养因子可以促进内源性NSCs的增殖和分化,有助于神经元的生长和突触形成。如静脉注射BDNF可以显著增加卒中大鼠海马的神经发生,同时促进SVZ NSCs向梗死腔周围的迁移[25]。另有研究发现中脑GDNF通过激活STAT3和ERK1/2通路,促进卒中大鼠SVZ NSCs的增殖及向胼胝体和梗死边界的迁移,增加梗死区成神经细胞的募集[26]。
4.1.2神经营养因子修复脊髓损伤
脊髓损伤后将神经营养因子以多种途径递送到中枢神经系统可以促进形态和功能恢复。用于治疗脊髓损伤的最常见的神经营养因子包括BDNF、NT3、NGF、bFGF、IGF和GDNF,这些神经营养因子增加神经元存活、改变胶质细胞表型、促进神经可塑性和轴突再生。
NT3是脊髓损伤后神经元再生和功能恢复中最有效的神经营养因子之一[27]。除了维持感觉神经元、基底前脑胆碱能神经元和运动神经元的存活外,NT3还可以支持多巴胺能神经元的分化,促进皮质脊髓束的侧支发芽[28]。增加NT-3浓度显著改善脊髓功能。当NT3与BDNF等其他神经营养因子联合使用时,可进一步减少红核脊髓束神经元的萎缩和死亡[29]。
4.2生物活性材料
中枢神经系统损伤后,损伤区液化形成空洞,生物活性材料作为支撑结构,为细胞外基质的重建和宿主细胞的迁移创造条件,通过与各种细胞因子或细胞结合,为细胞的存活、增殖和分化提供适宜的微环境,包括促进血管发生、抑制炎症、阻碍病变周围或病变区域胶质瘢痕的形成等。基于以上几个优点,生物活性材料引起了科研人员的广泛关注。
4.2.1生物活性材料修复脊髓损伤
Li等采用天然生物材料壳聚糖复合神经营养因子NT3构建了一种新型活性生物材料NT3-壳聚糖,其可以长期缓释NT3。大鼠急性全断性脊髓损伤后,损伤区内植入NT3-壳聚糖生物活性材料可以激活内源性NSCs,募集其迁移至病损部位分化为成熟的神经元,新生的神经元可与宿主形成功能性神经环路,最终使得功能恢复[30]。随后的研究进一步证明了新生神经元接受来自大脑皮层、皮层下中枢和脊上的轴突投射,新生神经元作为中继站,不仅可以重建脑-脊髓-肌肉神经环路,也能够正确桥接排尿的脑高级中枢和脊髓低级中枢,重建排尿反射神经环路,有效恢复脊髓损伤后的膀胱功能[31, 32]。
更重要的,Li等团队应用NT3-壳聚糖生物活性材料成功修复了成年恒河猴脊髓损伤[27]。胸段脊髓半侧切除后,损伤区植入NT3-壳聚糖可以诱导成年恒河猴皮质脊髓束的长距离再生,越过缺损区(10mm),重新长入远端宿主脊髓(15mm),实现了瘫痪肢体感觉和运动功能长期稳定恢复。
4.2.2生物活性材料修复脑损伤
Li等使用可生物降解的壳聚糖材料结合神经营养因子NT3,将NT3-壳聚糖移植至成年大鼠海马CA1区及以上皮质的损伤区后,生物活性材料持续向损伤局部释放神经营养因子,激活内源性NSCs,使其向损伤区募集、增殖并分化为成熟神经元且整合到宿主的神经环路中,最终导致大鼠认知功能的部分恢复[33]。NT3-壳聚糖促进神经再生的作用与抗炎、促进血管发生有关。
缺血性脑卒中后第5天,将包含有VEGF-肝素纳米颗粒的透明质酸水凝胶直接注射到脑卒中腔内,发现其可诱导脑卒中腔内及卒中腔周围的血管发生和轴突发生,同时促进SVZ成神经细胞的增殖和向卒中腔周围的迁移[34]。最近Li等团队的研究显示,缺血性脑卒中后第7天,将自主研制的bFGF-壳聚糖凝胶植入大鼠的卒中腔内,其可激活SVZ神经干/祖细胞,促进其向卒中腔迁移及新生成熟神经元的生成和长期存活,从而引起脑卒中后的功能恢复[35]。该研究首次成功地在缺血核心区内检测到了神经元新生和血管生成,这可能为缺血性脑卒中的临床治疗提供新的思路。
4.3细胞重编程
最近的研究表明,单一转录因子Dlx2能够诱导成年小鼠纹状体星形胶质细胞重编程为NPCs,进而分化成为多谱系神经细胞,包括神经元、星形胶质细胞和少突胶质细胞[36]。缺血性脑损伤后,使星形胶质细胞过表达Mash1基因,可以将其转分化为非成熟神经元,进而发育为新生成熟神经元[37]。脊髓损伤后,转录因子SOX2可使脊髓固有星形胶质细胞转分化为成神经细胞,进而发育为成熟神经元,形成突触联系[38]。
神经干细胞的发现为利用自体内源性NSCs修复中枢神经系统损伤提供了物质基础。正常情况下,NSCs位于特定的“巢”中,所处的微环境有利于NSCs的增殖、迁移并最终在特定部位分化为成熟神经元。但是,成年中枢神经系统损伤难以修复,一个核心原因是神经元死亡后无法再生;另一个重要原因在于损伤局部的微环境不利于神经元新生。因此,如何有效地促进神经元新生以及如何改善损伤局部的微环境以更好地激活内源性神经发生,是解决中枢神经系统损伤修复的关键问题。文章作者首先综述了脑外伤、缺血性脑卒中、脊髓损伤后内源性神经发生的改变,之后重点综述了增强内源性神经发生治疗中枢神经系统损伤的几种策略,为中枢神经系统损伤治疗提供了新的思路。作者强调了内源性神经发生,尤其是神经元新生在治疗中枢神经系统疾病中的重要作用。
然而,中枢神经系统损伤后的神经再生是一个十分复杂的过程,激活的NSCs如何有效地迁移至损伤区,迁移至损伤区的干细胞如何高效的分化为成熟神经元,并进一步整合入神经环路,这些过程在神经再生中起着关键作用。因此,在利用内源性NSCs促进神经再生时需要考虑如何精准地调控内源性神经发生的各个环节,从而设计出高效的神经再生策略。
参考文献
[1] Eriksson PS, Perfilieva E, Bjork-Eriksson T, et al. Neurogenesis in the adult human hippocampus. Nat Med. 1998;4:1313-1317.
[2] Spalding KL, Bergmann O, Alkass K, et al. Dynamics of hippocampal neurogenesis in adult humans. Cell. 2013;153:1219-1227.
[3] Sorrells SF, Paredes MF, Cebrian-Silla A, et al. Human hippocampal neurogenesis drops sharply in children to undetectable levels in adults. Nature. 2018;555:377-381.
[4] Boldrini M, Fulmore CA, Tartt AN, et al. Human Hippocampal Neurogenesis Persists throughout Aging. Cell Stem Cell. 2018;22:589-599 e585.
[5] Hao ZZ, Wei JR, Xiao D, et al. Single-cell transcriptomics of adult macaque hippocampus reveals neural precursor cell populations. Nat Neurosci. 2022;25:805-817.
[6] Wang W, Wang M, Yang M, et al. Transcriptome dynamics of hippocampal neurogenesis in macaques across the lifespan and aged humans. Cell Res. 2022;32:729-743.
[7] Zhou Y, Su Y, Li S, et al. Molecular landscapes of human hippocampal immature neurons across lifespan. Nature. 2022;607:527-533.
[8] Shen Q, Wang Y, Kokovay E, et al. Adult SVZ stem cells lie in a vascular niche: a quantitative analysis of niche cell-cell interactions. Cell Stem Cell. 2008;3:289-300.
[9] Sun GJ, Zhou Y, Stadel RP, et al. Tangential migration of neuronal precursors of glutamatergic neurons in the adult mammalian brain. Proc Natl Acad Sci U S A. 2015;112:9484-9489.
[10] Vieira MS, Santos AK, Vasconcellos R, et al. Neural stem cell differentiation into mature neurons: Mechanisms of regulation and biotechnological applications. Biotechnol Adv. 2018;36:1946-1970.
[11] Yao B, Christian KM, He C, et al. Epigenetic mechanisms in neurogenesis. Nat Rev Neurosci. 2016;17:537-549.
[12] Kempermann G, Kuhn HG, Gage FH. More hippocampal neurons in adult mice living in an enriched environment. Nature. 1997;386:493-495.
[13] Wang X, Gao X, Michalski S, et al. Traumatic Brain Injury Severity Affects Neurogenesis in Adult Mouse Hippocampus. J Neurotrauma. 2016;33:721-733.
[14] Zheng W, ZhuGe Q, Zhong M, et al. Neurogenesis in adult human brain after traumatic brain injury. J Neurotrauma. 2013;30:1872-1880.
[15] Sun D, McGinn MJ, Zhou Z, et al. Anatomical integration of newly generated dentate granule neurons following traumatic brain injury in adult rats and its association to cognitive recovery. Exp Neurol. 2007;204:264-272.
[16] Neuberger EJ, Swietek B, Corrubia L, et al. Enhanced Dentate Neurogenesis after Brain Injury Undermines Long-Term Neurogenic Potential and Promotes Seizure Susceptibility. Stem Cell Reports. 2017;9:972-984.
[17] Kaneko N, Herranz-Pérez V, Otsuka T, et al. New neurons use Slit-Robo signaling to migrate through the glial meshwork and approach a lesion for functional regeneration. Sci Adv. 2018;4:eaav0618.
[18] Kunze A, Achilles A, Keiner S, et al. Two distinct populations of doublecortin-positive cells in the perilesional zone of cortical infarcts. BMC Neurosci. 2015;16:20.
[19] Ohab JJ, Fleming S, Blesch A, et al. A neurovascular niche for neurogenesis after stroke. J Neurosci. 2006;26:13007-13016.
[20] Woitke F, Blank A, Fleischer AL, et al. Post-Stroke Environmental Enrichment Improves Neurogenesis and Cognitive Function and Reduces the Generation of Aberrant Neurons in the Mouse Hippocampus. Cells. 2023;12.
[21] Kluska MM, Witte OW, Bolz J, et al. Neurogenesis in the adult dentate gyrus after cortical infarcts: effects of infarct location, N-methyl-D-aspartate receptor blockade and anti-inflammatory treatment. Neuroscience. 2005;135:723-735.
[22] Woitke F, Ceanga M, Rudolph M, et al. Adult hippocampal neurogenesis poststroke: More new granule cells but aberrant morphology and impaired spatial memory. PLoS One. 2017;12:e0183463.
[23] Luo Y, Coskun V, Liang A, et al. Single-cell transcriptome analyses reveal signals to activate dormant neural stem cells. Cell. 2015;161:1175-1186.
[24] Li X, Liu D, Xiao Z, et al. Scaffold-facilitated locomotor improvement post complete spinal cord injury: Motor axon regeneration versus endogenous neuronal relay formation. Biomaterials. 2019;197:20-31.
[25] Schäbitz WR, Steigleder T, Cooper-Kuhn CM, et al. Intravenous brain-derived neurotrophic factor enhances poststroke sensorimotor recovery and stimulates neurogenesis. Stroke. 2007;38:2165-2172.
[26] Tseng KY, Anttila JE, Khodosevich K, et al. MANF Promotes Differentiation and Migration of Neural Progenitor Cells with Potential Neural Regenerative Effects in Stroke. Mol Ther. 2018;26:238-255.
[27] Rao JS, Zhao C, Zhang A, et al. NT3-chitosan enables de novo regeneration and functional recovery in monkeys after spinal cord injury. Proc Natl Acad Sci U S A. 2018;115:E5595-E5604.
[28] Joo W, Hippenmeyer S, Luo L. Neurodevelopment. Dendrite morphogenesis depends on relative levels of NT-3/TrkC signaling. Science. 2014;346:626-629.
[29] Ji WC, Li M, Jiang WT, et al. Protective effect of brain-derived neurotrophic factor and neurotrophin-3 overexpression by adipose-derived stem cells combined with silk fibroin/chitosan scaffold in spinal cord injury. Neurol Res. 2020;42:361-371.
[30] Yang Z, Zhang A, Duan H, et al. NT3-chitosan elicits robust endogenous neurogenesis to enable functional recovery after spinal cord injury. Proc Natl Acad Sci U S A. 2015;112:13354-13359.
[31] Hao F, Jia F, Hao P, et al. Proper wiring of newborn neurons to control bladder function after complete spinal cord injury. Biomaterials. 2023;292:121919.
[32] Wang Z, Duan H, Hao F, et al. Circuit reconstruction of newborn neurons after spinal cord injury in adult rats via an NT3-chitosan scaffold. Prog Neurobiol. 2023;220:102375.
[33] Hao P, Duan H, Hao F, et al. Neural repair by NT3-chitosan via enhancement of endogenous neurogenesis after adult focal aspiration brain injury. Biomaterials. 2017;140:88-102.
[34] Nih LR, Gojgini S, Carmichael ST, et al. Dual-function injectable angiogenic biomaterial for the repair of brain tissue following stroke. Nat Mater. 2018;17:642-651.
[35] Duan H, Li S, Hao P, et al. Activation of endogenous neurogenesis and angiogenesis by basic fibroblast growth factor-chitosan gel in an adult rat model of ischemic stroke. Neural Regen Res. 2024;19:409-415.
[36] Zhang Y, Li B, Cananzi S, et al. A single factor elicits multilineage reprogramming of astrocytes in the adult mouse striatum. Proc Natl Acad Sci U S A. 2022;119:e2107339119.
[37] Faiz M, Sachewsky N, Gascon S, et al. Adult Neural Stem Cells from the Subventricular Zone Give Rise to Reactive Astrocytes in the Cortex after Stroke. Cell Stem Cell. 2015;17:624-634.
[38] Su Z, Niu W, Liu ML, et al. In vivo conversion of astrocytes to neurons in the injured adult spinal cord. Nature communications. 2014;5:3338.
主要贡献者介绍

李晓光,首都医科大学基础医学院教授、博士生导师。主要从事应用组织工程修复中枢神经损伤机理和临床转化研究。主持和完成科技部863、国家重点研发计划、国家自然科学基金重点项目等。在国际著名期刊《PNAS》《STTT》《Biomaterials》等发表论文30余篇,获国家发明专利多项,获“2012年全国百篇优秀博士学位论文指导老师”及“2018年高等学校科学研究优秀成果-自然科学一等奖”。

杨朝阳,首都医科大学基础医学院教授、博士生导师。主要从事应用组织工程学方法修复中枢神经系统损伤研究。主持完成科技部重点研发计划、国家自然科学基金面上项目等多项国家级科研项目。在《PNAS》《STTT》《Biomaterials》等期刊上发表论文30余篇。获“2018年高等学校科学研究优秀成果-自然科学一等奖”“2012年全国百篇优秀博士学位论文”“2018年中华医学会-医学科学技术三等奖”。

苏国辉,中国科学院院士,中国医学科学院学部委员,美国发明家学会院士,美国医学及生物工程学会院士,DABI (Dana Alliance for Brain Initiatives)会员,香港大学荣休教授,现任暨南大学粤港澳中枢神经再生研究院院长,香港大学医学院、社会科学学院讲座教授,脑与认知科学国家重点实验室(香港大学)名誉主任,中国脊髓损伤研究协作组董事会联席主席,Neural Regeneration Research杂志总编辑。1977年于美国麻省理工大学获博士学位,致力研究视神经系统轴突再生。1985年首先证实了使用外周神经的移植方法,可以使成年哺乳动物的视网膜节细胞长距离再生。研究方向是使用多渠道的方法,来促进视神经及脊髓轴突再生,致力研究探索神经保护和再生的因素,包括纳米医学、营养因子、运动、中草药提取物、其他一些小分子、免疫反应、康复训练等。1995年获得国家自然科学奖,共发表500多篇SCI论文,拥有专利46项。






